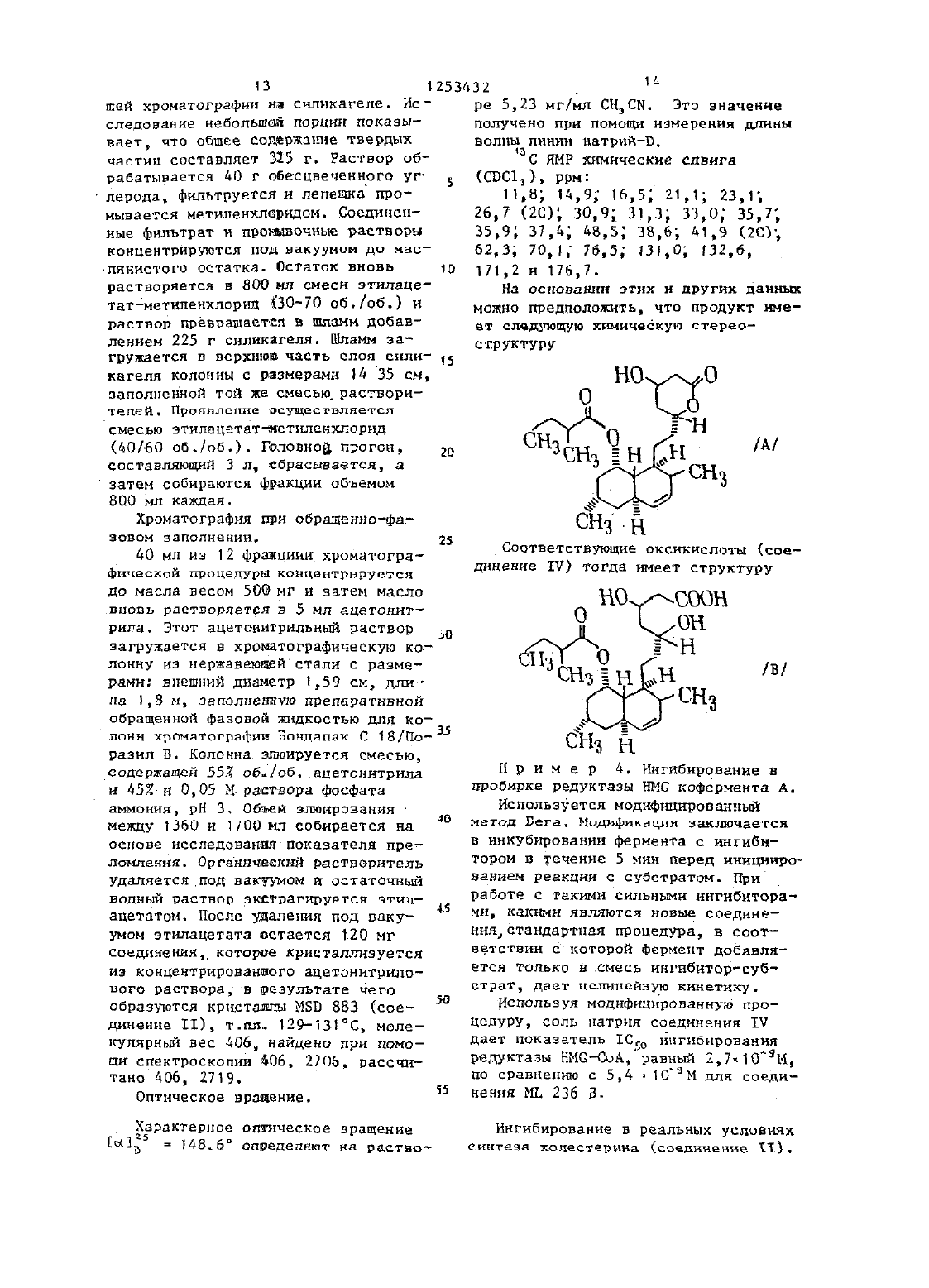
Способ получения оксикислот или их лактонов
Номер патента: 501
Опубликовано: 30.03.1995
Авторы: Карл Х. Хоффман, Генри Йошуа, Ричард Л. Монагэн, Мария Б. Лопез, Альфред В. Альбертс, Джордж Альберс-Сконберг
Текст
Изобретение относится к способу получения новых лекарственных веЭти соединения подавляют биосинтез холестерина И могут быть использованы для леиения атеросклероза,гнперлипемии и других подобных заболевании, а также в качестве противоплесневыш агентов.Оксикислоты или их лактоны получают путем ферментации питательной среды штамом Аврег 5111 п 5 сеггепв АТСС Ю 205 д 2 с последующим выделением соединений из ферментационной смеси экстрагированием растворителем и последовательной хроматографией.(фирма Мерк энд Ко., Инк. Ревей Нью-Йорк) помещен на постоянное хра ение в коплекцшо Американского обрання Видов КулЬтУР 12301, Паркалтн драйв, Роквилл Мэриленд 20852и получил номер по каталог АТССМорфологическая характеристика микроорганизмов АТСС Ю 20542 аналогична морфологическим характеристикам рода Аврег 5111 оэ. В результате сравнения с известньми видами установлено, что штамм принадлежит виду Аврег 5111 цв сеггецэ.Выращивание этого штамма с целью получения новых соединений осуществляется в водной среде, обычной ДЛЯ ПОЛУЧЕНИЯ ДрУГИХ ПРОДУКТОВ Фе ментации. Такая среда содержит источники углерода, азота и неорганичес 55НО О ФК СЪ 11 СНЪ Сне. О НО он СГ 3 1 чКИЕ СОЛИ, КОТОРЫЕ УСТЗНВЗЮТСЛ МИКРОЧ организмами.Углеводы, такие как сахара, например глкоэа фруктоза, мальтоэа,сахароза, ксилоза, МЗНИТОЛ И т.п.,кракмалы, такие как крахмал зерна,например овса, риса. кукурузный крах мал, кукурузная мука крупного по мола и т.п., можно использовать, как по отдельности, так и в комбинацин в качестве.нсточников усваиваемого углерода в питательной среде. Точное количество источника или источников углеводов, которое используется в среде, зависит частичо от других ингредиентов, содержащихся в среде,нов общем случае количество углеводов обычно варьируется В лределак от 1 до 6 вес.2 среды. Источники углерода можно использовать по отдельности или несколько таких неточниковуглерода используется в комбиВ качестве-источников азота в процессе ферментации можно использовать протеиновые материалы. К соответствтющим источникам азота относятся, например, гидролзаты дрожжей, первичные дрожжи, Мука крупного помола соевых бобов, мука семян хлопка гидролзаты казеина, насщенныйиз дНстиллнтораили томатная паста и тп. Источники азота используются либо по отдельности, либо В комбина цни В количествах от 0,2 до 6 вес-1К питательнм неорганическпм солям, которьщ можно использовать в среде для выращивания культуры, относятся обычные соли, содержащие натрнй, калий, аммоний, кальций, фосфат, 5 сульфат, хлорид, карбонат н дРУгие подобные ионы. Они также могут содержать следы металлов, таких как кобальт, марганец, железо и магний.Ферментация осуществляется при -10 2037 С. Однако с целью получения оптимальных результатов ферментация осуществляется при 22-3 ОС. рН питательной сред предназначенной для культивнрованя Аарег 3111 ц 5 и полу 15 чения новых соединений, может варьироваться от 6,0 до 8,0.Хотя новые соединения вырабатываются культурой как на поверхности,так и в погруженном состоянии, про- 20 Цесс ферментации осуществляется в погруженном состоянии. В небольших масштабах ферментация в общем случае ОСУЩЕСТВЛЯЕТСЯ ПРИ ПОМОЩИ ВНЕСЕНИЯ на соответствующую питательную срег 15 ду культуры Азрет 5111 и 5 и затем,после переноса питательной среды с привитой культурой в среду для продуцировання ферментация осуществляется при постоянной температуре 30 около 2890 в течение нескольких дней при периодическом встряхивания.Ферментация инициируется в сте рилизованной колбе со средой при помощи одной или нескольких стадий развития семян. питательной средой для стадии семени может быть любая ПОДХОДЯЩЗЯ комбинация ИСТОЧНИКОВ углерода и азота. Колба с семенами выдерживается в камере при постоянной температуре около 28 С в тече ние двух дней при периодическом встряхнвании или до тех пор, пока рост не достигнет удовлетворительного уровня и часть полученной в результате для прививки потомства второй стадии или среды для продуцирования. Колбы с потомством промежуточных стадий, если таковые используются, культивируются по существу тем же способом, т.е. часть содержиМОГО КОЛЫ СО СТЗДНН ПОСЛСДНЕГО потомства используется для прививки среды для продуцироваипя. Колбы с привитой культурой встряхиваются при постоянной температуре в течение нескольких дней, 3 в конце периода иикубнровапия содержимое колбподвергается центрифугированию или фильтруется.Для реализации в более значительным масштабах ферментация осуществляется в подходящем резервуаре,снаб жеином мешалкой н средствами для аэрации среды ферментации. В соотч ветствин с предлагаемм способом питательная среда загружается в резервуар и стерилизуется при помощи нагревания примерно до 120 С. После охлаждения стерилзованиая среда прививается предварительно выращен-А ньми семенами (потомством) продуцнт рушщей культуры и процесс ферментации продолжается в течение, например, 3-5 дней. Одновременно осуществляется перемешивание и/или аэрация птательной среды и поддерживается температура примерно 28 С. Этот способ биосннтезановых соединений предназначен, в частности, для полученив больших количеств.выделяются из бульона для фермента хдьттт. Соединения 1 и 11 можно под вергнуть гидролизу с основаниями,такими как паон, чтобы получить соли, такие как соли натрия соедниеч ний 111 и 1 Ч. Используя основания с другими прнемлемьши с фармацевтической точки зрения катионами, можно получить соли этих катионов. АккуРатное подкисление солей дает оксикислоты 111 и 1 Ч, которые можно превратить в соединения 1 н 11 при кислотных значений рН. обрабатывая Соединения 1 и 11 при помощи кислотного или щелочного катализа с металлометанолом, этанолом, пропанолом или бутанолом или с фенил, диМЕТНЛЗМННО ИЛН ЗЦЕТИПЗМННО алкалолами получают соответствующие сложные эфиры соединений 111 и ШЧ.Соединения 111 н 1 Ч (особенно 111) можно выделить известным способом без использования хроматографии в форме солей аммония. Такой способ выделения является более удобньм н гораздо больше приспособлен для промышленного использования, чем хроматография. Кроме того,соли соединения 111 и Ч являются гораздо более активными, чем соедИ нения 1 И 11 н реальных условиях С целью ингибирования процесса биосинтеза холестерина и в качестве проти 5 1253 д 32 0воплесневъш агентов. В действительности, оксикислоты (и их соли) являются вктивньми формами. Следователь НО, такие СОЛИ ЯПЛЯЮТСЯ бОЛЕЕ пред ПСЧТНТЛЬНЬЫН, В ЧЕСТНОСТИ,пользовании в форме доз. Кроме солей амония являются и соли тетраметиламмония и соли этилендиамина, натрия калия, кальция, Мччетилглюкамина, лизина, аргинина н орнитина. Указанные соединения являются фармакологически активныи соединениями и могут приеняться как лег карственные препараты стоматнческнм или парентеральным способом в форме капсул, таблеток инъекций и т.п. В общем случае используется стоматический способ применения. Дозы можно варьировать в зависимости от возраста, степени заболевания, веса тела и других факторов человека, но ежедневная доза для возрослого пациента содержится в области примерно от 2 до 2000 мг(в предпочтительном варианте 2100 мг), которая может быть разделена на две - четыре отдельные дозы. При необходимости можно использовать н более высокие дозы. СОЕДИНЕНИЯ МОЖНО также ИСПОЛЬП р и м е р 1. Ферментапил.Поп бирка с лиофилизонаниой культурой Аерст 5111 цв сегтец 5.АТСС н 20542 открывается в стерильных условиях н содержимое суспендируетсп в 250 мл колбу Эрленмайера без перегородки(семенная колба 11), содержащую 40 мл среды С, которая имеет следуюший состав, гНасыенный кукурузный ликер 5Овсяная мука крупного помола 10Среды элементов смеси Ю 2 10РН 6,8 при помощи На 0 Н. Колба с привитой культурой инкубируется в течение 24-48 ч при 28 С на вибратоРе, совершающем 220 кол./мин (размах или амплитуда 508 см). Часть(примерно 0,5 мл) содержимого этой колбы затем используется для прививки культуры в наклонной пробирке,содержащей среду Е. Среда Е имеет следующий состав, грН 7,0 при помощи Па 0 Н.Наклонная пробирка с привитой культурой инкубируетсн н течение 11 дней при комнатной температуре. Затем она хранится при -60 С в течение З-А мес. Часть содержимого этой пробирки затем суспендируется в 25 Омиллилитровую колбу Эрленмайера без перегородки (семенная колба 2),содержащую ДО мл среды С. Колба с привитой культурой инкубируется в течение 24 ч при 28 С на вибраторе,совершающем 220 коп/мин (размах,5.08 см). Приготавлнваются шесть колб Эрленмайера емкостью 250 мл без перегородки, содержащк 40 мл среды С. Затем в каждую колбу прививается культура при помощи 2 мл на каждую колбу содержиого семенной колбы 2. Эти шесть колб инкубируются в течение 48 ч при 28 С на вибраторе, совершающем 220 кол./мин (раз мах 5,08 см). Затем берут шесть двух литровыщ колб ЭрлеНайера содержащих среду Р в объеме 500 мл, н В каждУю колбу прививается культура при помощи содержимого семенной колбы 3. Среда Р имеет следующй состав, гКукуруэная мука грубого помола ТИзмельченные соевые бобы ДКолбы с привитой культурой инкубиршотся в течение 11 дн. без перемешивания при 28 С. После инкубирования в течение 11 дн. бульон подвергается экстрагированию.Весь бульон рн 6,0 смешивается в смесителе Варпнга с тем, чтобы разбить тяжелый слон мицелия, центриФУгируется и прозрачны верхин слой цекантнруется. После фильтрадин 10 л фильтрата экстрагируется при помощи 3 л этилацетата, в результате чего получается 1820 мл прозрачного экстракта. Второе экстрагирование при помощи 3 л этилацетата дает 3350 мл прозрачного экстракта. Твердое вещество бульона экстрагируется при помощи перемешивания в течение 1 ч с использованием 2 л метанола и после фильтрации получается 2100 мл фильтрата.Порции этих экстрактов сушатся и направляются для анализа. Фильтраты испытываются как ингибиторы фермента редуктазы НМС-Сон методом, описанным ВегомСтоником и-Бревером. при этом используются ферменты, полученные в соответствии с опсанием,приведенным Клейнзеком, Рангатамоми Портерон. Положительны тест ин-, гибирование составляет более 902,3 мкг/мл, что указывает на присут ствие очень сильного ингибитора син теза холестерина, действующего насодержание редуктазы НМС-СоА. Результаты анализа экстракта при ведены в табл.1. Т а 6 Л Н Ц а 1Объем, мл Общее содержа Общая акние твердых тивностъ,частиц, мг .ед.2100 13 16 1144067 ГельфилЬтрация. 4 Весь твердый материал, получен НЫ ИЗ ПЕРВЫХ ДВУХ ЭКСТРЗКТОБ, СОЕЩТЗНОЛЕ И ФИПЬТРУЕТСН С ЦЕЛЬЮ удале ния нерастворимых твердых частиц,30 мл фильтрата загружается в колонку для гелевой фильтрации(2,57 200 см, 980 мл), заполненную материалом Сефадекс ЬН-20, н проба фракционируется в соответствии с размером молекул при помощи метанола, который используется в качестве растворителя. испопьэуяиндекс лреломляемостп и данные УФ-анализа,наилучшие фракции определяются при помощи биоаиализа (сМ.табл.2). Т а б л и ц а 2Фракция Общее содер Общая акжание твер- тнвность ед.Выделение и очистка, . проба из фракции 2 предварительнофильтруется через слой В 1 г мате риала Уотерс Бондапак С 18 /Поразил В и элюируется пятью объемами метанола. Метаноловый элюат концентрируется до объема 0,5 мл. Эта проба подвергается хроматографии несколько раз на материале Уотерс С 18,. нз которого изготовлена колонна(3,9 мы 20 см), причем в качестве проявляющего растворителя используется смесь метанол 0,05 М раствор фосфата аммония, рН 2,9, (7525). Фракции исследуются на спектрофотометре Бекманаи те фракции, для которык максимум поглощения соответствует 236 м с изгибами в 229 и 245 нм, соединяются И концентрируются при пониженном давлении до водного раствора. рН концентрата довогчт ся до 6,5 при помощи 2 М раствора гидрата окиси калия и активные компоненты экстрагируются этилацетатом. Органический слой сушится, концентрируется до сухости и остаток раст ворнется в 0,3 мл метанола. Метаноловый раствор подвергается хромато графин и рециркулируется. Фракции,содержащие ранее элюированную компоненту, соединяются, концентрируются до водного раствора и экстрагируются хлороформом. Остаток из хлорофорМЭ. ПОМЕЩЗЭТСП В МЕТЗНОЛ И РЗСТЕОРИ3,5 мг высушенного продукта, полученного такнм образом, идентифицируется как оксикислота (соедине ние 111)фРгКЦИи,соДержащне вторую компоненту, соединяются и экстрагируются хлороформом. Получено 0,87 мг высушенного продукта, который идентифицирован как лактон (соединение 1).(масс-спектроскопия) 404 формула СНдБ 05 (найдено при помощи массспектроскопнн 402,555, рассчитано 404, 2563), УФспектр (в ацетоннтрыла), н 230,5 с як 505,7 237,5 с ЕЕ 576,6 246 с ЕЕ 395,2.ТЗС ЯМР химические сдвиги.Спектр получен в растворе СВ 01, (201 МГ в 0,35 мл). Химические сдвиги приведены относительно внутреннеготетраметилсилана при нуле ррм ПРИ
МПК / Метки
МПК: C12P 1/02, A61K 35/70
Метки: лактонов, оксикислот, способ, получения, или
Код ссылки
<a href="https://by.patents.su/9-501-sposob-polucheniya-oksikislot-ili-ih-laktonov.html" rel="bookmark" title="База патентов Беларуси">Способ получения оксикислот или их лактонов</a>
Предыдущий патент: Способ получения Z-2-ациламино-3-монозамещенных пропеонатов
Следующий патент: Способ получения Z-2-(ациламино)-3-монозамещенных пропеонатов
Случайный патент: Устройство для нанесения покрытий из металлических порошков на внутренние поверхности деталей