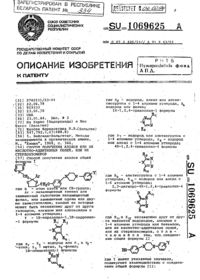
Способ получения хинолонов
Номер патента: 544
Опубликовано: 30.06.1995
Авторы: Раймонд Паркинсон, Давид Брайан Йатес, Джеймс Фрасер, Рой Вистор Давиес, Кеннет Джон Никол, Малькольм Фримен Сим
Текст
1 пазы ь 1 1 Изобретение относится к сннтетн ценна ч. ч затем при комнатной ческой органической химии, а именно температур перемешивание продолк способу получения хинолоиов об дается в течение ночи. Полученная в шей формулы речультате суспензия твердого ве О 5 щества экстрагируется водой (3 О 0 гш) ь ЫШИСНЗ и объем водного экстракта доводится 1 - по 333 мл добавлением воды. Водный.д экстракт, содержащий метил 3 окси Н 2 Ы -2-метилтиоакрилат соль-натрия с.. то (О,33 моль), добавляется в перемеЕ .-511 шиваемый раствор 3-хлордметоксн ь , анилина (52 г) в смеси иоды (8001 чп) где при рнмп или Ц н 11,6 раствора соляной кислоты к. дрд 9 лдд ни (33 мл) при 0 С. Смесь перемешивагг 9 Уь 5 ется 30 мин И продукт собирается К д фтр т 9 ифтрме фильтрацией, в результате чего пот 5 лучается новое промежуточное соеди С 1 С 4 алкил дн ЮдкгрУ- нение метил 3(3-клор 4-метоксиани ат Р д Равно 2 лино)2 метилтиоакрилат, т. пл. 11031 вдРдт на фтр дтрые д 112 С. Выход 77,5 г. Акрилат (776 г) у Обладают РТБгерт 9 нчЕк дан добавляется В днфениловый простой штанам и при введении тешокровньтн эфир (200 ил) , который перемешиваедж животнымв нетоксическнх дотах спи- - ся при 250 С В атмосфере а 30 Та дают 3 ыше дав крви . После перемешивания при 25 ОС в теЦель изобретения - получение но 25 чение 15 мин смесь охлаждается. Повьш биологически активны проиввод- лученный в результате осадок собира НЬШ хинолона. обладающих ценным фар ется фильтрацией, в результате чего иакопогическнм действием. ролучается новое промежуточное соеП р н м е р 1. Диметялсуиьфат динепие 7 хлор-6 метокси 3 метил(22 мл) покапельно добавляется влет 30 тиойхинолои, т. пл. 288290 С. ремешивагмъпо смесь Рхлор-б-метокскч- Выход 7,5 г. Исследование при помо 3 МЕТНПТН 04 ХНН 0 Л 0 Нд (5 д 2 Г 00 щи тонкослойной хроматографии покаДЭРЖЗЩВГО НЕК 0 Т 0 РЕКНПИч 8 ТВ 0 5 эало присутствие небольшого количеКЛОРНЗ 0 М 9 Ра) 5 В 3 В 0 дН 0 ГП Карббнат ства соответствующего 5-хлор изомера. калия (3,2 г) н бутанона (400 мл). . Смесь кипятят при температуре де 5 П р н м е р 2. 7 хлор 6 метоксифпегмирования в течение ночи, а 1-метил-3 метилтнодхинолон (5 г) затем п горячем сосгоянп фильтрут растворяется в дихпорметане (75 мл) ют Горячий фильтрат охлаждают, при и полученный в результате раствора. этом кристаллизуется нрцдукт.7-хлор- обрабатывается покапельно при -20 С 6 метокси 1 метнл 3-метилтио-4- 40 раствором 3 хлорперБензойной кисло хинолон т. пл. 220-222. Выход ты (852, ,2 О 3 г) в дихлорметане й 2,д г. . (75 мл). Реакционная смесь сливается Исходный материал для описанной в настенный водный раствор бикарньше реакции получают следующим боиата натрия (300 мл) и смесь экобразом, Ч 45 страгируется днхлорметаиом (4 х 5 О мл). Натрий (765 г) растворяется в Органический экстракт, не содержабезводном метаноле (д 50 мл) и раст- щий перекиси, сушится н выпаривавор выпаривается до сухости. ется. Полученное в результате тверцполученнй в результате иетилат - дое вещество перекристаллнаовывается натрия суспендируется в безводный 50 из этилацетата, метанола, в резуль. диэтиловый простой эфир (300 мл). тате чего получается 7-хлор 6 метокСуспензия перемешивается при 0 С сн-1-Метнлг 3-метилсульфинилтд-хино и затем в нее покапелъно добавляет лн, т. пл. 263265 С. Выход 0,92 г. ся метил метилтиоацетат (40 г)ь П р и м е р 3. Аналогично приСмесъ перемешивается при ООС в те- 55 меру 1 соответствующие -неаамешен. чение 1 ч, а затем обрабатывается ные хннопоны метилируются резуль. ППКЗПЕЛЬНО НЕТНЛФОПМННТВМ СТ Г)- . тате чего образуются следующие сое Смесь перемешивается при ООС в те днненпя (а)(е). Соединения (Е)(Ь) Лполучают тем же способом, за исключением того, что для соединений(Е)(1) метнлированне осуществляется в водном растворе гидрата окиси калия при 05 С н в водном растворе гидрата окиси натрия при комнатной температуре для соединений (П)ьНеобходимые 1-Н 4 кинолоНЫ для приведенных выше реакций получают аналогично примеру 1. гСоответствующий анилин превращает ся в сложи эфир акрилата формулы Ш, который затем п 0 ДВЕРГается ЦИКПИ зации, н результате чего образуется хииолонформулы Ч.Т . т н( таким способом были получены Аследующие новые промежуточные соеч динеиия, которые приведены в табл.1. П р и м е р Д. Аналогично при-у меру 2 сульфиды (а)(К) ИЗ ПРИМЕРЗ 3 окисляются в следУЮЩНе СУПЬФК сиП р и м е р 5. Аналогично приме ру 1, водный раствор 3-окси 2-метил-чформиата. Этот продукт взаимодействует с Н-метил-3-этиланилиномцукт выделдет экстрагированием этилацетатом, в результате чего получается метил-2(3 этилЫметиланилина)-метилтиоакрилат в виде масла. Концентрированная серная кислота О мл) добавляется пока-в пельно в переметиваемый раствор акрилата (10 г) п уксусном ангидрич де (20 мл) при комнатной температуре, в результате чего смесь закипа-7ет. Смесь охлаждается до комнатной температуры, спивается в смесь лед (вода) 300 мл и экстрагируется этилацетатом (3 х 2 О 0 мл) и затем дихлорметаном (2 х 50 мл). Соединенные экстракты сушатся и выпариваются, в результате чего получается смесь изомеров 5-этил-1-метил-3-метилтио-дтхинопона н 7 этил-1-метнл 3-метилтио 4-кинолоиа, которая выделяется в виде маслянистого твердого вещества. Изомеры разделяются при помощи жидкостной хроматографии при высоком давлении с использованием гилъзы с размерами 5,7 х 30 см,содержащей 325 г силикагеля Выход смешанных изомеров 5,6 г.Элюирование смесью дихлорметаиа иэопропанола (96 д) со скоростью потока 200 мл в минуту дает и 5 оме ры 7 этил--метил-3-метилтио 4 хинолон, т. пп.13840 С, выход,6 г. Продукт крнсталлизуют из толуола и идентифицируют с использованием ЯМР.П р и м е р- 6- Согласно способу, описанному в примере 2, сульфид по примеру 5 окисляют в сульфооксид 7-этил-1-метил-3 метил сульфинипд-иинолбй Т- Пд- 227 22900, выщод 3,6 г из 6,0 г сульфида.Ц р н м е р 7. Используя тот же способ, что в примере 2,реакцию окисления с З-хлорпербензойной кислотой в качестве окисляющего агента 7-фтор-1-метил 3-метилтиод финоло окисляется в дихлорметане при 20 С, в результате чего обра зуется 7-фтор 1 метип 3 метилсульфоП р и м е р 8. По способу, описанному в примере 2, смешаниьт изомерный продукт 16 трнметил-З- 5-метилтно 4 хинолона и ,536 трнметил 43-нетилтио 4 иинолона (1,2 г) окисляют до соответствующего суль фоксида. Продукт очищают с помощью жидкостной хроматографии на силнка- 10геле при высоком давлении, получая(37 д г) циклизуют до получения 6,7 тднметокси 1 метил 3-метилтио-4 хинолина т. пл. 18 Зт 185 С. Выход 6 г. 20(в) Аналогично способу описанному в примере 2, вьшеуказанное соединение(6,62 г) окисляют 3 хлорпербензойной кислотой до получения 6,7-диметоксиЕметипт 3-метилсульфинил 4-хи- 25Терапевтическую активность соединений общей формулы 1 изучают на стандартных лабораторных животных. Такие ИСПЫТЗНИН ВКЛЮЧЗЮТ НЗПРИМЕР,(А) стоматическое применение соединений к группе крыс со спонтанной гипертонией и (В) внутридуоденальное применение соединений к группе крыс с нормальным давлением.В испытании (А) группы из четы рек крыс НЗ 0 ЛИруЮТ 2 На ночь н кровяное давление у ник измеряется слет дующим образом. Крысы помещаются в ящик, в котором поддерживается тем пература 38 С таким образом, что их хвосты торчат из отверстия, продет ланного в ящике.щегося манжета, которы закреплен вокруг основания хвоста. В саном начале в манжете создается давление,превыающее ожидаемое кровяное дави пение, а затем при медленном снижении давления в манжете необходимо следить за появлением артериалънъшДЗЕЛЕНИЕМ- КРЫСЫ НЗВЛВКЗЮТСН ИЗ НЩНЙВВОДНТСЯ. ДОЗЗ НСПЫТЫВВЕМОГО соедине ния в виде раствора или суспензии в 0,252-ном растворе карбоксиметилцеллюлозы. Кровяное давление измеряется спустя 1,5 и 5,0 ч после введения препарата. Соединение опре деляется как активное, если Оно датет снижение кровяного давления на 20 или более на одиомилн ДРУГОМ ИЗ ВЬППЕУПОМННУТЪП ИНТЕВВЗЛОЕчВ тексте (В) группы из трех крыс усыпляются н в сонную артерию ввот днтся трубка, при этом изменяетсякровяное давление.в двенадцатиперст ной кишке злеитроннм средствомартериальной трубкой. Испытуемое соединенне вводится в двенадцатиперст ную кишкуд виде раствора ИЛИ СУСГ пензин в 0 д 252-нон водном растворедавление измеряется перед ВБЕДВНИВМ препарата и спустя 30 мин послевведения. Соединения, которые снижа ют кровяное давление на 10 илиц препарата ОПВЕДЕПЯЮТСЯКЗК ЗКТИВНЬЕЕ дниболее близкую химическую структу ру и обладающм антигипертоинческой активностью, днляетси толеЗ 0 КСНдзане в изобретении, и обнаружено, что он обладает активностью. В тесте 5 А соединения вначале испытывают в д.д дозах 90 мг/кг. Если они денонстрн 07 н руют активности на этом уровне, сле 1 н10 образом, определяют пороговую дозу,при которой соединения активны ввысокой активностью в дозах 90 мг/кг, но неактивные в дозах 30 мг/кг, от 15 носят к соединениям с пороговой ак тивностью 30-90 мг/кг. Аналогичным20 деляют как соединения с пороговой активностью 030 мг/кг. Пороговая 1 НКТНВНОСТЬ ДЛЯ ТОПМЗОКСДЗ Определяется в 30-90 мг/кг. 0 днак 9 дндо-езак 90 мг/кг толмезоксид-дает неже 25 пательные побочные эффекты седатив ности н летаргии .У .некоторын.крыс появилось затрудненное дыхание и они впадают вд просТРаЦИЮ. для 9 соединений определяют СЛЕДУЮЩИЕ ПОрОГОНЬХЕ ДОЗЫ (СМров -9 превосходят толмезоксид так как они либо являются более активными, либо являются активными в тех же дозах, что н толмеаокснд, 40 но не обладают серьезными. вредными эффектами толмеэоксида которые наблюдаются в дозах 90 мг/кг.
МПК / Метки
МПК: A61K 31/47, C07D 215/36
Метки: хинолонов, получения, способ
Код ссылки
<a href="https://by.patents.su/6-544-sposob-polucheniya-hinolonov.html" rel="bookmark" title="База патентов Беларуси">Способ получения хинолонов</a>
Предыдущий патент: Способ получения хинолонов
Следующий патент: Способ получения (1-арилциклобутил)-алкиламинов или их фармакологически приемлемых солей
Случайный патент: Машина для добычи кускового торфа