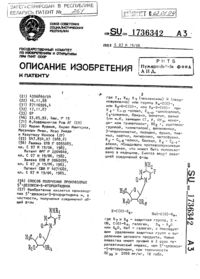
Способ получения 4′-дезокси-13(S)-дигидро-4′-йододоксорубицина
Номер патента: 542
Опубликовано: 30.06.1995
Авторы: Джованни Ривола, Джузеппе Каззинелли, Серджо Мерли, Тереза Бордони
Текст
инов, Новое соединение формулы (П), называемое далее как РСЕ 24883. является полезным в качестве противоопухолевого средства и проявляет активность на экспериментальных опухолях. сравнимую с активностью гГ-дезоксо-ЬГ-йододоксорубицина формулы (1). Субстратомдпя микробно ГО СТЕРЕОСВЛБКТИВПНОГО ВОССТЭНОВЛЭНИЯ ЯВдоксорубицина. Получают целевой продукт формулы ( 1)Морфология мутантного штаптма М 8 Р.1. не отличается от таковой материнского штамма 5. реисетшз АТСС 31428. в то время как обе культуры четко. различаются по своим купьтурапьэ-пьльч и биохимическим характеристикам. Так, мутантный штамм М В 9.1.не ППОДУЦИПуЕТ на ЗГЭРОВОЙ среде ОТ СОЛО.тление-желтого ДО ПИМОННСРЖЭЛТОГО раствоЗИМОГО ПИГМЕНТЭ, КОТОДЬЗЙ ЯВЛЯЕТСЯ характерным для материнского штамма 5. реисесшв АТСС 31428.Кроме того. мутантный штамм М 87 Гг.1. может избирательно превращать соединение (1) в соединение (Н). тогда как материнский штамм 5. реисетйиз АТСС 31428 не избирателен в этом отношении. Это свойство мутанта М 87 53.1. делает его высоко поЛЕЗНЫМ, как ОПИСЭНП В ЗЭЯЕКЕ.ние может бытьосуществл-ено в размножающейся культуре 5. реисеоиэ штамм М 87 Р. 1. при добавлении соединения Ш в качестве субстрата в культуральнуъо среду а инкубационном периоде.Соединение (1) может быть добавлено в форме гидрохлорида после оолкзбчпльчзации в стерильной дистиллированной воде. Куль туру выращивают в питательной среде, содержащей источник углерода. например усваиваемый углевод. и источник азота. т.е. усваиваемое соединение азота или белковый материал. Предпочтительные источники углерода включают глюкозу. сахарозу.тительные источники азота включают настой от замачивания зерна. дрожжевой экстракт. пивные дрожжи. осевую муку, муку из семян хлоп-ка. кукурузную муку. казеин,рыбную муку. сухие остатки дистилляции,животный пептон, мясной экстракт. соли аммония и др. Может быть выгодно испольд аовано сочетание таких источников углерода и азота. . . Процесс биопревращвния может длиться примерно 01172 часов до 8 дней. Инкубационная температура в процессе биопревращения может быть в интервале примерно от 25 С до 37 С.предпочтительно 29 С. Содержимое бродильных сосудов аарируют вабалтыванием -при 250 оборотах в минуту или перемешиванием стерилизованным воздухом. чтобы способствовать росту микроорганизма и таким образомповысить эффективность процесса превра-Ход реакции микробного превращения контролируют взятием образцов бродильной среды при различных временных интервалах и экстракцией при-рН 8.0 смесью дихлорметан-метаптолт в отношении 91. Когда пробу органического экстракта подверга ютто нкослойной хроматографии, испол ьзуя бв качестве элюента смесь хлороформа. ме танола. уксуснойкислотьл и воды в отноше нии 802073 по объему, соединение РСЕ т2488301 появляется при значении Н среды 0.50. тогда как 4-дезокси-А-йододоксорубицин (1) находятпри.НГ 0,60. Количественное определение двух антрациклинов может быть осуществлено после тонкослойной хроматографии с упомянутой выше злюируЮЩЕЙ СИСТЕМОЙ, СОСКЭБЛИВЗНИЕМ И ВЬЪМЫВЭ нием метанолом соответствующих зон с красным окрашиванинш и конечным спектрометрическим определением при 496 нанометрах. к Весь ферментационный бульон. в кото ром соединение подвергается превраще нию в соединение РСЕ 24883 (Н). фильтруютс помощью диатомовой земли. Отфильтрованный красный мицелий экстрагируют вмешивающимся с водойуортаническим растворителем. таким как метаноли другие низшиеспиртья, диоксан, ацетонитрьт и предпочтительно ацетон. Экстракты мицелиясобирают. концентрируют при пониженном т давлении И объединяют профильтрованнойферментационной жидкостью. устанавливают рН 80, затемьэкстрагирухот невмешивающимся с водой органическим растворителем. таким как н-бутанол, хлороформ. дхихлорметан или предпочтительно смесь диклорметан-метанол в отношении 91. Органические экстракты содержат сое 5динение РСЕ 24883 вместе с соединением имебольшими количествами других продуктов разложения.при пониженном давпениидосуха и остаток растворяют в дихлорметане и хроматографируют на колонке силикагеля. стабилизированного буфером срН 7.0 градиентом СМЕСИ дихлорметан-метанол-вода. СОВДИ нение вымывают первым смесью в отно 10шении 955 О,25 затем соединение РСЕ в 24883 (П) смесью в отношении 90100,5. Изобъединенных фракций после промывкиобъемов в присутствии н-лропанола. добав ления эквивалента хлористоводородной кислоты и избытка н-гексана. получают преципитат чистого РСЕ 24883 (Н) в виде гидрохлорида (НЕ)РСЕ 24885, (П) как свободное основание вгидрохлорид (Ш) растворим вводе, но мало растворим в органических растворителях. Гидрохлорид соединения СЕ 24883 имеет следующие физико-химические свойства . А Точка плавления 200 С 2(разлагается) удельное вращение а 1029 188 (с 0,05. метанол). а у Спектр поглощения вУФ и видимой области Н 2 О Макс 232, 254, 290 И 480 нано метров с ед 492, 370. 127, 103) ИК-спектр (КВт) пики при следующихСпектр ЯМР на ядрах ТН-ДМСО-ов, 200 С(до. А 6,0, 15,3 Гц, 1 Н, Н-В акс). 1,71.9 (м. 2 Н, СН 2-2) и 1,14 (д. Ц 6,0 Гц). ЗН. СНз-Б молекулярная формула СитнзоМю-НСЪ тп/2 в В эквиваленте к свободному основанию 656 (МНУ Б 55 (М) и 410 (МЙ, соответствующие агликону. - ,Селективная жидкостная хроматография высокого давления позволяет разделить (два максимума с временем задержки 18.8 и 1 О,3 минут) два стереоизомерныхИОДОДОКСОРУИЦИНЭ . ПОЛУЧЕННОГО БОСС новлением йода боргидридом натрия. Используя-тот же метод жидкостной хроматографии высокого давления, получают соединение РСЕ 24883 (Н) как отдельный пик с временем задержки 19,3 минуты, соответствующим времени медленно движущейся состааляюцдеп синтетического13-дигидропрои 3 водного. в . Метод жидкостной хроматографии высокого давления, Колонка две секции ПР сфе рисорб 5 300 5-2 (С 1 8 Зд. разделение фаз Великобритания размером 150 х 4,5 мм,соединенные в рядгтемпературта .45 С мо бильная фаза А 0.05 М водного КН 2 РО 4. лподкисленного дорН 3.0 смесью Н 3 Р 04-метанол в отношении 802 по объему подвижная фаза В метанол проявление,изократное за 30 минут (42 А 58 В) скот ростъ потока 0.6 мл/минъдетектирование 254 нанометра. Кислотный гидролиз соединения (Н)-(О,2 н. хлористоводородная кислота, 80 С,30 минут) дает красный осадок соответствующего агликона, тогда как сахарная компонента, а именно 3-амино-2,3,4,Б-тетрадеэокси-4-иод--ликсогексогексоза, присутствует в водной фазе и идентифицирована в сравнении с аутентичным образцом, попученным при кислотном гидролизе соединения .ния РСЕ 24883 испытывают Пп ийтго на клеткак Неаи Р 388 в сравнении с соединениемАктивность Зп уйуо соединения РСЕ 24883 (Н) испытывают против рассеянного лейкоза Гросса. Мышам линии СЗН вводят внутривенно инъекцию 2-106 клеток на мышь, обрабатывают соединениями и изу дют 24 часггпосле опухолевой инъекции.При оптимальной дозе соединение РСЕчйододоксорубицин (1), с малой токсичностью, проявленной при активных дозах. Противо опухопевую активностьсоединения (1 П), оцененную как среднее время выживания обработанных животных над контрольными мышами, можно сравнить с активностью соединения (1) и доксорубицина (табл. 2)Способ иллюстрируется следующими примерамиП р и м е р 1. Культуру микроорганизм Зтгертогпусез реисетшв штамм М 87 17.1. (О М 2444) ыращиваюттзд дней при 28 С на скошенном агаре следующей поддерживающей среды (Среда/д) глюкоза 3. пивные дрожжи 1,2 МаС 1 0,1, КН 2 РО 4 0.05. СаСОз 0,1 11119504 0.005 РеЗОА-/Ня-О о,ооо 5 2 п 5 О 47 Н 2 О о.ооо 5 Си 3 Ол 5 Н 2 О0000535 агар 2, водопроводная вода до100 мл, рН 0,7. Стерилизацию проводят нагреванием в автокл-аве в течение 20 минут. , у с ,Споры вьтращенной культуры собирают и суспендируют-в 3 мл стерильной дистиллированной водыДЭтойсуспенаией засева 10на твердой питательной среде, как описано в примере 1. Споры трех скошенных агаров объединяют и собирают в 10 мл стерильной дистиллированной воды. Полученную таким образом суспензию высевают в 2-х л опрокидывающиеся колбы с круглым дном, содержащие 500 мл посевной среды. описанной впримере 1. Колбу инкубируют 48 часов на роторной мешалке. вращающейся со скоростью 1-20 об/мин и описывающей окружность диаметром 7 см, при температуре 28 С. Весь посевной материал инокулиру ют в 10 л бродильный чан из нержавеющейстали, содержащий 7,5 п биотрансформирующей средьи. описанной в примере 1 и стерилизова-нной водяным паром при 120 С в течение 30 минут. Раствор глюкозы стерилизуют отдельно и добавляют в стерилизованный бродильный чан в- соответствующей концентрации. Культуру выращивают при 28 С при помешивании 6230 об/мин и аэра ции потоком воздуха со скоростью 1 п/лют 60 мл жидкой питательной среды, содержащейся в 300 мл колбах Эрленмейе ра пивные дрожжи 0,3. пептон 0,5, Са(МОз)-4 Н 2 О 0.05, водопроводная вода-ниемв автоклаве при 120 С в течение 20 ,минут, рН этой среды после стерилизации устанавливают междУ 5-8 и 7,0.Инокулиро 1 ванные колбы встряхивают два дня при тем пературе 289 С на роторной мешалке при 250 об/мин. описьквающей окружность диаметром 7 см. 1,5 мл культуры, выращенной описаннымспособом, высевают в 300 мл колбы Эрленмейера. содержащие 50 мл спедующей биотрансформирующей среды дрожжевой экстракт 1,5, К 2 РО 4 025,глюкоза. 1,5, водопроводная вода до 100 мл, рН 6,9, стерилизацию проводят нагреванием в автоклаве при 115 С в течение 20 минут. Раствор глюкозы стерилизуют отдельно и добавляют к каждой стерилизованной колбев нужной концентрации.Затем содержимое колб инкубируют при к28 С в условиях, описанных для фазы посева,-в течение 24 часов. В это время в каждую колбу добавляют по 1,0 мл раствора соеди нения (П) в стерилизованной воде в концентра ции. 5 мг/мл. Встряхиваемые колбы инку бируют еще два дня и получают 70-оебпревращение соединения (1) в соединение (Н).среды /ми-н, Ч ерез 48 часов добавляют субстратное соединение в концентрации,описан-ной в примере 1, иппосле инкубировения культуры втечение 3-х дней получают БОЗС-ную конверсию соединения (1) в соединение (Н). . .у П р и м е р 3. Цельное сусло (5 п) из ферментации. полученной по примеру 2. фильтруют с использованием 2 диатомо вой земли в качестве фильтра. Влажный осадок на фил ьтреэкстрагируют ацетоном (3 п). После фильтрации проводят две дополни ТЕЛЬНЫХ ЭКСТРЭКЦИИ ЭЦЕТОНОМ ДЛЯ ДОСТИЖВния полного выделения красных пигментов. Объединенныефацетоновые экстракты концентрируют при пониженном давлении и концентрат (1 л) обьединяют с профильтрсваннымбульоном и исчерпывающеэкстрагируют при рН 8.0 смесью дихлорме таи-метанол в отношении 9 1. Органический экстракт. содержащий соединения (1) и (Н) с теми же продуктами распада, кон центрируют досуха при пониженном давлении. Остаток. растворенный в дихлорметане,хроматографируют на колонке силикагеля,стабилизированного буфером с рН 7,0дихлорметанметанол-вода После вымывания некоторых, продуктов распада элюируют соединение смесью в отношении 95510.25 с последующим элюированием соединения РСЕ 24883 (Н) смесью в отношении 901005, 1 Из объединенных фракций после про мывки водой. концентрации до небольшогоА объема в присутствии н-пропанопа, добав ления одного эквивалента хлористоводородной кислоты и ьтзбытка н-гексанаполучают чистое соединение РСЕ 24883 (П).П р и м е р 4. Образец соединения РСЕ 24883 (Н) 200 мг растворяют в 0.2 н. водной хпористоводородной кислоте (50 мл) и нагревают 30 минут при 1-00 С. Кристаллический красный осадок (0 д 2 г)- агликона собирают фипьтрациегм промывают водой и сушат. Масс-спектр т/е 41.5 (МЧ Агликонзаключающийся в том. что 7 штамм Зггеототусэз реисеииз ВЗМ 2444 культивиВУЮТ. в аэробныхоусловиях в питательной среде. седепжащай источники азота и угдеРОДа И Минеральные соли. в присутствии 4 ДВЗОКСИ-Ф-йододоксирубицина в форме его хлоргидрата в конечной концентрации 0-1 МГ/Мд Среды при температуре 274 З 0 С полученную культуральную жидкость разде ляют. отделенный мицелий экстрагируют - ЗЦЕТОНОМ.ажидкуюфаэусмесьюндихлорме р тана и метанола в объемном соотноше идентифицирован как 13 д 5)-дигидроадриа- мицинон сравнением с аутентичным образцом. л а Феормула изобретения 1. Способ получения 4 дезокси-13(З)дигидро-Щ-иододоксорубицина формулыНИИ 931 ПРИ П 8.0. далее полученные экстракты объединяют и концентрируют при пониженном давлении до сухого-состояния,Затем КОНЦЕНтрат растворяют в дихлорме Тане И ХРОМНТОГП-афи-руют наколонке из силикагеля, забуференного до рН 7 оэлэоируют последовательно смесью дик.лорметана. метанола и воды при объемддм соотношении 95251125 901005 сватаетственно. полученный второй зпъоат конценТПИРУЮТ о присутствии н-пропгнппа,ВЫДЭЛЯЮТ целевой продукт и переводят в форму его хлоргидрата. оАа)доза дающая 50 снижение числа клеток а сравнении с контрольными необработан ными животнымито) клетки эпитепиоидной карциномы шеи человека
МПК / Метки
МПК: C12P 1/06
Метки: получения, способ, 4'-дезокси-13(s)-дигидро-4'-йододоксорубицина
Код ссылки
<a href="https://by.patents.su/6-542-sposob-polucheniya-4-dezoksi-13s-digidro-4-jjododoksorubicina.html" rel="bookmark" title="База патентов Беларуси">Способ получения 4′-дезокси-13(S)-дигидро-4′-йододоксорубицина</a>
Предыдущий патент: Композиция для дезинфекции семян
Следующий патент: Подвижная шпалоподбивочная машина
Случайный патент: Многослойное пассивирующее покрытие для высоковольтных полупроводниковых приборов