Способ кристаллизации производного тетрагидропиридина и полученные кристаллические формы
Текст
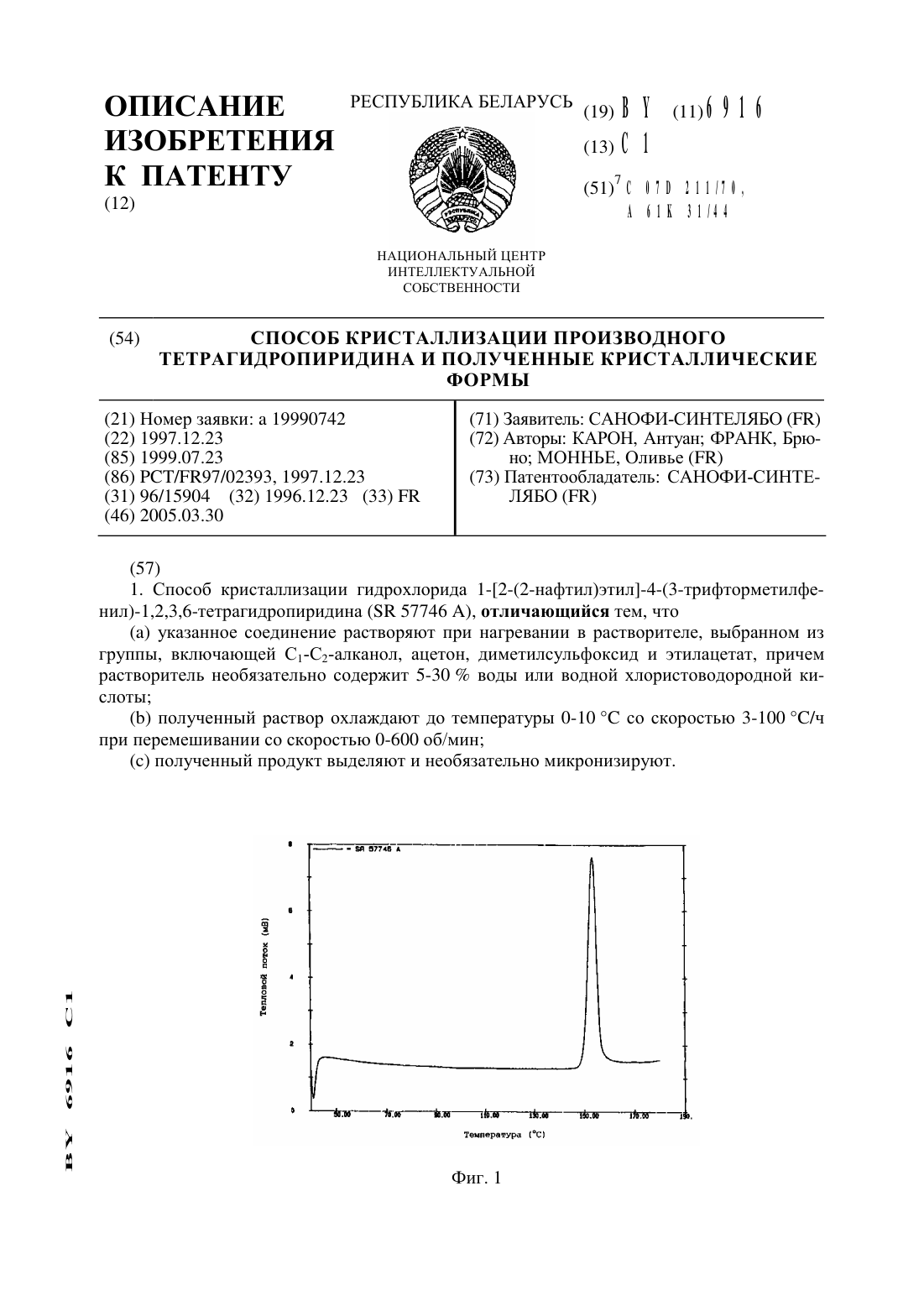
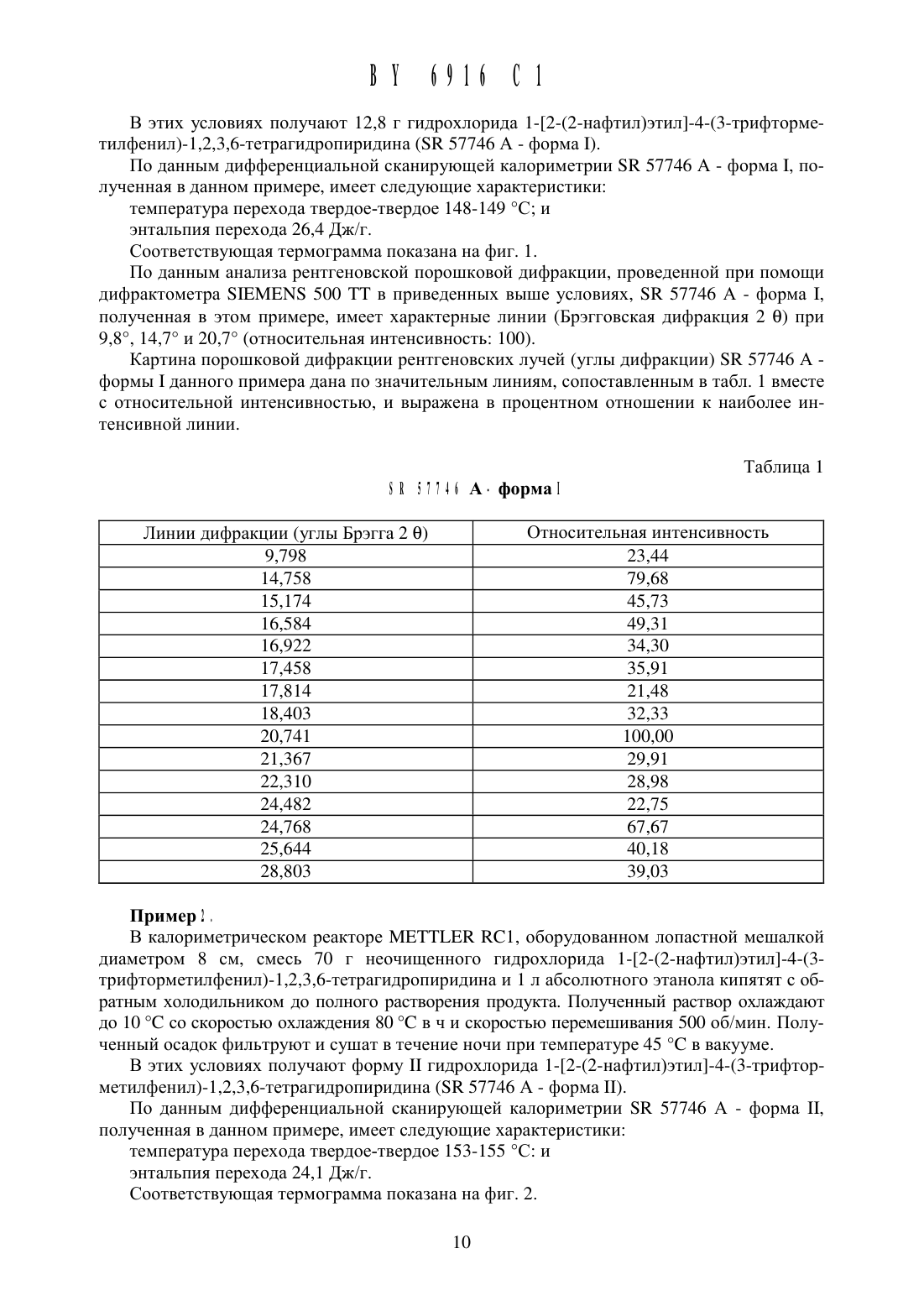
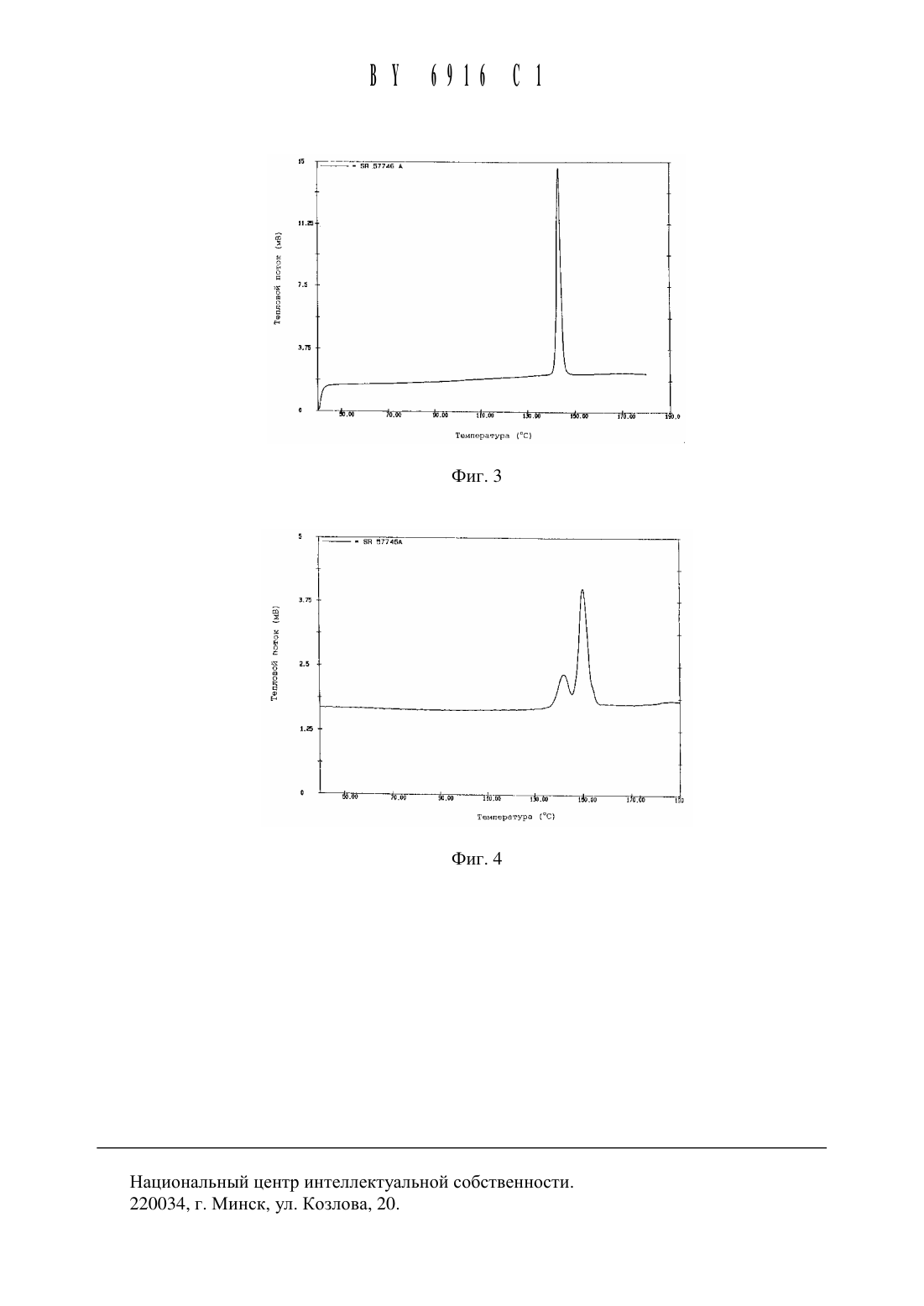
2. Способ по п. 1, отличающийся тем, что на стадии (а) ЭК 57746 А растворяют в смеси этанола И хлористоводородной КИСЛОТЫ, взятых в соотношении 9525, при кипячении с обратным холодильником до полного растворения, на стадии (Ь) полученный раствор охлаждают до температуры около 4 С при температурном градиенте 3-100 С в час без перемешивания и на стадии (с) выделяют форму 1 гидрохлорида 1-2-(2-нафтил)этил-4(3 -трифторметилфенил)- 1 ,2,3 ,6-тетрагидропиридина.3. Способ по п. 1, отличающийся тем, что на стадии (а) ЭК 57746 А растворяют в абсолютном этаноле или смеси этилацетата и воды, взятых в соотношении (955)-(9010),при кипячении с обратным холодильником до полного растворения, причем указанное соединение присутствует в концентрации 10-80 г/л в смеси этилацетата и воды или 5-150 г/л в абсолютном этаноле, на стадии (Ь) полученный раствор охлаждают до температуры около 5-10 С при температурном градиенте 30-100 С в час со скоростью перемешивания 100-600 об/мин и на стадии (с) выделяют форму П гидрохлорида 1-2-(2-нафтил)этил-4(3 -трифторметилф енил) - 1 ,2, 3 ,6-тетрагидропиридина.4. Способ по п. 1, отличающийся тем, что на стадии (а) ЭК 57746 А растворяют в диметилсульфоксиде при кипячении с обратным холодильником до полного растворения, на стадии (Ь) полученный раствор охлаждают при температурном градиенте 3-100 С в час со скоростью перемешивания 0-600 об/мин и на стадии (с) выделяют форму 111 гидрохлорида 1- 2-(2-нафтил)этил -4-(3-трифторметилфенил)- 1 ,2,3,6-тетрагидропиридина.5. Способ по п. 1, отличающийся тем, что на стадии (а) ЭК 57746 А растворяют в метаноле или в смеси этанола и воды, взятых в соотношении (9010)-(7030), или в смеси ацетона и воды, взятых в соотношении 9010, при кипячении с обратным холодильником до полного растворения, на стадии (Ь) полученный раствор охлаждают до примерно 5 С при температурном градиенте около 10 С в час и со скоростью перемешивания около 400 об/мин и на стадии (с) выделяют смесь форм 1 и П 1 гидрохлорида 1-2-(2-нафтил)этил -4(3-трифторметилфенил)-1,2,3,6-тетрагидропиридина в соотношении (8020)-(6535).6. Способ по п. 5, отличающийся тем, что на стадии (а) используют смесь этанола и воды, взятых в соотношении 9010, на стадии (Ь) полученный раствор охлаждают до температуры около 5 С при температурном градиенте около 10 С в час со скоростью перемешивания около 400 об/мин и на стадии (с) выделяют смесь форм 1 и П 1 гидрохлорида 12-(2-нафтил)этил-4-(3-трифторметилфенил)-1,2,3,6-тетрагидропиридина в соотношении около 6634.7. Способ по любому из пп. 1-6, отличающийся тем, что используют лопастную мешалку.8. Форма 1 гидрохлорида 1-2-(2-нафтил)этил-4-(3-трифторметилфенил)-1,2,3,6 тетрагидропиридина, полученная способом по п. 2.9. Форма П гидрохлорида 1-2-(2-нафтил)этил-4-(3-трифторметилфенил)-1,2,3,6 тетрагидропиридина, полученная способом по п. 3.10. Форма П 1 гидрохлорида 1-2-(2-нафтил)этил-4-(3-трифторметилфенил)-1,2,3,6 тетрагидропиридина, полученная способом по п. 4.11. Смесь формы 1 и формы 1 П гидрохлорида 1-2-(2-нафтил)этил-4-(3-трифторметилфенил)-1,2,3,6-тетрагидропиридина, полученная способом по любому из пп. 5-7.12. Кристаллическая форма по п. 11, отличающаяся тем, что она микронизирована.характеристические линии рентгенограммы порошка (Брэгговские углы 26) прихарактеристические линии рентгенограммы порощка (Брэгговские углы 2 6) при17. Смесь по п. 16, отличающаяся тем, что соотношение формы 1 и формы П 1 составляет около 6634.19. Фармацевтическая КОМПОЗИЦИЯ, обладающая антинейродегенеративной активностью, содержащая в качестве активного ингредиента гидрохлорид 1-2-(2-нафтил)этил-4(3-трифторметилфенил)-1,2,3,6-тетрагидропиридин в необязательно микронизированной кристаллической форме, выбранной из формы 1, формы П, формы П 1 и смеси формы 1 и формы 1 П по любому из пп. 8-17.20. Композиция по п. 19, отличающаяся тем, что в качестве активного ингредиента содержит смесь по п. 18 в виде единичной дозированной формы.21. Композиция по п. 20, отличающаяся тем, что каждая единичная дозированная форма содержит количество микронизированного активного ингредиента, которое соответствует дозе, выбранной из 0,5 1 1,5 2 2,5 и 3 мг свободного основания.Данное изобретение относится к способу кристаллизации производного тетрагидропиридина, к новым кристаллическим формам, полученным данным способом, и к фармацевтической композиции, содержащей указанное производное тетрагидропиридина в данной кристаллической форме в качестве активного ингредиента.Данное изобретение более конкретно относится к способу кристаллизации гидрохлорида 1-2-(2-нафтил)этил-4-(3-трифторметилфенил)-1,2,3,6-тетрагидропиридина, к трем кристаллическим формам данного продукта, к определенной смеси двух из трех данных форм и к фармацевтической композиции, содержащей одну из указанных форм или смесь двух из данных форм.1-2-(2-Нафтил)этил-4-(3-трифторметилфенил)-1,2,3,6-тетрагидропиридин, далее обозначенный под кодовым номером 5 К 57746, и его фармацевтически приемлемые соли впервые были описаны в ЕР 0 101 381 как анорексигенные агенты и впоследствии как антианксиодепрессанть 1 (115 5 026 716), антиконстипационные агенты (115 5 109 005), нейротропнь 1 е агенты (115 5 270 320), ингибиторы свободных радикалов (115 5 292 745) и кардиопротекторь 1 (115 5 378 709).В ЕР 0 101 381 описан 5 К 57746 в виде гидрохлорида, далее обозначенного как 5 К 57746 А, и эту соль использовали в преклинических и клинических испытаниях на здоровых добровольцах. Согласно указанному документу, 5 К 57746 А выделяли кристаллизацией из этанола, особенно из абсолютного этанола.В преклинических испытаниях, особенно в фармакологических и токсикологических тестах на животных, ЭК 57746 А продемонстрировал стабильную активность и поведение. Таким же образом, фармакокинетические исследования на животных дали стабильные и воспроизводимые результаты.Для сопоставления, в клинических исследованиях, проводимых на здоровых добровольцах (фаза 1), обнаружено, что ЭК 57746 А демонстрировал высокую изменчивость концентрации в плазме и фармакодинамического действия активного ингредиента.В первых клинических испытаниях, проводимых на пациентах, страдающих очень серьезными заболеваниями, особенно боковым амиотрофическим склерозом, дозу ЭК 57746 А поддерживали на очень низком уровне, а именно 2 мг/день, в этой дозе данный продукт оказался перспективным 077.6. ВгаЩеу, доклад, озаглавленный Ыеш бгиз Тог ашуоггоршс 1 агега 1 5 с 1 его 515, материалы встречи Американской академии неврологии, 23-30, марта,1996. - С. 240-23/240-28).Более того, было обнаружено, что при получении больших количеств ЭК 57746 А по методике выделения, описанной в ЕР О 101 381, невозможно достичь хорошего выхода продукта с постоянными характеристиками, которые делают возможным преодоление недостатков, отмеченных в фазе 1 клинических исследований.Более конкретно, было обнаружено, что по методике выделения, описанной в ЕР О 101 381,получают ЭК 57746 А, состоящий из кристаллов, размер которых не постоянен и определенно больше, чем 150 микрометров более конкретно по крайней мере около 75 кристаллов имеют размер 150-600 микрометров.Более того, обнаружено, что ЭК 57746 А, полученный по методике, описанной в ЕР О 101 381, состоит, как показывает дифференциальная сканирующая калориметрия, из, по крайней мере, 3 различных форм.В конце концов было обнаружено, что соответствующие соотношения различных форм не постоянны для различных партий ЭК 57746 А, что затрудняет контроль характеристик исходного материала для получения фармацевтических композиций.В настоящее время обнаружено, что при проведении кристаллизации ЭК 57746 А при подходящих и постоянных условиях, которые подразумевают растворитель, скорость смешивания и скорость охлаждения, имеется возможность выделения соединения в трех различных кристаллических формах или в виде смеси двух из этих трех форм с неизменными и воспроизводимыми соотношениями.форму 1 ЭК 57746 А получают охлаждением раствора ЭК 57746 А в смеси этанол/концентрированная хлористоводородная кислота без перемешиванияформу П ЭК 57746 А получают охлаждением раствора ЭК 57746 А в абсолютном этаноле или в смеси этилацетат/вода при контролируемой скорости охлаждения и скорости перемешиванияформу П 1 ЭК 57746 А получают охлаждением раствора ЭК 57746 А в диметилсульфоксиде исмесь формы 1 и формы П 1, имеющую фиксированный и воспроизводимый состав, получают охлаждением раствора ЭК 57746 А в смеси этанол/вода.Также было обнаружено, что эти новые кристаллические формы как в чистом виде, так и в смесях с фиксированным соотношением двух из указанных форм, абсорбируются одинаково и воспроизводимо и облегчают определение оптимальной дозы активного ингредиента. Даже больше, чем улучшение фармакокинетических и фармакодинамических свойств, возможность контролировать производство композиции ЭК 57746 А в кристаллической форме является крайне выгодной с точки зрения маркетинга.Окончательно было обнаружено, что если новые кристаллические формы или смеси двух указанных форм содержат очень мелкие кристаллы, особенно микронизированные кристаллы, активность активного ингредиента значительно повышается и его абсорбциястановится одинаковой И постоянной, что дает возможность вводить небольшие дозы при очень хорошем терапевтическим ответе реакции, и, в то же время, полного контроля потенциальных побочных эффектов.На рисунках показаны термограммы, полученные при дифференциальной сканирующей калориметрии формы 1, формы П, формы 1 П и смеси форма 1/форма П 1 в соотношении 65,7/34,3.На фиг. 1 показана термограмма формы 1 ЗК 57746 А, полученной по методике примера 1, указанная термограмма получена при помощи дифференциальной сканирующей калориметрии при температуре от 50 С до 180 С. На данной термограмме значение температуры перехода твердое-твердое составляет 148-149 С.На фиг. 2 показана термограмма формы П ЗК 57746 А, полученной по методике примера 2, указанная термограмма получена при помощи дифференциальной сканирующей калориметрии при температуре от 50 С до 180 С. На данной термограмме значение температуры перехода твердое-твердое составляет 153-155 С.На фиг. 3 показана термограмма формы П 1 ЗК 57746 А, полученной по методике примера 3, указанная термограмма получена при помощи дифференциальной сканирующей калориметрии при температуре от 50 С до 180 С. На данной термограмме значение температуры перехода твердое-твердое составляет 141-142 С.На фиг. 4 показана термограмма смеси форма 1/форма 1 П, полученной по методике примера 4, указанная термограмма получена при помощи дифференциальной сканирующей калориметрии при температуре от 50 С до 180 С. На данной термограмме показаны значения температур перехода твердое-твердое двух форм.Таким образом, согласно одному из аспектов, данное изобретение относится к способу кристаллизации гидрохлорида 1-2-(2-нафтил)этил-4-(3-трифторметилфенил)-1,2,3,6-тетрагидропиридина, отличающемуся тем, что(а) указанное соединение растворяют нагреванием в растворителе, выбранном из алканолов, имеющих от 1 до 3 атомов углерода, кетонов, имеющих от 3 до 6 атомов углерода, диметилсульфоксида и этилацетата, где указанный растворитель необязательно содержит от 5 до 30 об. воды или водной соляной кислоты(Ь) полученный раствор охлаждают до температуры -10/ 10 С со скоростью от 3 до 100 С/ч, при перемешивании от 0 до 600 об/мин и(с) полученный продукт выделяют и необязательно микронизируют.Процесс по данному изобретению проводят по обычной методике кристаллизации,однако тип растворителя, скорость охлаждения, присутствие или отсутствие воды и скорость перемешивания являются существенными параметрами для воспроизводимого получения той или иной кристаллической формы или для воспроизводимого получения смеси двух форм с неизменными пропорциями.На стадии (а) гидрохлорид 1-2-(2-нафтил)этил-4-(3-трифторметилфенил)-1,2,3,6-тетрагидропиридина например неочищенный продукт, полученный способом, описанным в ЕР 0 101 381, нагревают, предпочтительно с обратным холодильником, в выбранном растворителе необязательно в присутствии воды.Вода может использоваться для полного растворения ЗК 57746 А. Хотя в метаноле и этаноле, например, продукт растворяется полностью до приемлемой концентрации (например, 15-150 г/л), в ацетоне, метилэтилкетоне, изопропаноле или этилацетате при тех же концентрациях продукт полностью не растворяется. В эти растворители достаточно добавить от 5 до 30 воды для практически полного растворения при температуре кипения с обратным холодильником. Однако процент содержания воды не должен быть слишком высоким для избежания избыточной растворимости и потери конечного продукта.По одной из подходящих методик используют растворитель, выбранный из следующих смесей (об/об) от 100/О до 70/30 метанол/вода, от 100/О до 70/30 этанол/вода, от 95/5
МПК / Метки
МПК: A61K 31/44, C07D 211/70
Метки: полученные, формы, кристаллизации, кристаллические, производного, тетрагидропиридина, способ
Код ссылки
<a href="https://by.patents.su/14-6916-sposob-kristallizacii-proizvodnogo-tetragidropiridina-i-poluchennye-kristallicheskie-formy.html" rel="bookmark" title="База патентов Беларуси">Способ кристаллизации производного тетрагидропиридина и полученные кристаллические формы</a>
Предыдущий патент: Способ изготовления межкомпонентной изоляции интегральных микросхем
Следующий патент: Способ выявления постоянных носителей Helicobacter pylori
Случайный патент: Устройство обмена конфиденциальной информацией на основе нейросетевых технологий