Пептид и способ его получения
Номер патента: 7820
Опубликовано: 28.02.2006
Авторы: КОРОТКОВ Андрей Марксович, ДЕЙГИН Владислав Исакович
Текст
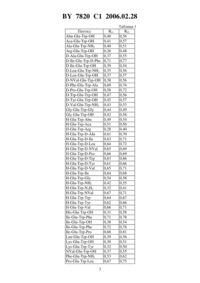
(51)07 5/06, 5/08, 5/10 НАЦИОНАЛЬНЫЙ ЦЕНТР ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ(71) Заявитель ИММУНОТЕХ ДЕВЕЛОПМЕНТС ИНК.(72) Авторы ДЕЙГИН Владислав Исакович КОРОТКОВ Андрей Марксович(73) Патентообладатель ИММУНОТЕХ ДЕВЕЛОПМЕНТС ИНК.,гдеобозначает , остаток , , , , , , , , , , -, -,-, -, -, -, -, -, -, , , , -аминомасляной кислоты или -аминокапроновой кислоты, обозначает остаток , , , , , , , , , , -, -, , -, -, -, -, -, -, , -аминомасляной кислоты или аминокапроновой кислоты, , 2, 23 или моно- или дизамещенный С 1-С 3 алкиламид, при условии, что еслиобозначает ,не обозначает ОН, или его фармацевтически приемлемая соль. 2. Пептид по п. 1, отличающийся тем, что представлен последовательностью , , 2, , , , , , 23, или , или его фармацевтически приемлемая соль. 3. Пептид по п. 2, отличающийся тем, что представлен последовательностью , или его фармацевтически приемлемая соль. 4. Способ получения пептида формулы ,гдеобозначает , остаток , , , , , , , , , , -, -,-, -, -, -, -, -, -, , , , -аминомасляной кислоты или -аминокапроновой кислоты, обозначает остаток , , , , , , , , , , -, -,-, -, -, -, -, -, -, , -аминомасляной кислоты или аминокапроновой кислоты, , 2, 23 или моно- или дизамещенный С 1-С 3 алкиламид, заключающийся в том, что алкиловый эфир аминокислоты вводят во взаимодействие в растворе с третбутилоксикарбониламинокислотой, затем последовательно наращивают пептидную цепь методом активированных эфиров и методом смешанных ан 7820 1 2006.02.28 гидридов, последовательно присоединяя третбутилоксикарбониламинокислоты с предварительным отщеплением на каждой стадии третбутилоксикарбонильной группы путем обработки реакционной смеси муравьиной кислотой, и последующей очисткой промежуточных продуктов кристаллизацией получают продукт формулы , который очищают обращенно-фазовой хроматографией. Изобретение относится к медицине, а именно к способам получения биологически активных веществ, обладающих иммунорегулирующими свойствами, и может найти применение в медицине, ветеринарии, а также в экспериментальной биохимии. Предшествующий уровень техники В практической медицине широко известны в качестве регуляторов иммунных процессов тимусные экстракты, в частности тимозин фракция 5 /,.,, Н.А.,./, тиналин/СН, 659586/. Эти экстракты состоят из комплекса веществ полипептидной природы, и получение их из природных источников ограничено сложностью производства, малым выходом активных веществ и значительной вариабельностью их физико-химических характеристик и биологических свойств. Кроме того, из-за присутствия в природных препаратах тимуса балластных компонентов при их использовании у больных иногда возникают побочные явления. Последнее обстоятельство явилось стимулом для создания синтетических пептидов. В настоящее время осуществлен синтез ряда пептидов, обладающих иммунорегуляторными свойствами РСТ 089/06134, ЕР 230052,5008246,5013723. Каждый из полученных синтетических пептидов с ограниченным комплексом необходимых свойств обладает высокой активностью, низкой токсичностью, отсутствием побочных эффектов, которые определяют их возможное применение в медицине. Раскрытие изобретения В основу изобретения положена задача создания нового синтетического биологически активного пептида, обладающего иммунорегулирующим свойством, формулы,где- Н или , , , , , , , Ту, , , -, -,-, -, -, -, -, -, -,-аминомасляная кислота,-аминокапроновая кислота- , , , , , , , , , , -, -, -,-, -, -, -, -, -, -аминомасляная кислота, аминокапроновая кислота, ОН, моно- или дизамещенный амид (Сз-Сз). Целью изобретения было также создание принципиально нового технологического процесса получения вещества пептидной природы, который позволил бы при минимальном количестве и простоте стадий получать с высоким выходом продукт вышеприведенной формулы. Сущность нового способа состоит в синтезе пептида в растворе путем последовательного наращивания цепи с С-конца молекул, используя стратегию максимального блокирования функциональных групп, исходя из алкилового эфира аминокислоты с помощью метода активированных эфиров и метода смешанных ангидридов, используя третбутилоксикарбониламинокислоты. Для ряда соединений нового пептида в табл. 1 приведены значенияв системе (хлороформ - метанол - 32 уксусная кислота 604520) и 2 в системе (бутанол - пиридин - вода - уксусная кислота 5541). Т-Ту 0,59 0,61 Пептид заявленной формулы, полученный в результате описанного способа, представляет собой белый порошок, который растворим в воде, мало растворим в спирте и практически нерастворим в хлороформе. Лучшие варианты осуществления изобретения. Изобретение иллюстрируется следующим примером. Пример. В этом примере описан способ получения пептида формулы ОН. 1. Получение . Смесь 46,0 г (0,2 моля) Вос-е-ОН и 40,5 г (0,22 моля) пентафторфенола в 100 мл этилацетата охлаждали до - 5 С и добавляли 45,3 г (0,22 моля) ,-дициклогексилкарбодиимида. Реакционную смесь перемешивали 3 часа при комнатной температуре, дициклогексилмочевину отфильтровывали, растворители упаривали в вакууме, остаток кристаллизовали в смеси этилацетат-гексан. Выпавший осадок отфильтровывали. Выход 71,3 г (90 ). 2. Получение . 19,8 г (0,05 моль) растворяли в 100 мл диметилформамида и при перемешивании добавляли раствор 20 г (0,06 моль) - и 5,0 г (0,06 моль) 3 в воде. Раствор перемешивали в течение 20 часов при комнатной температуре, затем упаривали растворители в вакууме. К остатку добавляли 200 мл этилацетата и 200 мл 2 раствора серной кислоты, перемешивали. Органический слой промывали раствором серной кислоты (2100 мл), насыщенным растворомдо рН 7, сушили над безводным сульфатом натрия, растворитель отгоняли в вакууме. Остаток кристаллизовали в системе этилацетатгексан, осадок отфильтровывали и сушили в вакууме. Выход 20,5 г (75 ). 3. Получение . 20,5 г растворяли в 150 мл муравьиной кислоты, перемешивали 3,5 часа при 45 и растворитель упаривали в вакууме. К остатку добавляли 200 мл воды и упаривали в вакууме еще раз. Остаток заливали смесью 300 мл изопропанола, 200 мл эфира и выдерживали 10 часов. Осадок фильтровали и сушили в вакууме. Выход 15,3 г(75 ). Очистку пептида проводили с помощью обращенно-фазной хроматографии в системе ацетоннтрил - 0,1 раствор трифторуксусной кислоты. Выход 13 г (85 ). В результате изучения физико-химических свойств пептида были получены следующие его характеристики Первичная структура - Брутто формула - 24-30-4-4 Молекулярный вес - 446,5 Внешний вид - белый с желтоватым оттенком или серый порошок Растворимость - растворим в воде, практически нерастворим в хлороформе У.Ф.-спектр в области 250-300 мм имеет максимум 2802 мм, плечо 2872 мм. Биологическая активность нового пептида изучалась на морских свинках с помощью общепринятого теста Е-розеткообразования. В табл. 2 приведены сравнительные данные воздействия препаратов тимуса и заявленного пептида на процесс Е-розеткообразования лимфоцитов морских свинок после обработки их трипсином. 4 7820 1 2006.02.28 Таблица 2 Количество Е-РОК ( ) Фон, ин- После обПосле обработки трипсином и препаратом в Препарат тактные работки концентрации мг/мл животные трипсином 10 10-7 10-8 10-9 10-10 10-и 10-12 тималин 66,5 36,1 57,0 40,1 37,0 35,3 37,4 36,5 34,7 тимозин фракция 5 66,5 36,1 60,3 35,4 33,4 39,5 39,1 33,7 35,8-66,5 36,1 61,4 63,9 64,8 60,2 37,5 40,0 34,3 Каждая концентрация исследовалась на пяти животных. Достоверным считается увеличение Е-РОК по сравнению с контролем на 50 , т.е. до 55 и выше. Установлено, чтозаявляемый пептид активнее известных препаратов в 103 раза. С целью изучения безопасности пептида проводили изучение его острой токсичности. Изучение острой токсичности проводили в соответствии с Методическими рекомендациями Фармакологического комитета РФ Требования к доклиническому изучению общетоксичного действия новых фармакологических веществ, М., 1985 г. Результаты исследований показали, что при внутрибрюшинном введении 1000-кратной дозы пептид не оказывал острого токсичного действия и при этих дозах оказалось невозможным достигнуть их 50. Промышленная применимость. Пептид, обладающий биологической активностью, может найти широкое применение в медицине и ветеринарии. Национальный центр интеллектуальной собственности. 220034, г. Минск, ул. Козлова, 20. 5
МПК / Метки
МПК: C07K 5/10, C07K 5/08, C07K 5/06
Метки: получения, пептид, способ
Код ссылки
<a href="https://by.patents.su/5-7820-peptid-i-sposob-ego-polucheniya.html" rel="bookmark" title="База патентов Беларуси">Пептид и способ его получения</a>
Предыдущий патент: Мелкозернистое железо, содержащее фосфор и способ его получения
Следующий патент: Пептид, способный модулировать пролиферацию клеток
Случайный патент: Установка для валковой штамповки с неприводными роликами