Способ выделения полимиксина
Номер патента: 4775
Опубликовано: 30.12.2002
Авторы: Солдатов Владимир Сергеевич, Водопьянова Людмила Александровна, Царенков Валерий Минович, Куваева Зоя Ивановна, Петров Петр Тимофеевич, Скрипко Галина Дмитриевна, Букатина Татьяна Валентиновна
Текст
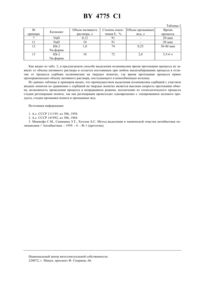
(73) Патентообладатель Институт физикоорганической химии НАН Беларуси(57) Способ выделения полимиксина, включающий сорбцию полимиксина из нативного раствора на катионите с последующим элюированием водным раствором щелочи, отличающийся тем, что в качестве катионита используют жидкий катионит, представляющий собой полинонилнафталинсульфокислоту или ее солевую форму в несмешивающемся с водой органическом неполярном растворителе или в смеси, содержащей несмешивающийся с водой органический неполярный растворитель и до 20 объемныхвысшего спирта (С 6 С 9), и сорбцию ведут при рН 1,5-5.(56) Мамиофе С.М. и др. Метод выделения и химической очистки антибиотика полимиксина // Антибиотики. Изобретение относится к микробиологической и медицинской промышленности и касается способа выделения полимиксина-антибиотика полипептида. Известны способы получения полимиксина 1, 2. В основе этих способов лежат следующие принципиальные стадии биосинтез, коагуляция и фильтрация культуральной жидкости, выделение антибиотика из нативного раствора, деминерализация раствора антибиотика, стерилизация, концентрирование и сушка. Выделение антибиотика из нативного раствора традиционно ведется путем ионообменной сорбции на ионообменных смолах. Так, в способе, описанном в 1, нативный раствор,полученный после обработки щавелевой кислотой и фильтрации культуральной жидкости . , пропускают через колонку, наполненную катионитом КБ 4-П 2 в натриевой форме, со скоростью 1 л/ч/г, затем ионит промывают последовательно дистиллированной водой и метанолом, после чего проводят вытеснение антибиотика 0,35 н раствором соляной кислоты в метаноле со скоростью 10 мл/ч/г. Полученный раствор солянокислого полимиксина в метаноле нейтрализуют на анионите ЭДЭ-10 в ОН-форме. Недостатками процесса выделения антибиотика с помощью твердых ионитов являются длительность процесса, 17-18 ч для 96 л нативного раствора, наличие большого количества промывных вод, низкий выход целевого продукта (4050 ). Наиболее близким по технической сущности и достигаемому эффекту к предлагаемому способу является способ выделения полимиксина из нативного раствора на катионообменных смолах 3. Согласно способу прототипу, нативный раствор, содержащий полимиксин, пропускают через колонку, наполненную катионитом с карбоксильными группами КБ-2 или КБ-1. Элюирование антибиотика с катионита ведется водными или метанольными растворами кислот или водными растворами аммиака. Использование карбоксильных катионитов позволяет повысить выход целевого продукта на стадии выделения из нативного раствора до 75 ,однако неизбежными остаются недостатки самого процесса сорбции на твердых ионитах многостадийность процесса, включение помимо стадии сорбции и десорбции полимиксина стадии промывки и регенерации ионита, длительность процесса, 5-6 ч для 10 л нативного раствора, присутствие промывных вод в процессе выделения, что не допустимо в современной экологической ситуации. Задачей изобретения является упрощение способа выделения полимиксина из нативного раствора и исключение промывных вод. Поставленная задача достигается тем, что в способе выделения полимиксина, включающем сорбцию полимиксина из нативного раствора на катионите с последующим элюированием водным раствором щелочи, в 4775 1 качестве катионита используют жидкий катионит, представляющий собой полинонилнафталинсульфокислоту или ее солевую форму в несмешивающемся с водой неполярном органическом растворителе или смеси,содержащей помимо неполярного, несмешивающегося с водой органического растворителя до 20 об.высшего спирта (С 6-С 9). Преимущества предлагаемого способа следующие. Скорость протекания ионного обмена в предлагаемом способе на порядок выше, чем при использовании традиционного метода сорбции на твердых ионитах и не зависит от объемов вступающих в реакцию веществ. На стадии элюирования одновременно с концентрированием полимиксина происходит и регенерация жидкого ионита, что позволяет снова использовать его для сорбции полимиксина, минуя стадии промывки и регенерации, то есть вести процесс в непрерывном замкнутом режиме и при отсутствии промывных вод. Это является существенным преимуществом использования жидких ионитов по сравнению с твердыми, для которых необходимы стадии дополнительной обработки. Предлагаемый способ иллюстрируется следующими примерами. Пример 1. В делительную воронку емкостью 500 мл, снабженную пропеллерной мешалкой, помещают 120 мл нативного раствора отфильтрованной культуральной жидкости полимиксина, полученной при использовании на стадии биосинтеза штамма продуцента Вас. , с содержанием полимиксина С 1,0 г/л, добавляют 30 мл 0,22 М раствора калиевой соли полинонилнафталинсульфокислотыв гептане. Таким образом,мольное отношение веществ, участвующих в реакциик-во молей полимиксина / к-во молей 0,015. Сорбцию ведут при рН 2 и перемешивании 5-10 мин. После разделения фаз органическую фазу обрабатывают раствором 0,2 н КОН в течение 5-10 минут при перемешивании. Объемное отношение веществ участвующих в реакции /2. Содержание полимиксина в элюате Сэ 6,1 г/л. Степень извлечения полимиксина относительно его исходного количества в нативном растворе Е 76 . Концентрация полимиксина в элюате 6,1 г/л соответствует активности полимиксина 61000 ед/мл. Активность полимиксина в нативном растворе и в элюате определялась микробиологическим методом. Параллельно содержание полимиксина в нативном растворе и в элюате определялось методом количественной сорбции полимиксина ионообменником КБ-2 с последующим количественным элюированием полимиксина 0,2 н . В от примесей таким образом нативном растворе и в элюате содержание полимиксина определялось фотоколориметрическим методом. Полученные данные совпадают с данными микробиологического анализа, то есть в процессе выделения полимиксина по предлагаемому способу не происходит инактивация антибиотика, а определение содержания полимиксина в элюате можно проводить наиболее удобным методом. Далее процесс получения препарата полимиксина можно вести по известной схеме, так же как и в случае использования твердых ионитов 1. Пример 2. В делительную воронку емкостью 55 мл, снабженную пропеллерной мешалкой, помещают 120 мл нативного раствора, полученного аналогично примеру 1, с концентрацией полимиксина 1,2 г/л, туда же вносят 30 мл 0,22 М раствора полинонилнафталинсульфокислотыв гексане. Мольное отношение веществ, участвующих в процессе сорбции,0,018. Сорбцию ведут при рН 4,2 и перемешивании в течение 5-10 мин. После разделения фаз и отделения водной фазы к органической фазе добавляют раствор 0,2 ни перемешивают 5-10 мин. Объемное отношение /2. Концентрация полимиксина в элюате определялась фотоколориметрическим методом, Сэ 7,4 г/л. Степень извлечения полимиксина относительно его исходного количества в нативном растворе Е 77 . Пример 3. В делительную воронку, снабженную пропеллерной мешалкой, помещают 120 мл нативного раствора,полученного аналогично примеру 1, с концентрацией полимиксина 1,2 г/л, туда же вносят 30 мл 0,22 М раствора натриевой соли полинонилнафталинсульфокислоты . Мольное отношение веществ, участвующих в реакции,0,018. Сорбцию ведут при рН 4,65 и перемешивании в течение 5-10 мин. После разделения фаз и отделения водной фазы к органической фазе добавляют раствор 0,2 ни перемешивают 5-10 мин. Объемное отношение при элюировании /2. Концентрация полимиксина в элюате определялась фотоколориметрическим методом, Сэ 7,5 г/л. Степень извлечения полимиксина Е 78 . Пример 4. 100 мл нативного раствора, полученного аналогично примеру 1, с концентрацией полимиксина 1,3 г/л помещают в делительную воронку с пропеллерной мешалкой. Туда же добавляют 40 мл 0,077 М раствора аммонийной соли полинонилнафталинсульфокислоты (4) в гептане, содержащем 10 изооктилового спирта. Мольное отношение 0,036. Сорбцию проводят при рН 5 и перемешивании в течение 5-10 мин. После разделения фаз и отделения водной фазы к органической фазе добавляют водный раствор аммиака,С 410 . Объемное отношение 4/42. Элюирование проводят при перемешивании в течение 5-10 мин. Концентрация полимиксина в элюате определялась фотоколориметрическим методом, Сэ 5,1 г/л. Степень извлечения полимиксина Е 78 . 4775 1 Пример 5. 120 мл раствора полимиксина с концентрацией 2,1 г/л помещают в делительную воронку с пропеллерной мешалкой. Для моделирования нативного раствора водный раствор полимиксина содержит 1. Туда же добавляют 35 мл 0,16 М раствора калиевой соли полинонилнафталинсульфокислотыв гептане, содержащем 16 гексилового спирта. Мольное отношение 0,03. Сорбцию проводят при рН 1,5 и перемешивании в течение 5-10 мин. Отделяют органическую фазу, добавляют к ней 0,2 н раствор КОН и перемешивают 5-10 мин. Объемное отношение при элюировании /2,9. Концентрация полимиксина в элюате определялась фотоколориметрическим методом, Сэ 16,1 г/л. Степень извлечения Е 78 . Пример 6. 120 мл модельного раствора полимиксина с концентрацией 1,16 г/л на фоне 1 растворапомещают в делительную воронку. Туда же добавляют в качестве жидкого ионита 24 мл 0,15 М раствора полинонилнафталинсульфокислотыв октане, содержащем 20 нонилового спирта. Мольное отношение 0,034. С помощью НС доводят рН до 4,5. Сорбцию полимиксина проводят при перемешивании в течение 5-10 мин. Отделяют органическую фазу, добавляют к ней 0,2 н раствори перемешивают в течение 5-10 мин. Объемное отношение при элюировании /2. Концентрация полимиксина в элюате определялась фотоколориметрическим методом, Сэ 10 г/л, степень извлечения полимиксина Е 86 . Пример 7. 120 мл нативного раствора полимиксина, полученного аналогично примеру 1, с концентрацией 1,92 г/л помещают в делительную воронку. Туда же добавляют 24 мл 0,13 М раствора натриевой соли полинонилнафталинсульфокислотыв гексане, содержащем 19 нонилового спирта. Мольное отношение 0,06. Сорбцию ведут при рН 3,8 и перемешивании в течение 5-10 мин. Отделяют органическую фазу,добавляют 0,2 н раствори перемешивают в течение 5-10 мин. Объемное отношение веществ при элюировании /2. Содержание полимиксина в элюате определялось фотоколориметрическим методом, Сэ 17,5 г/л. Степень извлечения Е 91 . Пример 8. 120 мл нативного раствора полимиксина, полученного аналогично примеру 1, с концентрацией 1,92 г/л помещают в делительную воронку. Туда же добавляют 24 мл 0,13 М раствора натриевой соли полинонилнафталинсульфокислотыв гексане, содержащем 19 нонилового спирта. Сорбцию проводят при рН 1 и перемешивании в течение 5-10 мин. После разделения фаз и отделения водной фазы к органической фазе добавляют 0,2 н растворпри объемном отношении /2. Содержание полимиксина в элюате определялось фотоколориметрическим методом, Сэ 16,8 г/л, степень извлечения полимиксина Е 87 . Хотя при данных условиях достигается высокая степень извлечения, но вместе с полимиксином из нативного раствора просорбировались сопутствующие примеси. Элюат имеет желтованый цвет и требует дополнительной очистки. Пример 9. 100 мл нативного раствора полимиксина, полученного аналогично примеру 1, с концентрацией 0,55 г/л помещают в делительную воронку. Туда же добавляют 20 мл 0,12 М раствора натриевой соли полинонилнафталинсульфокислотыв гексане, содержащем 22 нонилового спирта. Мольное отношение 0,098. Сорбцию проводят при перемешивании и рН 6 в течение 5-10 мин. После разделения фаз и отделения водной фазы к органической фазе добавляют 0,2 н раствори перемешивают 5-10 мин. Объемное отношение /2. Содержание полимиксина в элюате определялось фотоколориметрическим методом, Сэ 3,8 г/л, степень извлечения Е 70 . При значении рН сорбции больше 5 падает степень извлечения и уменьшается содержание полимиксина в элюате. Пример 10. 120 мл модельного раствора полимиксина с концентрацией 0,84 г/л на фоне 1 растворапомещают в делительную воронку. Туда же добавляют в качестве жидкого ионита 30 мл 0,15 М раствора калиевой соли полинонилнафталинсульфокислотыв гексане, содержащем 22 нонилового спирта. Мольное отношение 0,02. Сорбцию полимиксина проводят при рН 2 и перемешивании 5-10 мин. Отделяют органическую фазу, добавляют к ней 0,2 н раствор КОН и перемешивают 5-10 мин. Объемное отношение при элюировании /2. Концентрация полимиксина в элюате определялась фотоколориметрическим методом, Сэ 4,9 г/л. Степень извлечения полимиксина Е 73 . Снижение степени извлечения и содержания полимиксина в элюате связано с увеличением содержания спирта в растворителе до 22 . Данные примеров 1-10 приведены в табл. 1. 4775 1 Таблица 1 КонцентСодержание рация рН Степень полимиксиспирта в сорбЭлюент извлечена в элюате раствоции ния Е,Сэ, г/л рителе,об.6 7 8 9 10 0 2 КОН 0,2 н 76 6,1 0 4,20,2 н 77 7,4 0 4,650,2 н 78 7,5 изоокта 5,0 4 1078 5,1 нол 105 2,1 0,84 гексан нонанол 2,0 КОН 0,2 н 73 4,9 22 Выбор интервала рН в предлагаемом способе объясняется тем, что при значениях рН 1,5 из нативного раствора одновременно с целевым продуктом могут выделяться и сопутствующие вещества, например пигменты, а при значениях рН 5 процесс протекает менее эффективно и наблюдается снижение степени извлечения полимиксина (70 ). Кроме того, известно, что в сильнокислой и сильнощелочной среде полимиксин может инактивироваться (4).Фактором, снижающим эффективность выделения полимиксина из нативного раствора, является и увеличение содержания высшего спирта в растворителе выше предлагаемого(20 ). Пример 11. В экстрактор емкостью 20 л, снабженный мешалкой, помещают 10 л нативного раствора, полученного аналогично примеру 1, с содержанием полимиксина 1,92 г/л, добавляют 2 л 0,13 М раствора натриевой соли полинонилнафталинсульфокислоты в гексане, содержащем 19 нонилового спирта. Мольное отношение 0,06. Сорбция и элюирование проводятся аналогично примеру 7. Сорбция длится 5-10 мин при рН 3,8. После отделения водной фазы к органи-ческой фазе в экстрактор добавляют 1 л 0,2 ни перемешивают 5-10 минут. Активность полимиксина в элюате определяли микробиологическим путем, она составляет 175000 ед/мл, что соответствует концентрации полимиксина Сэ 17,5 г/л. Степень извлечения полимиксина Е 91 . На основании данных способа прототипа 3 и аналога 1 был воспроизведен опыт по извлечению полимиксина из нативного раствора с помощью твердых ионитов для разных объемов нативного раствора. Пример 12. 1000 мл нативного раствора, полученного аналогично примеру 1, с содержанием полимиксина 1,1 г/л пропускают через колонку, заполненную 7 г катионита КБ-2 в натриевой форме, со скоростью 1 л/ч/г. Емкость катионита 18105 /г. Время сорбции 9-10 мин. После сорбции ионит промывают 250 мл дистиллированной воды. Элюирование антибиотика проводят 1,5 н раствором аммиака. 30 мл 4 пропускают со скоростью 10 мл/час/г в течение 25 мин. Время процесса 30-40 мин. Объем промывных вод 250 мл. Активность полимиксина в элюате определяли микробиологическим методом, она составила 270000 ед/мл, что соответствует концентрации Сэ 27 г/л. Степень извлечения Е 74 . Пример 13. 10 л нативного раствора, полученного аналогично примеру 1, с содержанием полимиксина 1,1 г/л пропускают через колонку заполненную, катионитом КБ-2 в натриевой форме. Все условия сорбции и элюирования полимиксина такие же как, и в примере 11. Время процесса 5,5-6 ч, не считая времени, необходимого для регенерации ионита. Объем промывных вод 2 л. Концентрация полимиксина в элюате Сэ 26,4 г/л. Степень извлечения Е 72 . Сравнительные данные примеров 7, 11-13 приведены в табл. 2. КонКонцентцентрация поли миксина в Жидкий рация Раствоприисходном катионит катио- ритель мера нита, С,растворе С,М г/л 1 2 3 4 5 1 1,0 Степень извле- Объем промывных чения Е,вод, л 91 91 74 0,25 Как видно из табл. 2, в предлагаемом способе выделения полимиксина время протекания процесса не зависит от объема нативного раствора и остается постоянным при любом масштабировании процесса в отличие от процесса сорбции полимиксина на твердых ионитах, где время протекания процесса прямо пропорционально объему нативного раствора, поступающего в ионообменную колонну. Из данных таблицы и примеров видно, что преимуществом выделения полимиксина сорбцией с участием жидких ионитов по сравнению с сорбцией на твердых ионитах является высокая скорость протекания обмена, возможность проведения процесса в непрерывном режиме, исключение из технологического процесса стадии регенерации ионита, так как регенерация происходит одновременно с элюированием целевого продукта, стадии промывки ионита и промывных вод. Источники информации 1. А.с. СССР 111195, кл 30, 1958. 2. А.с. СССР 141992, кл 30, 1964. 3. Мамиофе С.М., Синицина З.Т., Хохлов А.С. Метод выделения и химической очистки антибиотика полимиксина // Антибиотики. - 1959. - 4. -1 (прототип). Национальный центр интеллектуальной собственности. 220072, г. Минск, проспект Ф. Скорины, 66. 5
МПК / Метки
МПК: C07K 7/62, A61K 31/70
Метки: выделения, полимиксина, способ
Код ссылки
<a href="https://by.patents.su/5-4775-sposob-vydeleniya-polimiksina.html" rel="bookmark" title="База патентов Беларуси">Способ выделения полимиксина</a>
Предыдущий патент: Способ дезактивации почво-грунтов
Следующий патент: Устройство автоматическое открывания и закрывания створок ворот
Случайный патент: Средство для фотодинамической терапии гнойных ран