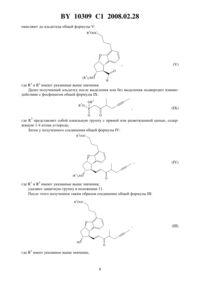
Способ получения берапроста и его солей
Номер патента: 10309
Опубликовано: 28.02.2008
Авторы: БАЛОГНЕ КАРДОС, Сусанна, ДАЛМАДИ, Дьюла, БОДИ, Йожеф, СЕВЕРЕНИ, Зольтан, САБО, Тибор
Текст
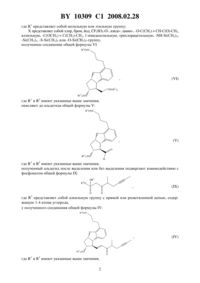
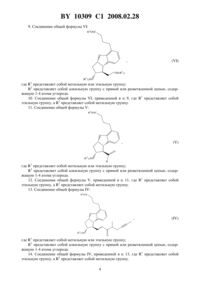
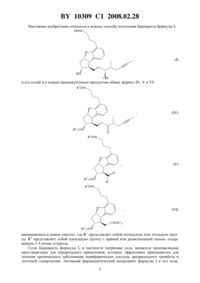
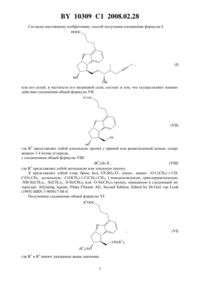
НАЦИОНАЛЬНЫЙ ЦЕНТР ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ СПОСОБ ПОЛУЧЕНИЯ БЕРАПРОСТА И ЕГО СОЛЕЙ(71) Заявитель ХИНОИН Дьдьсер эш Ведьесети Термекек Дьяра Рт.(73) Патентообладатель ХИНОИН Дьдьсер эш Ведьесети Термекек Дьяра Рт.(57) 1. Способ получения соединения формулы или его солей, в частности, его натриевой соли, отличающийся тем, что осуществляют взаимодействие соединения общей формулы 2 гдепредставляет собой алкильную группу с прямой или разветвленной цепью, содержащую 1-4 атома углерода,с соединением общей формулы 10309 1 2008.02.28 где 1 представляет собой метильную или этильную группупредставляет собой хлор, бром, йод, 32, азидо-, циано-, С(СН 3)СН-С-СН 3,аллильную, -С(ОСН 3)С(СН 3)-СН 3, 1-имидазолильную, трихлорацетильную, (СН 3)3,-(СН 3)3, (СН 3)3 или (3)3-группу,полученное соединение общей формулы 2 где 1 и 2 имеют указанные выше значения,окисляют до альдегида общей формулы 2 где 1 и 2 имеют указанные выше значения,полученный альдегид после выделения или без выделения подвергают взаимодействию с фосфонатом общей формулы 33 гдепредставляет собой алкильную группу с прямой или разветвленной цепью, содержащую 1-4 атома углерода,у полученного соединения общей формулы 2 гдеиимеют указанные выше значения,2 10309 1 2008.02.28 удаляют защитную группу в положении 11,полученное соединение общей формулы 2 где 2 имеет указанное выше значение,восстанавливают с получением соединения общей формулы 2 где 2 имеет указанное выше значение,которое затем подвергают гидролизу и выделяют кислоту формулы , которую, при необходимости, путем взаимодействия с основанием переводят в соль и затем соль выделяют,или полученную кислоту формулыпри необходимости без предварительного выделения переводят в соль и выделяют полученную таким образом соль. 2. Способ по п. 1, отличающийся тем, что используют соединение общей формулы, где 1 представляет собой этил, а Х - хлор, бром, йод, 32, азидо-, циано-,С(СН 3)СН-С-СН 3, аллильную, -С(ОСН 3)С(СН 3)-СН 3, 1-имидазолильную, трихлорацетильную, (СН 3)3, -(СН 3)3, (СН 3)3 или (3)3-группу. 3. Способ по п. 1, отличающийся тем, что соединение общей формулыокисляют до соединения общей формулысмесью диметилсульфоксида, оксалилхлорида и триэтиламина. 4. Способ по п. 1, отличающийся тем, что осуществляют взаимодействие альдегида общей формулыи фосфоната общей формулыв условиях реакции Виттига-ХорнераЭммонса. 5. Способ по п. 1, отличающийся тем, что защитную группу гидроксильной группы в положении 11 у соединения общей формулыудаляют в кислой среде. 6. Способ по п. 1, отличающийся тем, что восстановление соединения общей формулыпроводят с помощью диизобутилалюминий-2,6-дитрет-бутил-4-метилфеноксида. 7. Способ по п. 1, отличающийся тем, что соединение общей формулыподвергают гидролизу в основной среде. 8. Способ по п. 1, отличающийся тем, что кислоту формулыпереводят в ее натриевую соль и полученную соль выделяют. 3 10309 1 2008.02.28 9. Соединение общей формулы 2 где 1 представляет собой метильную или этильную группу 2 представляет собой алкильную группу с прямой или разветвленной цепью, содержащую 1-4 атома углерода. 10. Соединение общей формулы , приведенной в п. 9, где 1 представляет собой этильную группу, а 2 представляет собой метильную группу. 11. Соединение общей формулы 2 гдепредставляет собой метильную или этильную группу 2 представляет собой алкильную группу с прямой или разветвленной цепью, содержащую 1-4 атома углерода. 12. Соединение общей формулы , приведенной в п. 11, где 1 представляет собой этильную группу, а 2 представляет собой метильную группу. 13. Соединение общей формулы 2 гдепредставляет собой метильную или этильную группу 2 представляет собой алкильную группу с прямой или разветвленной цепью, содержащую 1-4 атома углерода. 14. Соединение общей формулы , приведенной в п. 13, где 1 представляет собой этильную группу, а 2 представляет собой метильную группу. 4 10309 1 2008.02.28 Настоящее изобретение относится к новому способу получения берапроста формулы и его солей и к новым промежуточным продуктам общих формул ,и 2 применяемым в новом синтезе, где 1 представляет собой метильную или этильную группу, 2 представляет собой алкильную группу с прямой или разветвленной цепью, содержащую 1-4 атома углерода. Соли берапроста формулы , в частности натриевая соль, являются производными простациклина для перорального применения, которые эффективно применяются для лечения хронического заболевания периферических сосудов, артериального тромбоза и легочной гипертензии. Активный фармацевтический ингредиент формулыи его соли,5 10309 1 2008.02.28 применяемые в коммерческих фармацевтических композициях, представляют собой рацемические соединения, содержащие четыре стереоизомера. Синтез соединения формулыи его солей описан в опубликованной заявке на европейский патент 084856 А, в опубликованной заявке на японский патент 59-134787 А и в публикации 55, стр. 2449-2474 (1999), а краткое описание синтеза приведено на схеме 1. Схема 1 3 На схеме 1 обозначениепредставляет собой трет-бутилдиметилсилильную группу, Ас означает ацетильную группу, реакция означает реакцию ВиттигаХорнера-Эммонса. Из схемы 1 и известного уровня техники можно заметить, что путь синтеза в соответствии с уровнем техники в данной области довольно длинный, а получаемый при этом выход продукта невысокий. Задачей настоящего изобретения является разработка более короткого синтеза целевого продукта с более высоким выходом. Неожиданно было обнаружено, что защита первичной гидроксильной группы чувствительной к кислоте защитной группой и защита вторичной гидроксильной группы чувствительной к основанию защитной группой необязательны, и соответственно последующее удаление защитной группы с первичной гидроксильной группы, если применять одну, специально выбранную защитную группу, которая в то же время делает возможным селективное окисление. Удаление описанной выше защитной группы перед восстановлением оксо-группы в положении 15 и тщательный выбор восстановителя увеличивают стереоселективность восстановления и выход синтеза в целом. 6 10309 1 2008.02.28 Согласно настоящему изобретению, способ получения соединения формулы или его солей, в частности его натриевой соли, состоит в том, что осуществляют взаимодействие соединения общей формулы 2 где 2 представляет собой алкильную группу с прямой или разветвленной цепью, содержащую 1-4 атома углерода,с соединением общей формулы(1)3- , 1 гдепредставляет собой метильную или этильную группупредставляет собой хлор, бром, йод, 32, азидо-, циано- -О-С(СН 3)СНС(О)-СН 3, -аллильную, -С(ОСН 3)С(СН 3)-СН 3, 1-имидазолильную, трихлорацетильную,(СН 3)3, -(СН 3)3, (3)3 или -О-(СН 3)3-группу, описанную в следующей литературе,,,.(1995)3-905617-08-0. Полученное соединение общей формулы 2 где 1 и 2 имеют указанные выше значения,7 10309 1 2008.02.28 окисляют до альдегида общей формулы 2 гдеиимеют указанные выше значения. Далее полученный альдегид после выделения или без выделения подвергают взаимодействию с фосфонатом общей формулы 3 гдепредставляет собой алкильную группу с прямой или разветвленной цепью, содержащую 1-4 атома углерода Затем у полученного соединения общей формулы 2 гдеиимеют указанные выше значения удаляют защитную группу в положении 11. После этого полученное таким образом соединение общей формулы 2 где 2 имеет указанное выше значение, 8 10309 1 2008.02.28 восстанавливают с получением соединения общей формулы 2 гдеимеет указанное выше значение,которое затем подвергают гидролизу и выделяют кислоту формулы , которую, при необходимости, путем взаимодействия с основанием переводят в ее соль и затем соль выделяют, или полученную кислоту формулы , при необходимости, без предварительного выделения переводят в соль и выделяют полученную таким образом соль. Во время осуществления описанного выше способа соединение общей формулывзаимодействует с соединением общей формулы , пригодным для введения триэтилсилильной или триметилсилильной группы, где 1 представляет собой этил, а -хлор,бром, йод, 32, азидо-, циано- -О-С(СН 3 )СН-С(О)-СН 3 , аллильную,-С(ОСН 3)С(СН 3)-СН 3, 1-имидазолильную, трихлорацетильную, (3)3, -(3)3,(3)3 или -О-(СН 3)3-группу, описанную в следующей литературе,,,.(1995)3-905617-08-0 предпочтительны триметилсилилгалогениды или триэтилсилилгалогениды, в частности хлориды или специфические производные, перечисленные выше. Полученные дисилилированные диолы общей формулыокисляют до альдегидов общей формулыпреимущественно смесью диметилсульфоксида, оксалилхлорида и триэтиламина. Альдегиды общей формулывзаимодействуют с фосфонатами общей формулыв условиях реакции Виттига-Хорнера-Эммонса (. . 89, стр. 863-927 (1989 с образованием соединений общей формулы . После удаления триэтилсилильной или триметилсилильной защитной группы, предназначенной для защиты вторичной гидроксильной группы в положении 11 в соединениях общей формулы , в кислой среде получают соединения енонольного типа общей формулы . Стереоселективное восстановление соединений общей формулыпроводят, предпочтительно используя диизобутилалюминий-2,6-дитрет-бутил-4-метилфеноксид, и получают соединения формулы . Предпочтительно соединение общей формулыподвергают гидролизу в основной среде, который приводит к берапросту формулы . Соли соединения формулыможно получить при взаимодействии указанного соединения с основаниями. Образование соли можно проводить после выделения берапроста формулыили без его выделения. Предпочтительно кислоту формулыпереводят в ее натриевую соль и полученную соль выделяют. Для получения натриевой соли берапроста в качестве основания наиболее предпочтительно применяют гидроксид натрия. Соединения общей формулыи фосфонаты общей формулы , применяемые в способе, соответствующем настоящему изобретению, можно получить так, как описано,например, в публикации 55, стр. 2449-2474 (1999). Соединения общей формулыотносятся к коммерчески доступным соединениям. 9 10309 1 2008.02.28 Дополнительными объектами настоящего изобретения являются промежуточные продукты общих формул ,и , применяемые в способе получения берапроста формулы . Соединения общей формулы 2 где 1 представляет собой метильную или этильную группу 2 представляет собой алкильную группу с прямой или разветвленной цепью, содержащую 1-4 атома углерода. Предпочтительно 1 представляет собой этильную группу,2 представляет собой метильную группу. Соединения общей формулы 2 где 1 представляет собой метильную или этильную группу 2 представляет собой алкильную группу с прямой или разветвленной цепью, содержащую 1-4 атома углерода. Предпочтительно 1 представляет собой этильную группу,2 представляет собой метильную группу. Соединения общей формулы 2 где 1 представляет собой метильную или этильную группу 2 представляет собой алкильную группу с прямой или разветвленной цепью, содержащую 1-4 атома углерода. Предпочтительно 1 представляет собой этильную группу,2 представляет собой метильную группу. 10 10309 1 2008.02.28 Настоящее изобретение более подробно будет описано с помощью следующих примеров, не ограничивающих формулу изобретения. Пример 1. Соединение общей формулы , где 1 представляет этильную группу, а 2 представляет метильную группу 1,84 г (6 ммоль) диола общей формулы , где 2 представляет метильную группу,растворяют в 10 мл пиридина. Раствор перемешивают и добавляют 2,35 мл (14 ммоль) триэтилсилилхлорида. Перемешивание продолжают в течение 30 мин и затем реакционную смесь выливают в смесь, состоящую из 50 мл воды и 20 мл гексана. Водную фазу экстрагируют гексаном (210 мл) и объединенный раствор в гексане промывают 30 мл 1 М водного раствора 4, 30 мл воды, 30 мл 1 М раствора 3, 230 мл воды, затем насыщенным раствором . Гексановый раствор сушат над 24 в течение одного часа и затем упаривают. Указанное в заголовке соединение получают в виде бесцветного маслянистого вещества. Выход 3,08 г (96 ).- (гексанэтилацетат 101)0,32. 1 Н ЯМР (400 мГц, 66), Н (м.д.) 0,54 кв., 0,63 кв. 12 Н 7,9 Гц (23)3 0,95 т, 1,02 т 18 Н 7,9 Гц (СН 2 СН 3)3 2,05 м, 2,06 м 3 Н 10-Н, 3-Н 2 2,16 м, 2,22 м,2,25 м 4 Н 12-Н, 2-Н 2, 10-Н 2,70 м 2 Н 4-Н 2 3,32 с 3 Н ОСН 3 3,51 дд 1 Н 8,8, 7,0 Гц 8-Н 3,63 м 2 Н 13-Н 2 4,01 тд 1 Н 7,4, 5,8 Гц 11-Н 4,85 ддд 1 Н 9 7,2, 5,4 Гц 9-Н 6,85 т 1 Н 7,3 Гц 2-Н 6,93 д 1 Н 7,3 Гц 1-Н 7,19 д 1 Н 7,3 Гц 3-Н. 13 С ЯМР (100 мГц, 66),(м.д.) 5,5, 5,9 (23)3 7,7, 7,8 (23)3 26,1 С-3 30,5 С-4 34,3 С-2 43,6 С-10 47,9 С-8 51,5 ОСН 3 59,0 С-12 63,0 С-13 73,6 -11 85,9 С-9 121,4 С-2 123,3 С-3 124,3 С-5 129,6 -1 132,0 С-7 158,8 С-6 173,9 С-1. Пример 2. Соединение общей формулы , где 1 представляет этильную группу, 2 представляет метильную группу 0,27 мл (3 ммоль) оксалилхлорида растворяют в 3 мл дихлорметана и охлаждают смесь до -60 С. К полученному раствору при -60 С по каплям добавляют 0,44 мл(6,2 ммоль) диметилсульфоксида, растворенного в 3 мл дихлорметана. После перемешивания в течение 5 мин к смеси добавляют 1,07 г (2 ммоль) соединения общей формулы , полученного по примеру 1, растворенного в 2 мл дихлорметана. Смеси дают нагреться до -35 С и перемешивают ее при указанной температуре в течение 30 мин. Реакционную смесь охлаждают до -60 С и добавляют 1,42 мл (10 ммоль) триэтиламина. Смесь перемешивают в течение 15 мин и при комнатной температуре добавляют 10 мл воды и 7 мл 10 М водного раствора 4. Водную фазу дважды экстрагируют 5 мл дихлорметана. Объединенную органическую фазу промывают 10 мл 1 М водного раствора аНСО 3, 10 мл воды и 10 мл насыщенного раствора . Органическую фазу сушат над 24, упаривают в вакууме, получая при этом указанное в заголовке соединение в виде желтого маслянистого вещества, которое после очистки или без очистки можно применять на стадии следующей реакции. Выход 0,83 г (99 ).- (гексанпростой диизопропиловый эфир 11)0,44,- (гексанэтилацетат 31)0,52. 1 Н ЯМР (400 мГц, 66), Н (м.д.) 0,41 кв. 6 Н 8,0 Гц (23)3 0,84 т 9 Н 8,0 Гц(СН 2 СН 3)3 1,94 м, 2,02 м 3 Н 10-Н, 3-Н 2 2,17 м, 2,20 т 3 Н 7,4 Гц 10 Н, 2-Н 2 2,64 м 2 Н 4-Н 2 2,73 т 1 Н 6,0 Гц 12-Н 3,32 с 3 Н ОСН 3 3,73 дд 1 Н 8,7, 6,4 Гц 8-Н 4,04 кв. 1 Н 6,0 Гц 11-Н 4,69 м 1 Н 9-Н 6,75 т 1 Н 7,4 Гц 2-Н 6,88 д, 6,91 д 2 Н 7,4 Гц 1-Н, 3-Н 9,46 д 1 Н 1 Гц 13-Н. 11 10309 1 2008.02.28 С ЯМР (100 мГц, 66), С (м.д.) 5,6 (СН 2 СН 3)3 7,5 (СН 2 СН 3)3 26,0 С-3 30,4 С-4 34,2 С-2 43,7 С-10 45,9 С-8 51,6 ОСН 3 68,8 С-12 73,9 С-11 85,7 С-9 121,6 С-2 123,2 С-3 124,3 С-5 129,9 С-1 130,4 С-7 158,7 С-6 173,9 С-1 200,6 С-13. Пример 3. Соединение общей формулы , где 1 представляет этильную группу, 2 представляет метильную группу 92 мг масляной дисперсии (60 ) гидрида натрия (2,3 ммоль) суспендируют в 2 мл толуола, 0,51 мл (2,2 ммоль) фосфоната общей формулы , где 3 представляет метильную группу, растворяют в 1 мл толуола и добавляют к смеси при 15 С в атмосфере азота. Смесь перемешивают в течение 20 мин при 15 С и затем полученный раствор, содержащий натриевую соль фосфоната, добавляют по каплям к 0,83 г (2 ммоль) полученного по примеру 2 неочищенного альдегида общей формулы , растворенного в 2 мл толуола при-10 С. После перемешивания в течение двух часов к реакционной смеси добавляют 10 мл воды и 2 мл 1 М водного раствора 4 и перемешивают в течение двух минут. Водную фазу дважды экстрагируют 5 мл толуола, а объединенный раствор в толуоле экстрагируют 10 мл воды, 10 мл 1 М водного раствора 3, 10 мл воды и 10 мл насыщенного раствора . Раствор сушат над 24, упаривают в вакууме, получая при этом указанное в заголовке соединение в виде желтого маслянистого вещества, которое можно применять на стадии следующей реакции без очистки. Выход 1,2 г ( 99 ).- (гексанэтилацетат 31)0,54. 1 Н ЯМР (400 мГц, 66), Н (м.д.) 0,47 кв., 0,48 кв. 6 Н 7,8 Гц (23)3 0,90 т,0,91 т 9 Н 7,8 Гц (СН 2 СН 3)3 1,16 д 3 Н 6,9 Гц 21-Н 3 1,54 м 3 Н 20-Н 3 2,02 м 2 Н, 3-Н 2 2,21 т 7,5 Гц 2-Н 2 2,67 м 2 Н 4-Н 2 3,04 м 1 Н 8- 3,32 с 3 Н ОСН 3 3,59 м 1 Н 11-Н 4,67 м 1 Н 9-Н 6,08 дд 1 Н 15,3, 2,3 Гц 14- 6,78 м 2 Н 13-Н, 2-Н 6,91 м 2 Н 1-Н, 3-Н. 13 С ЯМР (100 мГц, 66), С (м.д.) 4,0 С-20 5,7 (23)3 7,6 (23)3 17,0 С-21 23,2, 23,3 С-17 26,0 С-3 30,4 С-4 34,2 -2 43,7 С-10 45,2, 45,3 С-16 50,3 С-8 51,6 ОСН 3 59,6 С-12 77,1 С-11 77,8, 77,9, 78,0 С-18, С-19 84,9 С-9 121,6 С-2 122,8 С-3 124,5 С-5 130,1 С-1 130,4 С-7 130,7 С-14 146,8,146,9 -13 158,6 С-6 173,8 С-1 200,5 С-15. Пример 4. Соединение общей формулы , где 2 представляет метильную группу 1,2 г (2 ммоль) неочищенного силиленона общей формулы , полученного в примере 3, растворяют в 20 мл метанола и добавляют к нему 0,15 мл (1,8 ммоль) концентрированной соляной кислоты. Смесь перемешивают в течение 5 минут при 25 С и добавляют к ней 0,16 г (1,9 ммоль) твердого 3. Полученную смесь перемешивают в течение 10 мин при 25 С и затем упаривают в вакууме. Остаток растворяют в толуоле, неорганические соли отфильтровывают, а фильтрат упаривают. Сырой продукт очищают колоночной хроматографией, получая при этом указанное в заголовке соединение в виде бледножелтого маслянистого вещества. Выход 0,46 г (56 ). 10309 1 2008.02.28 С ЯМР (100 мГц, 3), С (м.д.) 3,5 С-20 16,4 С-21 22,3 С-17 24,7 С-2 29,1 С-4 33,4 С-3 41,8 С-10 44,1 С-16 50,3 С-8 51,5 ОСН 3 58,6 С-12 76,4 С-11 76,6, 77,2 С-18, С-19 84,6 С-9 120,7 С-2 121,9 С-3 123,5 С-5 129,1, 129,2 С-14,С-1 129,7 -7 146,0 С-13 157,2 С-6 174,1 С-1 201,7 С-15. Пример 5. Соединение общей формулы , где 2 означает метильную группу 5,14 г (22 ммоль) 2,6-ди-т-бутил-4-метилфенола растворяют в 50 мл дистиллированного толуола в атмосфере азота. К полученному раствору добавляют по каплям 1,55 г(11 ммоль) диизобутилалюминийгидрида, растворенного в 8 мл дистиллированного толуола. Реакционную смесь перемешивают в течение одного часа при 0 С, затем охлаждают до -78 С. К полученному реагенту диизобутилалюминий-2,6-ди-т-бутил-4-метилфеноксиду при -78 С медленно по каплям добавляют 0,45 г (1,1 ммоль) соединения общей формулы , полученного по примеру 4 и растворенного в 4 мл дистиллированного толуола. Реакционную смесь перемешивают в течение ночи при -50 С, а затем гасят 27 мл 2 М водного раствора соляной кислоты. После перемешивания в течение 30 мин фазы разделяют, водную фазу дважды промывают 15 мл толуола, объединенную органическую фазу промывают 20 мл насыщенного раствора , 15 мл 1 М водного раствора 3 и 220 мл насыщенного раствора . Органическую фазу сушат над 24 и упаривают в вакууме. Указанное в заголовке соединение получают после очистки остатка хроматографией в виде бесцветного маслянистого вещества. Выход 0,25 г (55 ).- (толуолдиоксануксусная кислота 20101)0,50. 1 Н ЯМР (400 мГц, 3), Н (м.д.) 1,02 т 3 Н 6,8 Гц 21-Н 3 1,79 м 1 Н 16-Н 1,80 т, 1,81 т 3 Н 2,6 Гц 20-Н 3 1,88-2,18 м 6 Н 3-Н 2, 10-Н, 17-Н, ОН 2,25 м 1 Н 17-На 2,33 м 1 Н 2-Н 2 2,48 м 1 Н 12-Н 2,61 м 2 Н 4-Н 2 2,66 м 1 Н 10-Н 3,46 т,3,47 т 1 Н 8,2 Гц 8-Н 3,66 с 3 Н ОСН 3 3,95 м 1 Н 11-Н 4,07 т, 4,21 дд 1 Н 7,0,5,8, 4,9 15-Н 5,12 м 1 Н 9-Н 5,63 дд 1 Н 15,5,5,8, 7,0 14-Н 5,70 дд,5,71 дд 1 Н 15,5, 8,4,15,5, 8,0 13-Н 6,77 м 1 Н 2-Н 6,97 м 2 Н 1-Н, 3-Н. Пример 6. Берапрост формулы 0,246 г (0,6 ммоль) соединения общей формулы , полученного в примере 5, растворяют в 1 мл метанола и к полученному раствору медленно по каплям добавляют 1 мл 1 М водного раствора гидроксида натрия. После перемешивания в течение часа метанол отгоняют из реакционной смеси в вакууме. Водный остаток разбавляют 10 мл воды, экстрагируют простым метил-трет-бутиловым эфиром и объединенную органическую фазу промывают насыщенным раствором , сушат над 24 и упаривают. Остаток после упаривания кристаллизуют из смеси этилацетат-гексан, получая при этом указанное в заголовке соединение в чистом виде в виде бесцветных кристаллов. Выход 0,21 г (87 ). 10309 1 2008.02.28 С ЯМР (100 мГц, 3), С (м.д.) 3,5, 3,6 С-20 14,7, 15,8 С-21 22,3, 22,6 С-17 24,6 С-2 29,1 С-4 33,1 С-3 38,2, 38,3 С-16 41,2 С-10 50,4 С-8 58,8 С-12 75,8,76,3, 76,4 С-11, С-15 77,2, 77,4 С-18, С-19 84,5, 84,6 С-9 120,6 С-2 121,9 С-3 123,2 С-5 129,0 С-1 129,7 -7 132,3, 133,0, 133,8, 134,0 С-13, С-14 157,2 С-6 178,3 С-1. Пример 7. Натриевая соль берапроста (натриевая соль соединения формулы ) 0,199 г берапроста растворяют в 2 мл метанола, к полученному раствору добавляют 0,5 мл 1 М водного раствора гидроксида натрия и после перемешивания растворитель выпаривают в вакууме, получая при этом указанную в заголовке соль в виде бесцветных кристаллов. Выход 0,21 г (100 ). Температура плавления 205 С. 1 Н ЯМР (400 мГц, -6), Н (м.д.) 0,90 д, 0,92 д 3 Н 6,7 Гц 21-Н 3 1,75-1,55 м 7 Н 10 Н, 16-Н, 3-Н 2, 20-Н 3 1,89 т 2 Н,7,6 Гц 2-Н 2 1,94 м 1 Н 17-Н 2,16 кв 1 Н,8,5 Гц 12-Н 2,25 м 1 Н 17-На 2,44 т 2 Н 7,5 Гц 4-Н 2 2,50 окт. 1 Н 10-Н 3,39 т 1 Н,8,5 Гц 8-Н 3,72 тд 1 Н 8,5, 6,1 Гц 11-Н 3,84 т, 3,96 т 1 Н,6,5, 6,0 Гц 15-Н 4,85 шир. 2 Н, ОН 5,01 дт 1 Н,8,5, 6,6 Гц 9-Н 5,46 дд, 5,47 дд 1 Н 15,4,6,5 Гц,15,4, 6,0 Гц 14-Н 5,65 дд, 5,66 дд 1 Н 15,4, 8,5 Гц 13-Н 6,71 м 1 Н 2-Н 6,92 м 2 Н 1-Н, 3-Н. Во время проведения описанной выше процедуры тонкослойной хроматографии(ТСХ) применяли пластины 60 254, толщина слоя составляет 0,2 мм,длина пластин 5 см. 13 Национальный центр интеллектуальной собственности. 220034, г. Минск, ул. Козлова, 20. 14
МПК / Метки
МПК: C07D 307/00
Метки: способ, получения, берапроста, солей
Код ссылки
<a href="https://by.patents.su/14-10309-sposob-polucheniya-beraprosta-i-ego-solejj.html" rel="bookmark" title="База патентов Беларуси">Способ получения берапроста и его солей</a>
Предыдущий патент: Ингибитор коррозии к минеральным маслам
Следующий патент: Электрооптический анализатор спектра
Случайный патент: Способ поверхностной модификации резинотехнических изделий