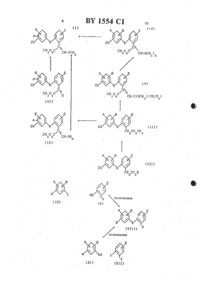
Производные пропеновой кислоты или их стереоизомеры
Номер патента: 1554
Опубликовано: 16.12.1996
Авторы: Вивьен Маргарет Энтони, Поль Джон де Фрейн, Патрик Джелф Кроули, Алан Джон Бакли, Кристофер Ричард Эйлз Годфри, Майкл Гордон Хатчингз, Стивен Пол Хиней, Кевин Бьютмент, Ян Фергусон, Джон Мартин Клаф
Текст
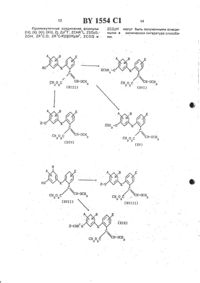
(жможно монозамещенньтй Срок шпатом, Сд-Сггалоицшпсгшом, Сд-С 4 ашшлгио, шанс, ншро, фенилом, НОдС,Сд-Сгшпсоксшшрбонилом или С 1-С 4 атпшлсульфонилом, или моно- или дизамещенньлй Сд-Сд-атпсокси, или моно-,ди- или тризамещенньщ галогеном, Шт дизамещенный галогеном и одной из Сд-Сгалтсил или Сд-Сгалкилтио, или дизамещенный С 1-С 4-алкил и С 1-С 4 алкилтио), пиразинил (возможно монозамещенный галогеном или циано,или дизамещенный Сд-Сгалшлом),пиридазинил (возможно монозамеЩенный С 1-С 4-ЗЕТКОКСИ, феннлом или аминокарбонилом, или моно- или дизамещенный твлогеном, или дизамещенный галогеном и С 1-С 4-ЭЛКИЛОМ) бензотиазолил, тиенил (возможно монозамещенньшй пиразолилом, Который сам по себе дизамещен Сд-Сд-шпшлом и Сд-Сгталотщадпшлом, или пирициниь лом, который сам по себе возможно монозамещен нитро- или дизамещен талотеном), 124-триазолил индексации-жил(монозамещеннъхй шлогеном), 1,3,5 триазинил (дизамещенный галогеном,или дизамещенный галогеном и С 1-С 4 алкокси), тиазолил (возможно монозамещенный нитро, или моно- или дизамещенный Сд-Сгалшшом), бензоксазолил, пиридинил-М-оксид, тиено-(2,3 сп-пиримидинил, пирролил (возможно монозамешнный Сд-Сд-алюшом),изоксазолил (монозамещеннътй С 1-С 4 алкилом), 1, 3, Фтиациазолил, пиразолил (замещенный плетеном и двумя Сгсд-атпсильными группами) или 1,2,4-триазинил (монозамещенный фенилом), при условии, что, когда 2 - незамещенный фенил а Х и К - оба кислород, то А не водород, или их стереоизомеры. Приоритет по признакам 15.0987 при А-Н, галоген, Сд-Сд-алшш,Сд-Сд-адшокси К-кислород, Х-Б, 5(О),(О)2 МН Ы(С 1 С 4 а-НКРШ)1 СН 2 СО СН 2 СН 2 СНСН, ОСН 2, СН 2 О, 8 СН 3,(О) СН 2, 5(О)1 СН 1, СОЫ(С 1-С 4 алкгш) Н(С 1-С 4-ал 1 ош)СН 2 СОд, 502 С 3(О 2)О,СОМН, ЫНСО, ЪТН 5(О)2 СН(С 1-С 4 алкидпО, СОБ, БСО, ЪТСН, СН 2 СНдО,М(С 1 С 4-алюш)11 СН, СНСНСН 2 О О,ЫЪТ 1 Т(С 1-С 4-а.пкил) СО, 5(0)2 ЫН 2-феннл, монозамещенный Сд-Сб-шпшлом, Сд-Сд-адпсокси, Сд-Сд-галоицшпсршом,фенокси, феннлом, златом, ОН, 1-(С 1 С 4 алкоксикарбонидп-З-(С-С 4-алко 1 си) винилом, Сд-Сггалоидалкокси, Сд-Сд-алкоксикарбонилом, моно- или дизамещенньтй галогеном, нитро, Сд-Сгалшалом, пиано нафтил, хинолинил, пиридинил, монозамещенный Сд-Сгапюишом, С 1-С 4- алкоксикарбонилом, амино, галогеном, нитро,Сд-Сгалюшкарбониламино, ди (Сд-Сдалкилсульфонъш) амино, СН(О)ЫН моноили дизамещенный Сд-Сггалоидалюшом,циано, дизамещенный амино и пиано, галотеном, СгСд-алкокси, нитро и Циано,диЮд-Сгалшш) амино Сд-Сгалкокси,замощенный пиано и двумя С 1-С 4 алюшьными группами, пиримидинил, монозамещенный С 1-С 4-алшшом, Сгсггалоидалкилом, Сд-Сггалоидапъсилом, Сд-Сд-алхсшгтио, циано, нитро фенилом, НО 2 С, С 1-С 4 алкоксикарбонилом, Сд-Сд-алюиглсульфоНИЛОМ, моно- или дизамещенный Сд-С 4 алкокси, моно-, ди- или тризамещенный галогеном, дизамещенньлй галогеном и Сд-Сд-алшшом, Сд-Сггалоидалкьшом,Сд-Сгшпоалом и Сд-Сгалпошом и Сд-С 4 ашсшпио гшразинил, монозамещенный галохеном, пиано, дизамещенный С 1-С 4 алкилом, пиридазинил, монозамещенный Сд-Сд-алкокси, фенилом аминокарбонилом, моно- или дизамещенньхй галогеном,дизамещенный галогеном и Сд-Сддалтсилом бензотиазолил, тиенил, монозамещенный пиразолилом, дизамещнньшм, в свою очередь, С 1-С 4-апшшом и Сд-Сдгалоидалюшом, пиридинил, возможно замощенный нитро- или дизамешенный галогеном, 1,2,3 триа 3 олил, хиноксалинил,монозамещенный галотеном, 1,3,5-триазинил, дизамещнный плетеном или галогеном и С 1-С 4-алкокси, тиазолил, возможно монозамещенный нитро моно- или дизамещенный Сд-Сд-алкокси, бензоксазолил,пиридинил-Ы-оксид, тиено-(2,3-с 1)пиримидинил, пирролип, возможно монозамещенный Сд-Сгалюшом, изоксазолил, дизамощенный С 1-С 4-шпшлом, 1,3,4-тиадиазолил, пиразолил, замощенный галогеном и двумя С 1-С 4-алкилами, 12,4-триа.зинил монозамешенный фениломИзобретение относится к органической химии. а именно к производным пропеновой кислоты общей формулы 12-х снзогс сноснэ или их стереоизомеров. где А представляет собой водрод. Гапоген, Ст-Сд-алкил Ст-Сл алкокси. гидрокси. фенокси или Ст-Сд алкипкарбонил к представляет собой кислород ипиеРУ Х предъставпяет собой О. (0)п. МН. МН . СН 2. СНН . СО. СН 2 СН 2. СНСН. ОСН 2. (снзно сня 1 о. осн 2 о. 5(0)сн 2.(О)СН 2 О. МК- СН. СОО. ООС. 5020. СОСН 2 О. сосн в 1 о. сомн, ннсо. МН 5 О 2. СОЗ. БСО, ММ. СНЮСО. С 25 С 0. СН 2 МНСО.СН 2 ОМСН.ОСН 2 СН 2 .М СН. СН 2 О ОМН. СН-СНСН 20. (П 2 РСН 2 О. М ОН , МСН. СНЮН). СО 2 СН 2. 5 СН 2 О. н о. всоьмн или сонкд к представляет собой С 1-С 4 алкил К представляет собой фенил п составляет 0.1 или 2 т составляет 123.4 или 5 О представляет собой галоидный анион 2 представляет собой фенипфенокси, щнипом. амино, гидрокси. 1-(С 1 Сл алкоксикарбониЩ--(Ст-Сд апкокси)-винил, С 1-С 4 галоидалкокси или С 1-С 4 алкоксикарбонилгруппой или моноц или дизамещенный галогеном. нитро. С 1-С 4 алкипом или цианогруппой) нафтил. хинопинил. пиридинил (возможно монозамещенный С 1 С 4 алкилом. Ст-Сц алкоксикарбонилом, амино. галогеном. нитро. Ст-Са алкилкарбониламино. ди-(Ст-Сл алкилсульфонит-аминогруппой или СН(О)МН или моно- или дизамещенный С 1-С 4мещенный аминогруппой и одной из циано. галоген или С 1-С 4 апкоксигруппы. или диза мещенный нитрогруппой и одной из циано.галоген, ди-(СгСа апкил)амино или Ст-Сд алкоксигруппы. или замещенный цианогруппой и двумя Са-Сд апкильными группами, пиримидинип. возможно монозамещенныйСт-Са алкилом. Сз-Сл галоидалкилом. С 1-С 4 циано. нитро. фенипом. НО 2 С. С 1-С 4 алкоксикарбонилом или Ст-Сд алкилсульфонилом. или моно- или дизамещенный Ст-Сд алкокси. или моно-. ди- или тризамещенный галогеном. или дизамещенный га логеном и одной из С 1-С 4 алкил или С 1-С 4алкиптио. или дизамещенный Съ-Сд алкил и Ст-Са апкилтио, пиразичип. возможно монозамощенный галогеном или циано. или дизамеЩЕННЫЙ С 1-С 4-алкокси. фенилом илиаминокарбонилом. или моно- или дизамещенный галогеном. или дизамещенный гапогеном и Ст-Са алкипом). бензотиазолил. тиенил (возможно монозамещенный пиразолилом), который сам по себе дизамещенпиридинилом который сам по себе. возмож НО МОНОЗЗМСЩВН НИТВО ИЛИ ДИЗЗМЕЩВНННЙгалогеном. 1.2.4-триазолил. хиноксалинил. монозамещенный галогеном. 1.3.5-триазинип. диэамещенный галогеном. или дизамещенный галогеном и С 1-С 4 алкокси. тиазолил возможно. моноэамещенный нитро или моно- или дизамещенный С 1 -С 4 алкилом. бензоксазолил. пиридинил-М-оксид,тиено-ЩЗ-о пиримидинип. пирролип возможно монозамещенный Ст-Сд алкилом. изоксазолил монозамещенный с 1-с 4 алкилом. 1.3.4-тиадиазолип. пиразолил. замещенный галогеном и двумя С 1-С 4 апкильными группами или 1.2.4-триаэннил,монозамещенный фенипом. при условии,что когда 2 представляет собой незамещенный фенил. а Х и К оба представляют собой кислород. тогда А не является водородом. обладающие фунгицидной активностью. Изобретение иллюстрируется соединениями, перечисленными в табл. 1-4 метилЗ-метоксипропеноатнад группа имеет(Ы-конфигурацию. - Табл. 3 включает 446 соединение приведенной формулы. Для первых 445 соединений все значения Х. В. Б. А. В и Е указаны в табл. 1. Т.е. соединения 1-445 те же, что и в табл. 1. 2 -за исключением значения К. которому в табл. 1 соответствует кислород. а в табл. 4 - сера. Соединение 446 отвечает приведенной формуле. где Х означает кислород и А. В. Е). Е и Б все означают водород. Описание получения соединения 446 приве дено в примере 11.Табл. 4 включает 320 соединений приведенной общей формулы. где все значения 2.1-320 те же. что и в табл. 3 за исключением значения К, которому в табл. 2 соответствует кислород. а в табл. 4 сера.В табл. 5 даны отдельные данные спектров Н-ЯМР.В табл. 5 приведены данные протонного ЯМР для некоторых соединений табл. 1-4. Химические сдвиги обозначают в млн от тетраметилсилана. во всех случаях в качестее растворителя используют дейтерированный хлороформ. Столбец. озаглавленный частота. относится к рабочим частотам спектрометра ЯМР. В табл. 5 используют следующие сокращения уш - уширенная полоса с - синглет д дублет т триплет к квартет М мультиплет.тезированы различными способами. некоторые из которых иллюстрируются Схемами реакцкяй -/1. Во всех схемах символы 2. Х. А. В. Е. К. Н. Н 2. 1723 и 15 принимают вышеуказанные значения. Не означают водород или металл (такой как натрий или калий). П означает алкил и 1. означает отходящуюгруппу. ТЭКУЮ как ГЗЛОИДИД (бромид. ХЛОПИДили йодид). СН 35 Од-анион или сульфониланион. Все превращения. описываемые схемами -/. проводят в приемлемых температурных условиях и либо в приемлемом раствориле. либо без растворителя.Схема 1 иллюстрирует споособ, в котором метил-бета-метоксипропеноатную группу образуют на конечных этапах синтеза соединения изобретения из предшественников с предварительно созданным скелетом из 3 ароматических циклов. Или ке метил-бетаметоксипропеноатная группа может быть образована на ранних стадиях синтеза. в этом случае конечная стадия или стадии заключаются в введении остальных деталей соединения изобретения с образованием скелета из 3 ароматических циклов. Примеры методик подобного рода показаны на схемах -Х.Независимо от порядка проведения остапьных стадий синтеза соединений изобретения простая эфирная или тиоэфирная дифенильная связь общая для всех соединений изобретения может быть образована в одной из реакцией сшивания, показанной на схеме . Обзор синтеза простой эфирнойсвязи по Ульману можно найти в Успехахстберг. См. также О.Напоз. 51.5 ННгаП. .Н.В. утюги. ТЕ. Чеглоеуеп. щнекегосуегйс спет. 1986. 23. 1333. Такое сшивание часто проводят в присутствии катализатора. состоящего из переходного металла или соли переходного металла. или соединения переходного металла. например меди. соли или соединения меди или их смеси. На схеме г символ ЧМ представляет либо группу 2-Х-. где 2 и Х принимают указанные значения. либо группу. которая стандартными способами может быть превращена в группу 2-Х-. где И их принимают указанные значения. либо группу. которая стандартными способами может быть превращена в группу -Х-. к примеру может представлять -ОН. -5 Н или-МНЕ. Символ У представляет либо альфаметил в метил-бета-метоксипропеноатной группе соединений изобретения. либо группу. которая может быть превращена в указанную группу стандартными способами. описанными а литературе и/или показанными на схеме 1быть группойформул -СНСООН ДндсооМе или -СНО. В контексте схемы Н символ предпочтительно представляет галоид. Так. Соединение формулы (Х) реагирует с соединением формулы (ХН) в условиях реакции Ульмана. приведенных выше. с образова- нием промежуточного соединения формулы(УПР). В виде примера одной из таких реакций сшивания, показанных на схеме . замещенные З-феноксифенолы в виде их солей вступают в реакцию сщ-ивания с солями 2-бром или хлорфенилуксусной кислоты с образованием врезультате подкисления замещенных 2-(3-феноксифеноксюфенилуксусной кислот (со, например. патент Великобритании М 2078-743. выдан лага слет. а. 27.06.80). Или же промежуточные соединения формулы (/ могут быть получены взаимодействием соединений формулы (Х) с соединениями формулы (Х) в уже описанных условиях реакции Ульмана. Изобретения включает способ получения соединения формулы . заключающийся в рекции соединен я общей формулы (хна)снзогс св-оспа где представляет галоид. с фенолом или тиофенолом общей формулы Шав присутствии основания или с солью фенола или тиофенола формулы (Ха) предпочтиТВЛЬНО Б присутствии КВТВЛИЗВТОРЭ. содержащего соответствующий переходной МВТЭПЛ. СОЛЬ ИЛИ СОЕДИНЕНИЕ ПЕОХОДНОГО МЕТЭЛЛЗ ИЛИ ИХ СМЕСЬ.Соединения изобретения формулы Емо- тут быть получены обработкой фенилацетатов формулы Н основанием (таким как гидрид натрия или метоксид натрия) и метилформатом. Если затем в реакционную смесь добавить реагент формулы СНзЬ. где принимает указанные значения. можно получить соединения формулы 1. Если а реакционную смесь добавить водородную кислоту. в этом случае получают соединения формулы . где КБ представляет водород. Или же из реакционной смеси могут быть выделены соединения формулы . в которыхны в соединения формулы Е. в которых На представляет водород. обработкой реагентом формулы СНЫ где . принимает выше указанные значения. Соединения фрмулы Н. в которых На представляет водород. могут(таким как карбонат калия) и реагентом формулы СН 3.Или же соединения формулы могут быть получения из ацетапей формулы Шудалением метанола в кислотных или щелочных условиях. Примеры реагентов или смесей реагентов. которые могут быть использованы для такого превращения. включают дииэопропиламид лития. кислый сульфат калияработе ссылки) и тризтипамин часто в присутствии кислоты Льюиса. такой четыреххлористый титан (см. например. К. Мэипоа. 1 Негры. ..Спегп 5 ос Спетаса Соттпитсаиопз. 1985. 1000).Ацетали формулы Ш могут быть получены обработкой ацеталей метилсилилкетана формулы у. где В представляет алкил, триметилортоформатом в присутствии кислотыЛьюиса. такой как четыреххлористый титанТ.Маауагла. Спегтзтгу Ьепегв. 1976. 769). Ацетали метипсилипкетена формулы /могут быть получены из фенилацетатов фор мулы П обработкой основанием и тралкил силилгелоидом формулы 8353 СЕ или Н 351 Вг. таким триметилсилилхлорид. или основанием (таким как триэтиламин) и триалкилсилилтрифлатом формулы К 35 Е-О 5 О 2 СР 3 (смНе всегда необходимо выделять промежуточные соединения формулы / и /, в соответствующих условиях соединения формулы Гмогут быть получены из фенилацетатов формулы Н реакций в одном сосуде последовательным вышеперечисленных реагентов. АИли же соединения формулы (1) могут быть получены обработкой кетоэфиров формулы / метоксиметиленирующим реагентом. . например, метоксиметилентрифенилфосфораном (см например. шдтеонсп. Ббспгатт, Т.Апе, Р.Ооегшп 1 ег Европейский патент Н 0044448317. 1980).Кетозфиры формулы / могут быть получены описанными в литературе способами. Особенно полезные способы включают (1) реакцию соответствующего фенилмагнийгалоида ИЛИ производного фен иллития с диметилоксалатом по методике. описанной(Н) окисление фенилацетатов формулы ш двуокисью селена. как правило. в отсутствии растворителя и при температуре выше 10 ОС окисление эфиров миндалевой кислоты использованием. к примеру. двуОКИСИ марганца В СООТВЕТСТВУЮЩЕМ ПВСТВО ритепе.Фенилацетаты формулы Ш и соответствующие фенилуксусные кислоты формулы Ш могут быть также синтезированы разнообразными другими описанными в литературе способами. Например. несколько приемлемых методов описано О.С.Аткпзоп. К.Е. (Зоотгеу. Р.1.Меуег.М.С. Рп 111 р 5.М.д. Битлов. А.Р. учеъьошп. ЦААНео. Слепи 1983. 26. 1361 и В.С.А(Епзоп, К.Е. Соотгеу. В. Маек, д.15. Зет/те. МЛ. Бтйшпоз. ьмев. Слет. 1983. 26.1353. кроме того. большинство способов. приведенных в работе .1 Р Шел. А. Воиспегге. Н.Соизе. Смоишп. Тетга Ьеогоп. 1986. 42. 4095. для синтеза эфиров З-арилпропионовых кислот и самих кислот также применимы для получения фенилацетатом формулы Ш и фенилуксусных кислот использованием соответствующих предшественников. в которых ортозамеЩЕННЫЙ ФЕНОКСИЗЭМЕСТИТЕЛЬ И ЗЭМВСТИТЕПЬ
МПК / Метки
МПК: C07C 69/734
Метки: кислоты, или, пропеновой, стереоизомеры, производные
Код ссылки
<a href="https://by.patents.su/30-1554-proizvodnye-propenovojj-kisloty-ili-ih-stereoizomery.html" rel="bookmark" title="База патентов Беларуси">Производные пропеновой кислоты или их стереоизомеры</a>
Предыдущий патент: Твердый катализатор, способ его получения и способ получения полипропилена
Следующий патент: Производные акриловой кислоты
Случайный патент: Устройство для выявления флюоресценции материала для пломбирования и протезирования зубов