Способ определения наличия остаточных опухолевых клеток при лечении Common-В (CD10+) или Пре-В (СD10+) субтипов острого лимфобластного лейкоза у ребенка
Номер патента: 18696
Опубликовано: 30.10.2014
Авторы: Шман Татьяна Викторовна, Белевцев Михаил Владимирович, Мовчан Людмила Викторовна, Савва Наталья Николаевна
Текст
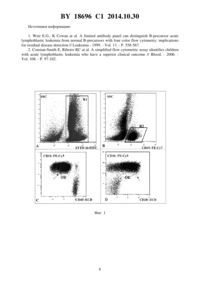
(51) МПК НАЦИОНАЛЬНЫЙ ЦЕНТР ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ СПОСОБ ОПРЕДЕЛЕНИЯ НАЛИЧИЯ ОСТАТОЧНЫХ ОПУХОЛЕВЫХ КЛЕТОК ПРИ ЛЕЧЕНИИ -В (10) ИЛИ ПРЕ-В (С 10) СУБТИПОВ ОСТРОГО ЛИМФОБЛАСТНОГО ЛЕЙКОЗА У РЕБЕНКА(71) Заявитель Государственное учреждение Республиканский научнопрактический центр детской онкологии, гематологии и иммунологии(72) Авторы Мовчан Людмила Викторовна Белевцев Михаил Владимирович Шман Татьяна Викторовна Савва Наталья Николаевна(73) Патентообладатель Государственное учреждение Республиканский научно-практический центр детской онкологии, гематологии и иммунологии(56) ВИЛЬЧЕВСКАЯ Е.В. и др. Современная педиатрия. - 2009. - Т. 1. -23. С. 151-157. ПОПОВ А.М. и др. Иммунология. 2010. -2. - С. 60-64. Оценка эффективности лечения лимфолейкозов с использованием иммунофенотипического и молекулярно-генетического методов. Инструкция по применению. - Минск, 2006. - С. 1-20.(57) Способ определения наличия остаточных опухолевых клеток при лечении (10) или Пре-В (10) субтипов острого лимфобластного лейкоза у ребенка, заключающийся в том, что на 15-й и 36-й дни индукционной терапии берут образец костного мозга пациента, идентифицируют в нем методом проточной цитофлуориметрии среди всех жизнеспособных ядросодержащих клеток клетки с лейкоз-ассоциированным иммунофенотипом для каждого из субтипов с использованием панели моноклональных антител,включающей следующие комбинации иммунофенотипических маркеров, конъюгированных с флуоресцентными метками 16 /20 /45 /10 -5/19/45 /10 -5/19 -7, 16 /11 /45 /10 5/19 -7 и 16 /38 /45 /10 -5/19 -7, определяют процентное содержание клеток с лейкоз-ассоциированным иммунофенотипом в образце и при получении значения не менее 0,01 судят о наличии остаточных опухолевых клеток. 18696 1 2014.10.30 Изобретение относится к медицине, к иммунологии и гематологии, а именно к способу оценки эффективности противоопухолевой терапии у детей с острым лимфобластным лейкозом из предшественников В-лимфоцитов (ВП ОЛЛ) при - и Пре-В(10 ВП ОЛЛ) субтипах. Динамика количества опухолевых клеток в костном мозге (КМ) во время индукционной терапии является важной информацией, отражающей ответ на терапию и риск возникновения рецидива во время лечения острого лимфобластного лейкоза у детей. В настоящее время исследования, проводимые для оценки прогностических факторов возникновения рецидивов при острых лейкозах, показывают, что достижение цитоморфологической ремиссии (менее 5 бластных клеток в костном мозге) на этапах терапии не является абсолютным критерием прогноза в отношении рецидива заболевания. Это связано с тем, что пациенты с ОЛЛ, находясь в гематологической ремиссии после терапии, могут сохранять в костном мозге до 1010 опухолевых клеток (остаточные опухолевые клетки ООК), обнаружение которых возможно с использованием более чувствительных и специфичных способов. К современным способам оценки уровня ООК относится способ полимеразной цепной реакции (определение химерных онкогенов и/или реаранжировок генов иммуноглобулинов и Т-клеточного рецептора) и определение аберрантных иммунофенотипических характеристик опухолевых клеток с использованием проточной цитофлуориметрии (ПЦ). Мониторинг ООК с использованием техники многопараметрической проточной цитометрии является перспективным и наиболее предпочтительным способом оценки эффективности терапии, а также прогнозирования рецидивов на ранних этапах терапии детей с ОЛЛ. Данный способ основан на выявлении лейкоз-ассоциированного иммунофенотипа(ЛАИФ) опухолевых клеток на момент постановки диагноза и идентификации его в ходе терапии среди нормальных гемопоэтических клеток КМ. Критерием позитивности содержания ООК в образце является наличие группы клеток с ЛАИФ в количестве 0,01 . Таким образом, количество и комбинации используемых для детекции остаточных опухолевых клеток моноклональных антител (МКА) являются важными факторами для адекватного анализа. Известен способ оценки остаточных опухолевых клеток с помощью ПЦ с использованием ограниченной панели МКА. Уровень остаточных опухолевых клеток в образцах КМ пациентов с ОЛЛ из предшественников В-лимфоцитов определяли с применением 19/45-/20-/10- или 19-/45-/9-/34 комбинаций МКА. Также полученные результаты анализировали с использованием шаблона заданных регионов, полученных в результате иммунофенотипического исследования нормальных предшественников (гематогонов) 1. Недостатком способа является то, что данный подход не применим в случаях низкого содержания остаточных опухолевых клеток в образце КМ среди нормальных предшественников В-лимфоцитов. Также анализ ООК с использованием ограниченного числа маркеров и применение шаблона регионов способствуют получению ложноотрицательных результатов в случаях иммунологической модуляции, которая может происходить на ранних этапах индукционной терапии. Также известен способ оценки остаточных опухолевых клеток у пациентов с ОЛЛ из предшественников -лимфоцитов, основанный на детекции только маркеров 19, 10,34. Экспрессию данных маркеров оценивают на момент диагностики, а также на ранних этапах химиотерапии 2. Недостатком является то, что этот упрощенный способ имеет также множество ограничений. Данный подход может способствовать получению ложноотрицательных результатов в случаях изменения экспрессии антигенов 10 и 34 под действием глюкокортикоидов, используемых в индукционной терапии, или же ложноположительных результатов в случаях неспецифического связывания МКА и регенерации КМ, которая может наблюдаться уже к окончанию индукции ремиссии. 2 18696 1 2014.10.30 Проведенное патентно-информационное исследование позволяет сделать вывод о том,что идентичных многоцветных комбинаций МКА для оценки ООК на ранних этапах терапии ВП ОЛЛ у детей не обнаружено. Задача предлагаемого изобретения состоит в том, чтобы провести оценку динамики остаточных опухолевых клеток на ранних этапах интенсивной химиотерапии у детей с- и Пре- (10 ВП ОЛЛ) иммунологическими типами ВП ОЛЛ с использованием техники многопараметрической проточной цитометрии. Поставленную задачу решают путем разработки оптимальной панели многоцветных комбинаций моноклональных антител на основе ЛАИФ опухолевых клеток прии Пре- (10 ВП ОЛЛ) субтипах ВП ОЛЛ у детей. Способ осуществляют следующим образом. По данным исследований, проведенных в ГУ РНПЦДОГ, в структуре ОЛЛ у детей 88 занимают лейкозы из предшественников -лимфоцитов. Согласно иммунофенотипической классификации и экспрессии лейкемическими клетками линейно-специфичных и дифференциально-диагностических маркеров, ВП ОЛЛ подразделяются на следующие иммунологические варианты (таблица). Иммунологические варианты ВП ОЛЛ Иммунологические варианты ВП ОЛЛ Про- ОЛЛ Комбинация дифференциальнодиагностических маркеров 19/22/79, ,10-, 34/-,ц/п 19/22/79,10, 34/-,ц/п 19/22/79, ,10, 34/-,ц, п Доля ОЛЛ с характерным иммунофенотипом диагностированных в ГУ РНПЦДОГ с 2005 г. по март 2011 г.251 8,8 После диагностического иммунофенотипирования при - и Пре(10 ВП ОЛЛ) субтипах ВП ОЛЛ проводят идентификацию индивидуального ЛАИФ для дальнейшего мониторинга остаточных опухолевых клеток на этапах индукционной терапии (15-й и 36-й дни). Для исследования используют цельный костный мозг (КМ) костный мозг набирают в пробирку, содержащую антикоагулянт (калий ЭДТА) в объеме от 2,5 до 5,0 мл. В течение не более 2-3-х часов образец КМ доставляют в лабораторию и обрабатывают. По 100300 мкл цельного костного мозга (в зависимости от объема и клеточности образца) помещают в сухие пробирки и добавляют моноклональные антитела, согласно представленной панели в количестве, указанном в инструкции по применению фирмы-производителя. В панель для следования входят комбинации МКА, конъюгированных с флуоресцентными метками , , , -5 и -7 6 /20 /45 /10 -5/19 -7 6 /58 /45 /10 -5/19 -7 6 /34 /45 /10 -5/19 -7 6 / /45 /10 -5/19 -7 6 /38 /45 /10 -5/19 -7. Далее образцы тщательно перемешивают и инкубируют в темноте при комнатной температуре в течение 20 мин (согласно инструкции по применению фирмы-произво 3 18696 1 2014.10.30 дителя). После инкубации проводят лизирование эритроцитов на автоматической станциис использованием оригинальных растворов для лизирования и фиксации. Учет и анализ результатов проводят на проточном цитофлуориметре 500 () в программе СХР. Для анализа ЛАИФ учитывают не менее 50 тыс., а для мониторинга остаточных опухолевых клеток не менее 500 тыс. жизнеспособных, ядросодержащих клеток. Результат выражают как процентное содержание ООК среди всех жизнеспособных, ядросодержащих клеток. Способ иллюстрируется следующими фигурами. На фиг. 1 показан пример выделения регионов, необходимых для определения ЛАИФ и оценки ООК, где исходный регион (1) устанавливают на точечном графике 16/ для учета всех жизнеспособных, ядросодержащих клеток (фиг. 1 А). Далее, на графике 19/ устанавливают второй регион (2), который выполняет заданный критерий 1 и включает все 19 клетки (фиг. 1 В). Последующие графики, отражающие различные комбинации МКА согласно панели, выполняют заданный критерий 2. На данных графиках по аберрантной экспрессии МКА проводят анализ и подсчет клеток с ЛАИФ (фиг. 1, 1). На фиг. 2 представлен пример определения индивидуального ЛАИФ опухолевых клеток с использованием разработанной панели МКА при - ОЛЛ и Пре-В ОЛЛ(10 ВП ОЛЛ). У данного пациента Г. с диагнозом - ОЛЛ опухолевые клетки характеризуются высокой экспрессией маркера 10, сниженной экспрессией 45,58 и 38, отсутствием экспрессии маркеров 20 и 11 а, а также гетерогенной экспрессией 34. Пример оценки уровня ООК у пациента Г. на 15-й день противоопухолевой терапии показан на фиг. 3. На основании вышеописанной характеристики ЛАИФ, а также с учетом возможности изменения уровня экспрессии иммунофенотипических маркеров под действием глюкокортикоидов, применяемых в ходе индукционной терапии, идентифицируют опухолевые клетки среди нормальных гемопоэтических клеток КМ и проводят их количественный подсчет. У данного пациента уровень ООК на 15-й день терапии составляет 0,27 . На фиг. 4 проиллюстрирован пример оценки ООК у пациента Г. на 36-й день противоопухолевой терапии. На основании вышеописанной характеристики ЛАИФ, а также с учетом изменения уровня экспрессии иммунофенотипических маркеров идентифицируют опухолевые клетки среди нормальных гемопоэтических клеток КМ и проводят их количественный подсчет. У данного пациента уровень ООК на 36-й день терапии составляет 0,01 , таким образом, результат считается отрицательным. На фиг. 5 представлен другой пример определения индивидуального ЛАИФ опухолевых клеток с использованием разработанной панели МКА при - ОЛЛ и ПреОЛЛ (10 ВП ОЛЛ). ЛАИФ пациента Ш. с диагнозом Пре-В ОЛЛ характеризуется высокой экспрессией антигена 10, 34, сниженной экспрессией 58, 38 и полным отсутствием экспрессии маркеров 20 и 11 а. На фиг. 6 представлен пример оценки уровня ООК в КМ пациента Ш. на 15-й день индукционной терапии. Учитывая вышеописанную характеристику ЛАИФ, а также возможность изменения уровня экспрессии иммунофенотипических маркеров под действием глюкокортикоидов, идентифицируют опухолевые клетки среди нормальных гемопоэтических клеток КМ и проводят их количественный подсчет. У данного пациента уровень ООК на 15-й день терапии составляет 0,95 . На фиг. 7 продемонстрирована оценка МОБ пациента Ш. на 36-й день противоопухолевой терапии. С учетом определенного ЛАИФ лейкемических клеток, а также возможности изменения уровня экспрессии иммунофенотипических маркеров в ходе лечения идентифицируют опухолевые клетки среди нормальных гемопоэтических клеток КМ и проводят их количественный подсчет. У пациента Ш. уровень ООК на 36-й день терапии составляет 0,06(результат считается положительным). 4 18696 1 2014.10.30 С использованием вышеописанных комбинаций МКА исследованы образцы костного мозга 96 пациентов с ВП ОЛЛ (88 - - ОЛЛ и 8 - Пре- ОЛЛ). В результате проведенного исследования, остаточные опухолевые клетки выявлены у 76 на 15-й день и 41 на 36-й день интенсивной химиотерапии. У остальных пациентов остаточные опухолевые клетки не выявлены в данные сроки наблюдений. Преимуществом предлагаемого способа оценки остаточных опухолевых клеток по сравнению с известными и уже существующими способами является то, что применение разработанной многоцветной комбинации моноклональных антител позволяет с высокой специфичностью и чувствительностью идентифицировать опухолевые клетки среди нормальных гемопоэтических клеток-предшественников в образцах КМ пациентов с - ОЛЛ и Пре- ОЛЛ (10 ВП ОЛЛ) субтипами ВП ОЛЛ. Отличительные признаки нашего изобретения заключаются в том, что применение разработанной комбинаций МКА для оценки ООК способствует получению достоверных результатов в случаях изменения уровня экспрессии значимых для определения ООК иммунофенотипических маркеров неспецифического связывания МКА регенерации КМ на момент окончания индукционной терапии (36-й день исследования). Клинические примеры, иллюстрирующие данный способ диагностики. Пример 1. Пациентка Г., 2008 года рождения, поступила в ГУ РНПЦДОГ 26.07.2010 года,где на основании иммунофенотипической диагностики КМ поставлен диагноз - ОЛЛ. В ходе цитогенетических и молекулярно-биологических исследований патологических генетических изменений не выявлено. Пациентка стратифицирована по стандартной группе риска и получала лечение по протоколу 2008. С использованием разработанной панели МКА при - ОЛЛ и Пре-В ОЛЛ (10 ВП ОЛЛ) методом многопараметрической проточной цитометрии проведено определение ЛАИФ и оценка динамики ООК на ранних этапах противоопухолевой терапии (фиг. 2-4). В результате проведенного исследования уровень ООК в КМ пациентки на 15-й день лечения составлял 0,27 , на 36-й день ООК не выявлены (ООК 0,01 ), по данным цитоморфологического исследования на 36-й день терапии наблюдалась гематологическая ремиссия. Исход пациентка жива и находится в клинико-гематологической ремиссии. Пример 2. Пациент Ш., 1994 года рождения, поступил в ГУ РНПЦДОГ 8.04.2005 года, где на основании иммунофенотипической диагностики КМ поставлен диагноз Пре-В ОЛЛ. В ходе цитогенетических и молекулярно-биологических исследований патологических генетических изменений не выявлено. Пациент стратифицирован по стандартной группе риска и получал лечение по протоколу 2008. С использованием разработанной панели МКА методом многопараметрической проточной цитометрии проведено определение ЛАИФ и оценка динамики ООК на ранних этапах противоопухолевой терапии (фиг. 5-7). В результате проведенного исследования уровень ООК в КМ пациента на 15-й день лечения составлял 0,95 , на 36-й день - 0,06 , тогда как по данным цитоморфологического исследования на 36-й день терапии больной находился в гематологической ремиссии. Исход 3.09.2006 диагностирован изолированный костномозговой рецидив заболевания. Таким образом, предлагаемый способ является быстрым, информативным, надежным,позволяет с высокой степенью специфичности проводить оценку уровня ООК в образцах КМ пациентов с - и Пре- (10 ВП ОЛЛ) иммунологическими вариантами ВП ОЛЛ. Полученные результаты позволяют идентифицировать пациентов с высоким риском развития рецидива от тех больных, которые могут оставаться в полной ремиссии,проводить дополнительную стратификацию пациентов на ранних этапах противоопухолевой терапии с целью ее усиления для элиминации остаточного опухолевого клона и предотвращения развития рецидива или ослабления для снижения побочных эффектов. Представленный способ может быть рекомендован для использования в медицинских учреждениях Министерства здравоохранения Республики Беларусь. 5 Национальный центр интеллектуальной собственности. 220034, г. Минск, ул. Козлова, 20. 12
МПК / Метки
МПК: G01N 33/533
Метки: остаточных, сd10+, common-в, определения, способ, острого, лейкоза, лечении, наличия, клеток, лимфобластного, cd10+, пре-в, субтипов, опухолевых, или, ребенка
Код ссылки
<a href="https://by.patents.su/12-18696-sposob-opredeleniya-nalichiya-ostatochnyh-opuholevyh-kletok-pri-lechenii-common-v-cd10-ili-pre-v-sd10-subtipov-ostrogo-limfoblastnogo-lejjkoza-u-rebenka.html" rel="bookmark" title="База патентов Беларуси">Способ определения наличия остаточных опухолевых клеток при лечении Common-В (CD10+) или Пре-В (СD10+) субтипов острого лимфобластного лейкоза у ребенка</a>
Предыдущий патент: Способ модифицирования сплавов
Следующий патент: Способ охлаждения многослойного ограждения здания
Случайный патент: Гербицидная композиция