Фармацевтическая композиция с антиоксидантным и ноотропным действием
Номер патента: 15604
Опубликовано: 30.04.2012
Авторы: Романовский Дмитрий Иосифович, Кравченко Елена Валериевна, Петров Петр Тимофеевич, Жебракова Ирина Вениаминовна
Текст
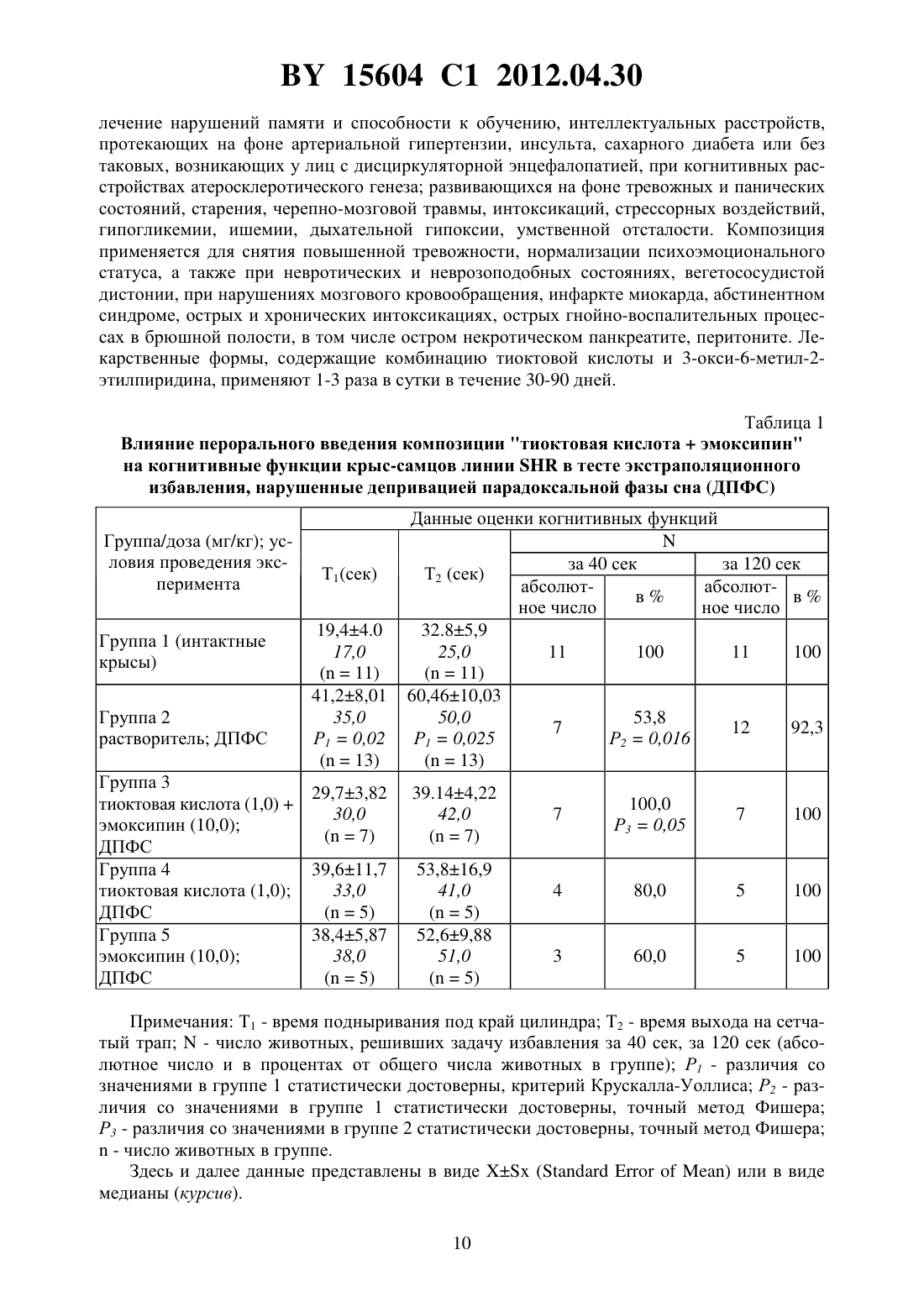
(51) МПК НАЦИОНАЛЬНЫЙ ЦЕНТР ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ(71) Заявитель Государственное учреждение Научно-производственный центр Институт фармакологии и биохимии Национальной академии наук Беларуси(72) Авторы Романовский Дмитрий Иосифович Кравченко Елена Валериевна Петров Петр Тимофеевич Жебракова Ирина Вениаминовна(73) Патентообладатель Государственное учреждение Научно-производственный центр Институт фармакологии и биохимии Национальной академии наук Беларуси(56)5990152 , 1999. ДЮМАЕВ К.М. и др. Антиоксиданты в профилактике и терапии патологий ЦНС. - М. Институт биомедицинской химии РАМН, 1995. - С. 145-151. ВАЛЧЕГОРСКИЙ И.А. и др. Клиническая медицина. - 2008. - Т. 86. -10. С. 52-59.2324479 2, 2008.(57) 1. Фармацевтическая композиция с антиоксидантным и ноотропным действием, содержащая тиоктовую кислоту и фармацевтически приемлемую соль 3-окси-6-метил-2 этилпиридина в эффективном количестве, а также фармацевтически приемлемые вспомогательные вещества. 2. Фармацевтическая композиция по п. 1, отличающаяся тем, что содержит 3-окси-6 метил-2-этилпиридина гидрохлорид, 3-окси-6-метил-2-этилпиридина сукцинат или 3-окси 6-метил-2-этилпиридина фумарат. 3. Фармацевтическая композиция по п. 1, отличающаяся тем, что предназначена для приема внутрь и выполнена в форме таблетки, капсулы, гранул или порошка. 4. Фармацевтическая композиция по п. 2 или 3, отличающаяся тем, что выполнена в форме таблетки, покрытой оболочкой, и имеет следующий состав, г тиоктовая кислота 0,0001 - 1,0 3-окси-6-метил-2-этилпиридина гидрохлорид 0,0001 - 1,0 янтарная кислота 0,0001 - 1,0 целлюлоза микрокристаллическая 0,015 - 0,450 лактоза 0,010 - 0,500 крахмал 0,010 - 0,450 поливинилпирролидон 0,004 - 0,200 магния стеарат 0,0005 - 0,03 метилцеллюлоза 0,00001 - 0,10 твин-80 0,00001 - 0,008. 15604 1 2012.04.30 5. Фармацевтическая композиция по п. 2 или 3, отличающаяся тем, что выполнена форме твердой желатиновой капсулы, содержащей гранулы следующего состава, г тиоктовая кислота 0,0001 - 1,0 3-окси-6-метил-2-этилпиридина сукцинат 0,0001 - 1,0 целлюлоза микрокристаллическая 0,015 - 0,450 лактоза 0,010 - 0,500 крахмал 0,010 - 0,450 поливинилпирролидон 0,004 - 0,220 магния стеарат 0,0005 - 0,030. 6. Фармацевтическая композиция по п. 2 или 3, отличающаяся тем, что выполнена форме мягкой желатиновой капсулы с содержимым следующего состава, г тиоктовая кислота 0,0001 - 1,0 3-окси-6-метил-2-этилпиридина сукцинат 0,0001 - 1,0 масло растительное 0,001 - 1,0 лецитин очищенный 0,001 - 1,0 воск пчелиный 0,001 - 1,0. 7. Фармацевтическая композиция по п. 2 или 3, отличающаяся тем, что выполнена форме гранул для приема внутрь и имеет следующий состав, г тиоктовая кислота 0,0001 - 3,0 3-окси-6-метил-2-этилпиридина гидрохлорид 0,0001 - 3,0 янтарная кислота 0,0001 - 3,0 целлюлоза микрокристаллическая 0,015 - 0,450 лактоза 0,010 - 1,500 крахмал 0,010 - 0,500 поливинилпирролидон 0,004 - 0,200 магния стеарат 0,0005 - 0,030. 8. Фармацевтическая композиция по п. 2 или 3, отличающаяся тем, что выполнена форме порошка для приема внутрь и имеет следующий состав, г тиоктовая кислота 0,0001 - 3,0 3-окси-6-метил-2-этилпиридина фумарат 0,0001 - 1,0 янтарная кислота 0,0001 - 15,0 сахар-песок 0,001 - 15,0. Изобретение относится к области медицины (фармакологии, психиатрии) и фармацевтической промышленности и может быть использовано для коррекции патологических сдвигов, обусловленных оксидантным стрессом, а также для повышения умственных способностей, профилактики и терапии нарушений высших психических функций у человека. Антиоксиданты выполняют функцию защиты живого организма против токсического действия молекулярного кислорода и свободных радикалов, тормозят перекисное окисление липидов, являются необходимыми компонентами всех тканей и клеток человеческого организма, предохраняя биологические субстраты от самопроизвольного окисления. В многочисленных исследованиях подтверждены высокая биологическая активность и широкие терапевтические возможности антиоксидантов. Ряд соединений с антиоксидантной активностью обладают ноотропными свойствами, то есть улучшают когнитивные функции, стимулируют обучение, память и умственную деятельность, повышают устойчивость мозга к повреждающим факторам. К числу таких соединений в последние годы относят тиоктовую (альфа-липоевую) кислоту. Уникальные физико-химические свойства тиоктовой кислоты позволяют ей участвовать в ряде важных биохимических реакций, в том числе в окислительно-восстановительных процессах цикла трикарбоновых кислот (цикл Кребса) в качестве кофермента,2 15604 1 2012.04.30 оптимизируя реакции окислительного фосфорилирования 1. Как известно, свободные радикалы (супероксид анион 2-, гидроксильный радикал - и др.) оказывают выраженное токсическое воздействие на различные ткани. В эксперименте отмечено защитное действие тиоктовой кислоты на клеточном уровне при перекисном окислении липидов 1. Улучшение когнитивных функций при применении тиоктовой кислоты отмечено как у лабораторных животных при моделировании болезни Альцгеймера 2, так и у человека(замедление снижения когнитивных функций у пациентов с болезнью Альцгеймера) 3. При этом в эксперименте на крысах среди испытанных доз тиоктовой кислоты 50, 100 и 200 мг/кг (перорально) статистически значимое улучшение выявлено лишь при применении дозы 200 мг/кг 2. Тиоктовая кислота играет важную роль при сахарном диабете - патологии, сопровождающейся когнитивными нарушениями. Это соединение оказывает влияние на утилизацию углеводов и осуществление нормального энергетического обмена, улучшая энергетический статус клетки. Тиоктовая кислота непосредственно влияет на фазы кетогенеза и глюкогенеза, способствуя утилизации и окислению глюкозы, улучшая энергетические параметры, является биокатализатором энергетического обмена, положительно влияет на аксональный транспорт и нормализует анормальное поступление глюкозы к нерву, облегчает превращение молочной кислоты в пировиноградную с последующим ее декарбоксилированием, т.е. способствует ликвидации метаболического ацидоза, обладает положительным липотропным действием. Тиоктовая кислота не только обладает самостоятельным антиоксидантным потенциалом, но и может взаимодействовать с комплексом других антиоксидантов, поддерживая как липидный, так и водный антиоксидантный статус на физиологическом уровне 1. Она обеспечивает мощную поддержку работы других антиоксидантных звеньев в организме(ферменты, металлосвязывающие белки, молекулы - уборщики свободных радикалов). При патологических процессах, сопровождающихся оксидантным стрессом, нарушается организация и физико-химические характеристики биомембран, меняется конформация и способность мембранных рецепторов связывать биологически активные вещества. Для тиоктовой кислоты не установлена способность улучшать структуру и функциональную активность мембраны клеток. С учетом этого целесообразно комбинировать тиоктовую кислоту с другими антиоксидантами, обладающими мембранотропной активностью. Известен ряд лекарственных средств на основе тиоктовой кислоты, применяемых при коронарном атеросклерозе, заболеваниях печени (болезнь Боткина, цирроз печени), полинейропатии (диабетической, алкогольной), отравлениях солями тяжелых металлов и других интоксикациях, среди них - Тиогамма, Тиоктацид БВ, Эспа-липон, Берлитион и др. 4. С целью повышения биодоступности тиоктовой кислоты предложена фармацевтическая композиция, содержащая тиоктовую кислоту или ее фармацевтически приемлемые соли (прототип) 5. Применение этой запатентованной композиции позволяет обеспечить более полное поступление неизмененной субстанции тиоктовой кислоты в кровь пациента 5. Вместе с тем использование таких солей тиоктовой кислоты не ведет к появлению качественно новых лечебных свойств. Отсутствуют данные исследований на животных или клинические данные, подтверждающие выраженное усиление эффективности прототипа в сравнении с известными средствами на основе тиоктовой кислоты. Прототип не обеспечивает мембранотропного действия. Описаны антиоксидантные лекарственные средства на основе производных 3-окси-6 метил-2-этилпиридина (эмоксипин, мексидол) обладающие способностью эффективно ингибировать свободно-радикальное окисление липидов биомембран, оказывать ноотропное действие, улучшать биоэнергетические процессы в экстремальных условиях, а также характеризующиеся мембраномодулирующими эффектами, приводящими к стабилизации биомембран, улучшению их структурно-функциональных характеристик 6. Мембранотропное действие производных 3-окси-6-метил-2-этилпиридина особенно важно с учетом 3 15604 1 2012.04.30 того, что большинство биохимических процессов, протекающих в организме, в той или иной степени регулируются системой клеточных мембран. Эмоксипин (3-окси-6-метил-2-этилпиридина гидрохлорид 7, 6-метилил-2-этилпиридин-3-ола гидрохлорид, 3-окси-6-метил-2-этилпиридина гидрохлорид, этилметилпиридинола гидрохлорид 4) выпускается в виде глазных капель, а также в виде инъекционных лекарственных форм (в том числе эмоксипин, раствор для инъекций 14, 7 и 37,раствор для инфузий 0,5. Эмоксипин обладает антиоксидантными и ноотропными свойствами. Применяется в офтальмологии, а также - при лечении заболеваний других органов и систем организма, сопровождающихся усилением перекисного окисления липидов и гипоксией (инфаркт миокарда, нестабильная стенокардия, острые и хронические нарушения мозгового кровообращения (в том числе при черепно-мозговой травме), кожные заболевания и др.). Эмоксипин эффективен в эксперименте на крысах с черепно-мозговой травмой в дозе 25 мг/кг 8. Вместе с тем эмоксипин не принимает участия в окислительновосстановительных процессах цикла трикарбоновых кислот (цикл Кребса) и ряде других биохимических процессов, в которых задействована тиоктовая кислота, что ограничивает спектр терапевтического действия лекарственных средств на основе эмоксипина в сравнении с заявляемой композицией. Мексидол (3-окси-6-метил-2-этилпиридина сукцинат 7, 2-этил-6-метил-3-гидроксипиридина сукцинат 6, этилметилгидроксипиридина сукцинат 4), как и заявляемая композиция, характеризуется антиоксидантными и ноотропными свойствами, улучшает когнитивные функции - в дозе 100 мг/кг оказывает антиамнестическое действие, в том числе при амнезии у крыс, вызванной депривацией парадоксальной фазы сна (ДПФС) 6. Однако мексидол не обладает гаммой биохимических эффектов, которые присущи тиоктовой кислоте. В частности, у него отсутствует характерное для тиоктовой кислоты гипогликемическое действие, выраженное нормализующее влияние на утилизацию углеводов, обусловливающее коррекцию функционирования нервной системы при нарушениях углеводного обмена. Фумаровая кислота относится к числу легкодоступных источников и активаторов образования и сохранения энергии, особенно эффективна при экстренных ситуациях резкого нарушения обмена веществ, например при стрессах. Фармакологическая активность 3-окси-6-метил-2-этилпиридина фумарата не описана, лекарственные средства на его основе неизвестны. Учитывая, что тиоктовая кислота и соли 3-окси-6-метил-2-этилпиридина характеризуются разными механизмами фармакологического действия, при применении заявляемой композиции будет достигаться усиление антиоксидантной и ноотропной активности, что может обеспечить снижение действующих доз активных соединений при их совместном применении. Задача настоящего изобретения - установить новый эффект синергизма, заключающийся в усилении эффективности тиоктовой кислоты и соли 3-окси-6-метил-2-этилпиридина при их совместном применении, а также осуществить направленную разработку фармацевтической композиции с антиоксидантным и ноотропным действием, содержащей тиоктовую кислоту и фармацевтически приемлемую соль 3-окси-6-метил-2-этилпиридина в эффективном количестве, а также фармацевтически приемлемые вспомогательные вещества. Такая фармацевтическая композиция может применяться в качестве антиоксидантного и ноотропного средства - с целью повышения умственных способностей, профилактики и лечения нарушений памяти и способности к обучению, интеллектуальных расстройств, в том числе когнитивных нарушений при деменции легкой и умеренной степени выраженности на фоне артериальной гипертензии, инсульта, при диабетическом поражении центральной нервной системы (диабетическая энцефалопатия, инфаркты мозга и др.) и при иных патологических состояниях, вызывающих нарушения функционирования нервной 4 15604 1 2012.04.30 системы. Заявляемая композиция может применяться также для терапии многих других заболеваний, сопряженных с оксидантным стрессом. Ноотропные, антиоксидантные и иные полезные лечебно-профилактические свойства комбинации тиоктовой кислоты и соли 3-окси-6-метил-2-этилпиридина, как и содержащие их фармацевтические композиции, не описаны. Поставленная задача решается тем, что в направленных психофармакологических экспериментах по стандартным методикам выявлено ноотропное действие комбинации тиоктовой кислоты и соли 3-окси-6-метил-2-этилпиридина, разработана фармацевтическая композиция, включающая тиоктовую кислоту, соль 3-окси-6-метил-2-этилпиридина, а также фармацевтически приемлемые вспомогательные вещества. Техническим результатом, достигаемым при реализации изобретения, является выявление возможности использования такой композиции в качестве антиоксидантного и ноотропного средства, а также получение лекарственной формы, обеспечивающей точность дозирования и удобство применения. Фармацевтическая композиция содержит в качестве активных действующих веществ тиоктовую кислоту (как рацемат, так и -, -изомеры) в диапазоне доз 0,0001-3,0 г (предпочтительно 0,010-1,8 г) и соль 3-окси-6-метил-2-этилпиридина (предпочтительно гидрохлорид, сукцинат, фумарат), в диапазоне доз 0,0001-3,0 г (предпочтительно 0,010-1,0 г). Предпочтительно применение заявляемой композиции в виде пероральной или инъекционной лекарственной формы, поскольку при этих способах введения обеспечивается наибольшая точность дозирования активного вещества. К числу пероральных лекарственных форм заявляемой композиции могут относиться таблетки, капсулы (в том числе мягкие и твердые), порошки и гранулы для орального применения. При этом фармацевтическая композиция может содержать одно или несколько разрешенных к медицинскому применению вспомогательных веществ (целевых добавок), способных улучшить фармацевтические характеристики заявляемой композиции, из числа описанных в Государственной Фармакопее Республики Беларусь 9 или иных фармакопеях. К числу предпочтительных вспомогательных веществ относятся целлюлоза микрокристаллическая, лактоза (наиболее предпочтительно в виде моногидрата), крахмал, аэросил, поливинилпирролидон низкомолекулярный, магния стеарат, янтарная кислота, метилцеллюлоза, твин-80, масла растительные (подсолнечное, соевое, кукурузное и др.), лецитин, воск пчелиный, гидроксипропилцеллюлоза, метилгидроксипропилцеллюлоза (гипромеллоза), макрогол в количествах,требующихся для приготовления фармацевтической композиции такие количества хорошо известны специалистам в области фармации и составляют для таблеток, твердых и мягких желатиновых капсул - 0,00001-1,0 г, гранул для приема внутрь - 0,0005-1,5 г, для порошка для приема внутрь - 0,0001-15,0 г. Заявляемая композиция отличается от прототипа 5 тем, что дополнительно содержит высокоэффективный антиоксидант с мембранотропными свойствами - соль 3-окси-6 метил-2-этилпиридина. В отличие от эмоксипина и мексидола, в состав заявляемой композиции входит тиоктовая кислота, что обеспечивает более широкий спектр лечебного действия. В отличие от эмоксипина, заявляемая композиция применима в виде пероральной лекарственной формы. Пример 1. Эффективность заявляемой комбинации, а также эмоксипина или липоевой кислоты изучали при пероральном введении в условиях моделирования расстройств адаптивного поведения и способности к экстраполяции, вызванных депривацией парадоксальной фазы сна (ДПФС) у половозрелых спонтанно гипертензивных крыс-самцов линии. Адаптивное поведение крыс исследовали с помощью теста экстраполяционного избавления (ТЭИ) 10. Крысу помещают в цилиндр, погруженный вертикально в воду на глубину 1-2,5 см. Задача животного состоит в том, чтобы найти выход из стрессирующей 5 15604 1 2012.04.30 ситуации - поднырнуть под нижний край цилиндра и выбраться на сетчатый трап, прикрепленный у внутреннего края бассейна. Ноотропные средства, в том числе антиоксиданты натрия и лития оксибутират ускоряют реакцию избавления от стресс-ситуации 10. При проведении эксперимента на протяжении 120 сек регистрировали значения показателей, характеризующих когнитивные функции время подныривания под край цилиндра (Т 1), время выхода на сетчатый трап (Т 2), число животных, решивших задачу избавления за 40 сек, за 120 сек. Формировали 5 групп животных. При этом особям группы 1 вводили плацебо и не применяли депривацию парадоксальной фазы сна, крысам группы 2 осуществляли ДПФС на фоне введения растворителя (здесь и далее - дистиллированная вода), животным группы 3 применяли одновременно эмоксипин (10,0 мг/кг) и липоевую кислоту (1,0 мг/кг), а крысам группы 4 - эмоксипин (10,0 мг/кг), крысам группы 5 - липоевую (тиоктовую) кислоту (1,0 мг/кг). Тестируемые образцы вводили непосредственно после депривации сна,за 45 мин до ТЭИ. Метод ДПФС, который заключается в помещении крыс на малые площадки, окруженные водой, был предложен. в 1964 году и используется как модель нарушений сна при невротических расстройствах различной тяжести. ДПФС проводили в бассейне с водой, в котором находятся площадки диаметром 6-6,5 см, выступающие на 2 см над уровнем воды. На таких площадках животные могут свободно сидеть. Во время бодрствования, дремоты и медленноволнового сна у крыс сохраняется напряжение мышц, что позволяет животным удерживаться на площадках. Во время парадоксальной фазы сна мышцы расслабляются и животные падают в воду, таким образом достигается избирательная депривация парадоксальной фазы сна (в среднем 85 ДПФС). В условиях этой модели в результате иммобилизации, изоляции, падений в воду и охлаждения у животного возникает сильный стресс, сопровождающийся дезадаптацией, нарушениями когнитивных функций, способности к экстраполяции. Все крысы группы 1, не подвергшиеся ДПФС, сумели менее чем за 40 сек поднырнуть под край цилиндра. Лишь 53,8 животных группы 2 (ДПФС, применение растворителя) сумели решить экспериментальную задачу за 40 сек (различия с интактным контролем статистически достоверны, Р 0,016, точный критерий Фишера) 7,7 крыс не сумели успешно осуществить подныривание даже за 120 сек. Среди крыс группы 3, получавших лечение заявляемой комбинацией, 100 животных сумели решить экстраполяционную задачу избавления за 40 сек, 100- за 120 сек (показатели идентичны таковым в группе 1 различия с животными, получавшими плацебо на фоне ДПФС, статистически значимы,Р 0,05, точный критерий Фишера) (табл. 1). В случае введения только эмоксипина или только тиоктовой кислоты имела место частичная компенсация различия с контролем (группа 1) по числу животных, сумевших решить экспериментальную задачу за 40 сек, были статистически незначимыми, однако не достигались статистически значимые различия с животными, подвергшимися ДПФС(группа 2). Это доказывает, что в случае введения комбинации достигается лучший результат, чем при введении активных компонентов по отдельности. Депривация сна ведет к статистически значимому увеличению у крыс группы 2 показателя Т 1 (Р 0,02, критерий Крускалла-Уоллиса) - на 21,8 сек в сравнении с интактным контролем. Кроме того, при этом отмечается резкое замедление принятия правильного решения при выходе на сетку (Р 0,025, критерий Крускалла-Уоллиса) - на 27,7 сек дольше, чем у крыс группы 1. В случае применения заявляемой комбинации, как и эмоксипина либо тиоктовой кислоты, статистически значимых различий с интактным контролем не отмечается, однако в первом случае зарегистрировано более быстрое решение задачи, чем во втором и в третьем случаях, соответственно (табл. 1). Приведенные данные подтверждают эффективность заявляемой комбинации при нарушениях высших интегративных функций мозга на фоне диссомнии (неспособности к 6 15604 1 2012.04.30 адаптивному поведению в стрессирующей ситуации и к экстраполяции). При этом достигается преимущество в сравнении с эмоксипином либо липоевой кислотой, вводимыми в тех же дозах, что и в заявляемой композиции. Пример 2. Изучали эффективность заявляемой комбинации при пероральном введении в условиях моделирования нарушений неассоциативного обучения (габитуация, ), вызванных ДПФС у половозрелых крыс-самцов линии. В норме у крыс привыкание к окружающей обстановке проявляется постепенным снижением двигательной активности в вертикальной плоскости (вертикальная двигательная активность, ВДА). При 2-й и последующих высадках в бокс актометра животные помнят,что уже находились в этой камере, и совершают меньше движений при повторных обследованиях установки (долговременная память габитуации). Это проявляется уменьшением ВДА. Крыс-самцов линииобеих групп адаптировали к камерам актометра(Италия), а затем 2-кратно проводили актометрию, помещая животных поодиночке в камеры на 15 мин интервал между 1-ми 2-м сеансами регистрации составлял 3 дня. При этом 2-й высадке предшествовал такой повреждающий фактор, как 24-часовая ДПФС. Сопоставляли показатели ВДА (выражаемой в условных единицах - усл. ед.) за 1-ю минуту наблюдения при первой и повторной актометрии. Формировали 2 группы животных. Крысам группы 1 (контрольная) применяли растворитель перорально, однократно, непосредственно после ДПФС (моделируемой, как описано в примере 1), за 60 мин до 2-го сеанса регистрации. Животным группы 2 вводили тестируемую комбинацию (тиоктовая кислота - 1,0 мг/кг, эмоксипин в дозе 10,0 мг/кг) при использовании того же режима введения. Вызванные ДПФС нарушения памяти у крыс-самцовконтрольной группы проявляются статистически достоверным возрастанием ВДА от 1-го ко 2-му сеансу актометрии, что связано с забыванием ранее приобретенной информации и вызванной этим необходимостью повторно обследовать камеру актометра. При первой высадке (без ДПФС) уровень ВДА составил 12,35,36 усл. ед., при повторной высадке (после ДПФС) 52,29,86 усл. ед., Р 0,05, критерий Уилкоксона (табл. 2). При использовании заявляемой комбинации статистически значимых изменений в сравнении с 1-м сеансом регистрации не отмечалось, повышение ВДА было менее выраженным, чем у крыс контрольной группы (табл. 2). Это подтверждает эффективность заявляемой комбинации при нарушениях неассоциативного обучения, вызванных ДПФС. Тиоктовая кислота и эмоксипин взяты в заведомо малых дозах (1,0 и 10,0 мг/кг), многократно более низких, чем описанные для каждого из них в отдельности (200,0 и 25,0 мг/кг соответственно) 2, 8. Пример 3. Пероральная лекарственная форма в виде таблеток тиоктовая кислота 0,2 г 3-окси-6-метил-2-этилпиридина гидрохлорид 0,125 г янтарная кислота 0,02 г целлюлоза микрокристаллическая 0,0983 г лактоза 0,20 г крахмал 0,04 г поливинилпирролидон 0,014 г магния стеарат 0,0027 г метилцеллюлоза 0,003 г твин-80 0,00005 г Таблетки, содержащие тиоктовую кислоту и соль 3-окси-6-метил-2-этилпиридина, могут быть получены из композиций данного изобретения любым подходящим способом получения таблеток (например, методом прямого прессования или путем таблетирования 7 15604 1 2012.04.30 с предварительным влажным или сухим гранулированием). Лекарственную форму в виде таблеток предпочтительно получать путем влажного гранулирования, что в последнем случае включает операции просеивание и смешивание порошков, увлажнение порошков раствором связывающих веществ и их перемешивание, гранулирование влажной массы,сушку влажных гранул, обработку сухих гранул, таблетирование, фасовку и упаковку. Берут 0,2 г тиоктовой кислоты, 0,125 г 3-окси-6-метил-2-этилпиридина гидрохлорида,0,02 г янтарной кислоты, 0,20 г лактозы, 0,07 г микрокристаллической целлюлозы, 0,04 г крахмала, просеивают, загружают в чистый сухой смеситель, перемешивают 10-15 минут и увлажняют при перемешивании 10 -ным раствором ранее просеянного поливинилпирролидона (0,014 г). Увлаженную смесь гранулируют, влажные гранулы раскладывают на лотки слоем 1,5-2 см и сушат (предпочтительно в сушилке с псевдоожиженным слоем). Предпочтительно осуществлять сушку при температуре 603 С в течение 10-12 ч, периодически помешивая, до остаточной влажности 3,00,5 . 0,0283 г микрокристаллической целлюлозы и 0,0027 г магния стеарата просеивают, добавляют к сухому грануляту и перемешивают в течение 10-15 мин. Прессуют полученную смесь для получения таблеток(например, с использованием пресса для формования таблеток). Ядро таблетки весит 700 мг и содержит 200 мг тиоктовой кислоты, 125 мг 3-окси-6-метил-2-этилпиридина гидрохлорида. Ядро таблетки покрывают оболочкой, для чего используют водный раствор метилцеллюлозы, содержащий метилцеллюлозу в количестве 0,003 г и твин-80 в количестве 0,00005 г. Пример 4. Пероральная лекарственная форма в виде твердых желатиновых капсул тиоктовая кислота 0,1 г 3-окси-6-метил-2-этилпиридина сукцинат 0,1 г целлюлоза микрокристаллическая 0,048 г лактоза 0,16 г крахмал 0,03 г поливинилпирролидон 0,01 г магния стеарат 0,002 г. Твердые желатиновые капсулы, содержащие тиоктовую кислоту и соль 3-окси-6 метил-2-этилпиридина, могут быть получены из композиций данного изобретения любым подходящим способом. Для лекарственной формы в виде твердых желатиновых капсул используют гранулят,получаемый аналогично способу, описанному в примере 3, при этом в качестве второго активного ингредиента используют 3-окси-6-метил-2-этилпиридина сукцинат. Полученный гранулят (0,45 г) с содержанием 100 мг тиоктовой кислоты, 100 мг 3-окси-6-метил-2 этилпиридина гидрохлорида капсулируют в твердые желатиновые капсулы. Пример 5. Пероральная лекарственная форма в виде мягких желатиновых капсул тиоктовая кислота 0,1 г 3-окси-6-метил-2-этилпиридина сукцинат 0,2 г масло растительное 0,15 г лецитин очищенный 0,05 г воск пчелиный 0,05 г. Мягкие желатиновые капсулы, содержащие тиоктовую кислоту и соль 3-окси-6-метил 2-этилпиридина, могут быть получены из композиций данного изобретения любым подходящим способом. В качестве наиболее предпочтительных для получения композиции могут использоваться масла растительные, лецитин, воск пчелиный, твердые животные жиры, триглицериды, глицерин. Для лекарственной формы в виде мягких желатиновых капсул приготовляют раствор из 150 мг масла растительного, 50 мг лецитина очищенного с добавлением 50 мг воска 8 15604 1 2012.04.30 пчелиного. 100 мг тиоктовой кислоты и 200 мг 3-окси-6-метил-2-этилпиридина равномерно распределяют в этом растворе. Полученную суспензию вводят традиционно применяемым способом в мягкие желатиновые капсулы, по 550 мг на 1 капсулу. Полученную смесь (0,55 г) с содержанием 100 мг тиоктовой кислоты, 200 мг 3-окси-6 метил-2-этилпиридина сукцината капсулируют в мягкие желатиновые капсулы. Пример 6. Пероральная лекарственная форма в виде гранул для приема внутрь тиоктовая кислота 0,6 г 3-окси-6-метил-2-этилпиридина гидрохлорид 0,3 г целлюлоза микрокристаллическая 0,198 г лактоза 0,7 г крахмал 0,161 г поливинилпирролидон 0,038 г магния стеарат 0,003 г. Гранулы для приема внутрь, содержащие тиоктовую кислоту и соль 3-окси-6-метил-2 этилпиридина, могут быть получены из композиций данного изобретения любым подходящим способом. Для лекарственной формы в виде гранул для приема внутрь используют гранулят, получаемый аналогично способу, описанному в примере 3. Полученный гранулят (2,0 г) с содержанием 600 мг тиоктовой кислоты, 300 мг 3-окси-6-метил-2-этилпиридина гидрохлорида фасуют в пакеты. Пример 7. Пероральная лекарственная форма в виде порошка для приема внутрь тиоктовая кислота 0,6 г 3-окси-6-метил-2-этилпиридина фумарат 0,15 г янтарная кислота 0,1 г сахар-песок 3,5 г. Порошок для приема внутрь, содержащий тиоктовую кислоту и соль 3-окси-6-метил 2-этилпиридина, может быть получен из композиций данного изобретения любым подходящим способом. Проводят измельчение исходных материалов, разделяют частицы порошка по размерам. Смешивают 600 мг тиоктовой кислоты, 150 мг 3-окси-6-метил-2-этилпиридина фумарата, 100 мг янтарной кислоты и 3,5 г сахара-песка. Проводят фасовку (например, в пакеты) по 4,35 г. Пероральная лекарственная форма в виде порошка для приема внутрь, предназначенная для использования пациентами с сахарным диабетом или для иных случаев, когда использование сахара нежелательно, содержит указанные выше количества активных ингредиентов, при этом вместо сахара-песка в состав композиции вводятся разрешенные к медицинскому применению подсластители. Все описанные в примерах 3-7 лекарственные формы должны удовлетворять требованиям Государственной фармакопеи Республики Беларусь 9. Понятно, что в примерах описаны наиболее применяемые на практике варианты фармацевтических композиций,однако заявляемые активные вещества (тиоктовая кислота и соль 3-окси-6-метил-2 этилпиридина в дозировках 0,0001-1,0 г) могут быть включены и в другие фармацевтические композиции (не ограничиваясь приведенными примерами) как для энтерального, так и для парентерального применения, описанные в Государственной фармакопее Республики Беларусь 9. Заявляемая композиция эффективна при патологических состояниях, для которых установлена эффективность тиоктовой кислоты и/или солей 3-окси-6-метил-2-этилпиридина 1-8. Показаниями для применения заявляемой фармацевтической композиции являются патологические состояния, сопровождающиеся оксидантным стрессом профилактика и 9 15604 1 2012.04.30 лечение нарушений памяти и способности к обучению, интеллектуальных расстройств,протекающих на фоне артериальной гипертензии, инсульта, сахарного диабета или без таковых, возникающих у лиц с дисциркуляторной энцефалопатией, при когнитивных расстройствах атеросклеротического генеза развивающихся на фоне тревожных и панических состояний, старения, черепно-мозговой травмы, интоксикаций, стрессорных воздействий,гипогликемии, ишемии, дыхательной гипоксии, умственной отсталости. Композиция применяется для снятия повышенной тревожности, нормализации психоэмоционального статуса, а также при невротических и неврозоподобных состояниях, вегетососудистой дистонии, при нарушениях мозгового кровообращения, инфаркте миокарда, абстинентном синдроме, острых и хронических интоксикациях, острых гнойно-воспалительных процессах в брюшной полости, в том числе остром некротическом панкреатите, перитоните. Лекарственные формы, содержащие комбинацию тиоктовой кислоты и 3-окси-6-метил-2 этилпиридина, применяют 1-3 раза в сутки в течение 30-90 дней. Таблица 1 Влияние перорального введения композиции тиоктовая кислотаэмоксипин на когнитивные функции крыс-самцов линиив тесте экстраполяционного избавления, нарушенные депривацией парадоксальной фазы сна (ДПФС) Группа/доза (мг/кг) условия проведения эксперимента Группа 1 (интактные крысы) Группа 2 растворитель ДПФС Данные оценки когнитивных функций за 40 сек за 120 сек Т 2 (сек) абсолютабсолютв в ное число ное число 32.85,9 25,0 11 100 11 100 Примечания Т 1 - время подныривания под край цилиндра Т 2 - время выхода на сетчатый трап- число животных, решивших задачу избавления за 40 сек, за 120 сек (абсолютное число и в процентах от общего числа животных в группе) Р 1 - различия со значениями в группе 1 статистически достоверны, критерий Крускалла-Уоллиса Р 2 - различия со значениями в группе 1 статистически достоверны, точный метод Фишера Р 3 - различия со значениями в группе 2 статистически достоверны, точный метод Фишера- число животных в группе. Здесь и далее данные представлены в виде или в виде медианы (курсив). 10 15604 1 2012.04.30 Таблица 2 Влияние перорального введения композиции тиоктовая кислотаэмоксипин на неассоциативное обучение, нарушенное депривацией парадоксальной фазы сна (ДПФС), у крыс-самцов линииГруппа/ доза (мг/кг) Группа 1 Вертикальная двигательная активность за 1-ю мин наблюдения (усл. ед.) Высадка 1 (без ДПФС) Высадка 2 (после ДПФС) 12,35,36 52,29,86 8,5 55,0 Примечания Р 1 - различия со значениями при первой высадке статистически достоверны, критерий Уилкоксона- число животных в группе. Источники информации 1. Стаховская Л.В., Алехин А.В., Гусева О.И. // Справочник поликлинического врача. 2007. - Т. 5. -5. 2., //. - 2003. - . 13. . 4. - Р. 241-247. 3..,.,.,.,. // . . . . 2007. - . 72. - Р. 189-193. 4. Регистр лекарственных средств России // Аптекарь. - 2007. - Изд. 9. - С. 113, 627,628, 641, 961, 1130. 5. Патент США 5990152, 1999. 6. Дюмаев К.М., Воронина Т.А., Смирнов Л.Д. Антиоксиданты в профилактике и терапии патологий ЦНС. - М. Институт биомедицинской химии РАМН, 1995. - С. 145,146, 151. 7. Машковский М.Д. Лекарственные средства. 15 изд., перераб., испр. и доп. - М. РИА Новая волна, 2007. - С. 732,733. 8. Мезен Н.И. Медицинский журнал. - 2006. -3. - С. 63-65. 9. Государственная фармакопея Республики Беларусь. (1 изд.) / Под. ред. Г.В.Годовальников, А.А.Шеряков. - Минск, 2006. 10. Савченко Н.М., Островская Р.У., Буров Ю.В. Бюлл. эксперим. биол. и мед. - 1988.8. - С. 170-172. Национальный центр интеллектуальной собственности. 220034, г. Минск, ул. Козлова, 20. 11
МПК / Метки
МПК: A61K 31/385, A61K 31/44, A61P 25/00, A61P 39/06
Метки: композиция, фармацевтическая, действием, антиоксидантным, ноотропным
Код ссылки
<a href="https://by.patents.su/11-15604-farmacevticheskaya-kompoziciya-s-antioksidantnym-i-nootropnym-dejjstviem.html" rel="bookmark" title="База патентов Беларуси">Фармацевтическая композиция с антиоксидантным и ноотропным действием</a>
Предыдущий патент: Способ одномоментного внутреннего дренирования общего желчного протока и протоковой системы поджелудочной железы
Следующий патент: Способ хирургического лечения аваскулярного некроза полулунной кости
Случайный патент: Способ профилактики мочекислого диатеза у кур