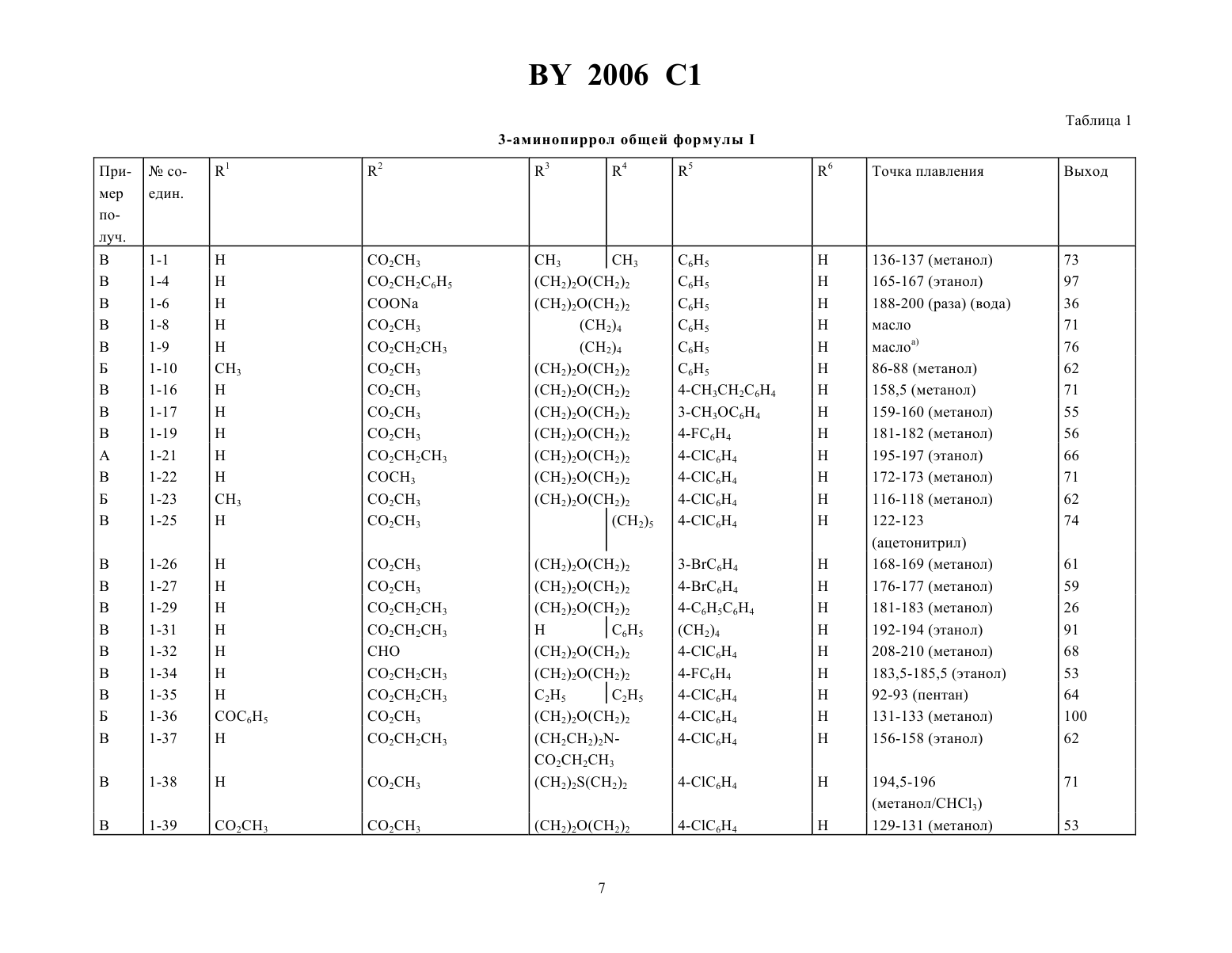
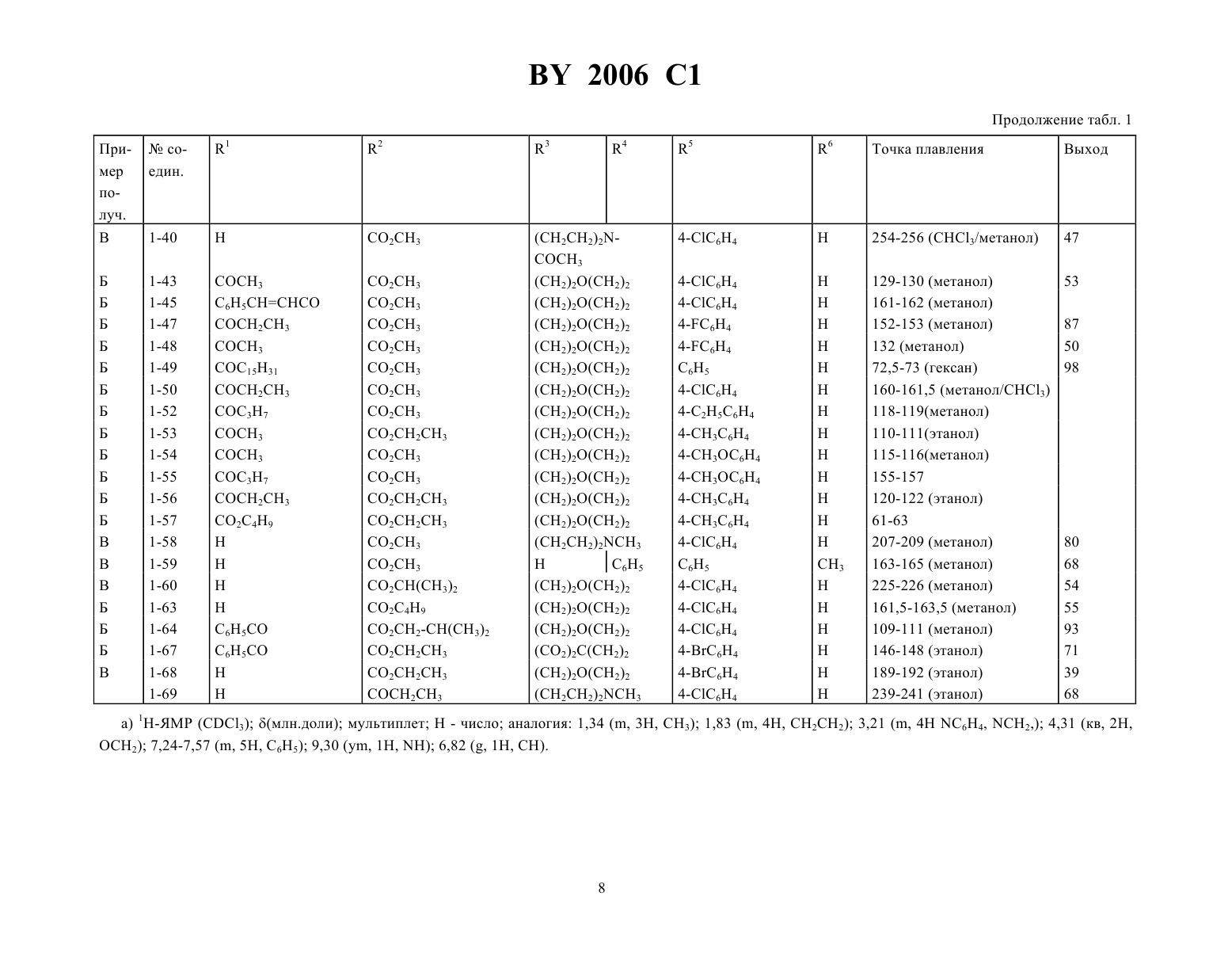
3-аминопирролы и фармацевтическое средство, обладающее антиконвульсивным действием
Номер патента: 2006
Опубликовано: 30.12.1997
Авторы: Александр КНОЛЛЬ, Эвелине МОРГЕНШТЕРН, Андреас РОЛЬФС, Петер ШАРФЕНБЕРГ, ЮРГЕН ЛИБШЕР, Готфрид ФАУСТ, Дитер ЛОМАНН, Алексей УШМАЕВ
Текст
ГОСУДАРСТВЕННЫЙ ПАТЕНТНЫЙ КОМИТЕТ РЕСПУБЛИКИ БЕЛАРУСЬ(71) Заявитель АРЦНАЙМИТТЕЛЬВЕРК ДРЕЗДЕН ГМБХ(72) Авторы Юрген Либшер , Александр Кнолль,Алексей Ушмаев , Андреас Рольфс, Дитер Ломанн, Гоффрид Фауст, Эвелине Моргенштерн,Петер Шарфенберг(73) Патентообладатель АРЦНАЙМИТТЕЛЬВЕРК ДРЕЗДЕН ГМБХ, в которой 1 означает водород, метил, метоксикарбонил, этоксикарбонилметил, ацетил, пропионил, бутирил, пентадеканкарбонил, бензоил, циннамоил, бутоксикарбонил,2 метоксикарбонил, этоксикарбонил, изопропоксикарбонил, бутоксикарбонил, изобутоксикарбонил, натрийкарбоксилато, формил, ацетил, пропионил, бензилоксикарбонил,3 и 4 одинаковые или различные и означают водород, метил, этил, фенил, или группа 34 означает остаток пирролидина, пиперидина, морфолина, тиоморфолина, 4-метилпиперазина, 4-ацетилпиперазина, 4 этоксикарбонилпиперазина,5 означает фенил, 4-толил, 4-этилфенил, 3-метоксифенил, 4-метоксифенил, 4-фторфенил, 4-хлорфенил,3-бромфенил, 4-бромфенил, 4-дифенил,6 - водород или метил,причем 1 и 6 не могут являться водородом, когда 34 является остатком морфолина и 2 и 5 являются соответственно метоксикарбонилом и фенилом, этоксикарбонилом и фенилом, метоксикарбонилом и 4 хлорфенилом, метоксикарбонилом и 4-толилом, этоксикарбонилом и 4-толилом, метоксикарбонилом и 4 метоксифенилом. 2. 3-аминопирролы п п.1, представляющие собой соединения, выбранные из группы, содержащей метиловый эфир 3-диметиламино-4-фенилпиррол-2-карбоновой кислоты,бензиловый эфир 3-морфолино-4-фенилпиррол-2-карбоновой кислоты,натриевую соль 3-морфолино-4-фенилпиррол-2-карбоновой кислоты,метиловый эфир 4-фенил-3-пирролидинопиррол-2-карбоновой кислоты,этиловый эфир 4-фенил-3-пирролидинопиррол-2-карбоновой кислоты,метиловый эфир 1-метил-3-морфолино-4-фенилпиррол-2-карбоновой кислоты,метиловый эфир 4-(4-бромфенил)-3-морфолинопиррол-2-карбоновой кислоты,метиловый эфир 4-(4-хлорфенил)-3-(4-метилпиперазино)-пиррол-2-карбоновой кислоты,метиловый эфир 1-ацетил-4-(4-хлорфенил)-3-морфолинопиррол-2-карбоновой кислоты,2006 1 этиловый эфир 3-морфолино-4-(4-фенилфенил)-пиррол-2-карбоновой кислоты,метиловый эфир 4-(3-метоксифенил)-3-морфолинопиррол-2-карбоновой кислоты,метиловый эфир 4-(4-хлорфенил)-3-тиоморфолино-пиррол-2-карбоновой кислоты,этиловый эфир 4-(4-хлорфенил)-3-(этоксикарбонилпиперазино)-пиррол-2-карбоновой кислоты,метиловый эфир 4-(4-фторфенил)-3-морфолинопиррол-2-карбоновой кислоты,этиловый эфир 4-(4-хлорфенил)-3-морфолинопиррол-2-карбоновой кислоты,метиловый эфир 4-(4-хлорфенил)-1-метил-3-морфолинопиррол-2-карбоновой кислоты,2-ацетил-4-(4-хлорфенил)-3-морфолинопиррол,4-(4-хлорфенил)-2-формил-3-морфолинопиррол,метиловый эфир 4-(4-хлорфенил)-3-пиперидинопиррол-2-карбоновой кислоты,метиловый эфир 4-(3-бромфенил)-3-морфолинопиррол-2-карбоновой кислоты. 3. Фармацевтическое средство, обладающее антиконвульсивным действием, содержащее активный компонент и фармакологически инертные вспомогательные вещества и/или носители, отличающееся тем, что в качестве активного компонента оно содержит соединения формулыпо п.1 в количестве 0,5-20 мг на 1 кг веса пациента.(56) 1. Патент ФРГ 2605419, МКИ С 07 207/34, 1978 г. 2. Патент США 4198502, МКИ С 07 207/14, 1980 г. 3. Кнолль А.П. и Либшер Ю. Синтез эфиров замещенных 3-аминопиррол-2-карбоновых кислот из тиоакриламидов и эфиров глицина // Химия гетероциклических соединений.- 5.-1985.-с. 628. Данное изобретение относится к области лекарственных средств и касается 3-аминопирролов, применяемых в фармацевтических средствах, обладающих антиконвульсивным действием. Антиконвульсивное действие 3-аминопирролов до сих пор не было известно. Описано, что 3-аминопирролы,имеющие в 4-положении аминокарбонильную (патент ФРГ 2605419) или карбонильную группу (патент США 4198502), представляют собой вещества, способные воздействовать на центральную нервную систему. Известно, что это действие носит седативный и анальгетический характер, однако, результаты испытаний в литературе не опубликованы. Синтез этих соединений основан на модификации аминопиррол-производных, которые со своей стороны могут быть получены из -аминонитрилов и -дикарбонильных соединений ( 2605419,2439284,462967,2462966,462962, Брит. 1492663, США 4198502). Шесть представителей 3-морфолино-4-арилпирролкарбоновой кислоты с сильно ограниченными видами заместителей удалось получить путем циклизации морфолидов 3-алкоксикарбонилметиламиноарилтиоакриловой кислоты (А.Кнолль и И.Либскер Хим. Гетероцикл. соед., 1985, 628). О фармакологической активности подобных соединений до сих пор ничего не известно. 3-амино-4-арилпирролы, аминогруппы, в которых незамещены, получали путем восстановления 3-нитропирролов ( , . ., 1960, 3270). 3-амино-2,4-дифенилпиррол образуется при гомоконденсации фенациламина (., . . . ., 41/1908/1127). Известные методы не включают 3-аминопирролов, замещенных по аминогруппе и обладающих при этом антиконвульсивной активностью. Возможности вариации заместителей сильно ограничены. Кроме того, известные антиконвульсивные средства имеют один общий недостаток - они обладают нежелательным побочным действием (например, нейротоксичностью). Задачей изобретения является разработка новых 3-аминопирролов, обладающих активностью в отношении центральной нервной системы, и в частности таких, которые отличаются антиконвульсивной и анальгетической активностью, и их применение в качестве лекарственных веществ и лекарственных средств. При этом следует стремиться снизить до минимума побочное действие, например, сократить нейротоксичность и сделать ее меньше, чем у известных на сегодняшний день антиконвульсивных препаратов. Неожиданно было установлено, что 3-аминопирролы общей формулы 2006 1 3 и 4 одинаковые или различные и означают водород, метил, этил, фенил, или группа 3 4 означает остаток пирролидина, пиперидина, морфолина, тиоморфолина, 4-метилпиперазина, 4-ацетилпиперазина, 4 этоксикарбонилпиперазина,5 означает фенил, 4-толил, 4-этилфенил, 3-метоксифенил, 4-метоксифенил, 4-фторфенил, 4-хлорфенил, 3 бромфенил, 4-бромфенил, 4-дифенил, 6 - водород или метил, причем 1 и 6 не могут являться водородом, когда 34 является остатком морфолина и 2 и 5 являются соответственно метоксикарбонилом и фенилом,этоксикарбонилом и фенилом, метоксикарбонилом и 4-толилом, метоксикарбонилом и 4-метоксифенилом, обладают ценными в фармакологическом отношении свойствами, предпочтительно антиконвульсивной и анальгетической активностью. Заявляемые соединения выбранные из группы, содержащей метиловый эфир 3 диметиламино-4-фенилпиррол-2-карбоновой кислоты, бензиловый эфир 3-морфолино-4-фенилпиррол-2- карбоновой кислоты, натриевую соль 3-морфолино-4-фенилпиррол-2-карбоновой кислоты, метиловый эфир 4 фенил-3-пирролидинопиррол-2-карбоновой кислоты, этиловый эфир 4-фенил-3-пирролидинопиррол-2-карбоновой кислоты, метиловый эфир 1-метил-3-морфолино-4-фенилпиррол-2-карбоновой кислоты, метиловый эфир 4-(4 бромфенил)-3-морфолинопиррол-2-карбоновой кислоты,метиловый эфир 4-(4-хлорфенил)-3-(4 метилпиперазино)-пиррол-2-карбоновой кислоты,метиловый эфир 1-ацетил-4-(4-хлорфенил)-3 морфолинопиррол-2-карбоновой кислоты, этиловый эфир 3-морфолино-4-(4-фенилфенил)-пиррол-2 карбоновой кислоты, метиловый эфир 4-(3-метоксифенил)-3-морфолинопиррол-2-карбоновой кислоты, метиловый эфир 4-(4-хлорфенил)-3-тиоморфолинопиррол-2-карбоновой кислоты, этиловый эфир 4-(4-хлорфенил)-3(этоксикарбонилпиперазино)-пиррол-2-карбоновой кислоты, метиловый эфир 4-(4-фторфенил)-3-морфолинопиррол-2-карбоновой кислоты, этиловый эфир 4-(4-хлорфенил)-3-морфолинопиррол-2-карбоновой кислоты, метиловый эфир 4-(4-хлорфенил)-1-метил-3-морфолинопиррол-2-карбоновой кислоты, 2-ацетил-4-(4-хлорфенил)-3 морфолинопиррол-4-(4-хлорфенил)-2-формил-3-морфолинопиррол, метиловый эфир 4-(4-хлорфенил)-3 пиперидинопиррол-2-карбоновой кислоты, метиловый эфир 4-(3-бромфенил)-3-морфолинопиррол-2 карбоновой кислоты, являются предпочтительными. Заявляемые согласно изобретению соединения с общей формулойв испытании на различных моделях судорог показали высокую антиконвульсивную активность, меньшую токсичность и, главное, - значительно более высокий защитный эффект, чем известные на сегодняшний день антиконвульсивные средства. Удивила их необычайно высокая антиконвульсивная активность, поскольку ранее для 3-аминопирролов такое действие было неизвестно. Новые активные вещества можно включать в обычные лекарственные формы, такие как таблетки, капсулы, драже, гранулы или растворы, при использовании инертных нетоксичных подходящих для этой цели веществ-носителей или растворителей. Получение заявляемых согласно изобретению соединений производится различным способом. Например, соединения с общей формулойможно получать в ходе реакций циклизации, синтезируя их из амидов аминотиоакриловой кислоты и глицериновых радикалов (А. Кнолль,И. Либснер. Хим. гетероцикл., соед., 1985,628). Поэтому другим объектом изобретения является фармацевтическое средство, обладающее антиконвульсивным действием, содержащее активный компонент и фармакологически инертные вспомогательные вещества и/или носители, отличающееся тем, что в качестве активного компонента оно содержит соединения формулыв количестве 0,5-20 мг на кг веса пациента. 3-аминопирролы общей формулы , где 1, 2, 3, 4 или 3/4, 5 или 6 или 5/6 имеют указанное выше значение и в которой 1 и 6 - водород и 34 морфолино, 2 и 5 метоксикарбонил и фенил, этоксикарбонил и фенил, метоксикарбонил 4-хлорфенил, метоксикарбонил и 4-толил, этоксикарбонил и 4-толил,могут быть получены путем циклизации соли триметиния с общей формулой где 1, 2, 3, 4 или 3/4, 5 и 6 или 5/6 - имеют указанное выше значение и в которой Х 1 - отщепляемая группа, например, галоген, алкоксигруппа или аминогруппа, а - - анион кислотного остатка, как-то галогенид, алкилсульфат, сульфонат, сульфат, тетрафтор- или тетраарилборат или пикрат или же, в случае необходимости, соответствующее свободное основание соли триметиния с общей формулойпредпочтительно в присутствии основания. Синтез заявляемых по изобретению соединений общей формулывозможен также за счет введения заместителей. Например, -замещенные 3-аминопирролы общей формулы где 2, 3, 4 или 3/4, 5 и 6 или 5/6 имеют указанное выше значение, взаимодействуют с алкилирующими и ацилирующими средствами общей формулы 11 ,гдеимеет указанные выше значения, и в которой Х - отщепляемая группа, с образованием -замещенных 3 аминопирролов общей формулы , где 1- не водород. Далее для синтеза заявленных по изобретению 3 аминопирролов можно использовать обмен и превращение заместителей у пиррольного скелета. Так, например,3-аминопиррол-2-карбоновые кислоты общей формулы где 1, 3, 4 или 3/4, 5 и 6 или соответственно 5/6 имеют указанные выше значения,при взаимодействии со спиртами превращаются в 3- аминопирролы общей формулы , в которой 2- алкоксикарбонильная группа. Можно также в 2-незамещенные 3-аминопирролы общей формулы, 1 в которой 1, 3, 4 или 3/4, 5 и 6 или 5/6 имеют указанные значения, в 2-положении по известному методу Вильсмайера или по типу ацилирования Фриделя Крафтса вводить группу формила или ацила,вследствие чего происходит образование 3-аминопирролов общей формулы , в которой 2 - формил или ацил. Экспериментальная часть описания. Изобретение иллюстрируется несколькими приведенными ниже примерами. Пример 1. Синтез 3-аминопирролов с общей формулой . В таблице 1 приведено несколько соединений, полученных и испытанных в рамках настоящего изобретения. Их синтез проводился с учетом следующих методик А. Этиловый эфир 4-(4-хлорфенил) 3-морфолино-пиррол-2-карбоновой кислоты (1-21). Раствор 10 ммолей морфолида 2-(Этоксикарбонилметиламино)-2-(4-хлорфенил)тиоакриловой кислоты и 2,2 г метилйодида в 20 мл метанола нагревали в течение 15 минут с обратным холодильником. После добавления 1 мл триэтиламина нагревали еще 5 минут до кипения. После охлаждения разбавляли небольшим количеством воды, отсасывали и перекристаллизовывали. Б. Метиловый эфир 4-(4-хлорфенил)-1-метил-3-морфолинопиррол-2-карбоновой кислоты (1-23). Раствор 5 ммолей метилового эфира 4-(4-хлорфенил)-3-морфолинопиррол-2-карбоновой кислоты в 40 мл метиленхлорида разбавляли 7,5 ммолями алкилирующего средства с общей формулой , где Х 11, и 0,05 г бензилтриэтиламммонийбромида. После добавления раствора 0,05 г бензилтриэтиламмонийбромида в 15 мл 50-едкого натра перемешивали смесь в течение 5 часов при комнатной температуре. После этого нейтрализовали смесь разбавленной соляной кислотой, отделяли органическую фазу, а водную фазу дважды экстрагировали метиленхлоридом. Соединенные органические экстракты промывали водой и раствором карбоната калия. После просушивания над сульфатом натрия растворитель выпаривали. Остаток, представляющий собой конечный продукт, перекристаллизовывался. Аналогичным образом получали соединение 1-10, а с применением ацилирующего средства - соединения 1-36, 1-39, 1-42, 1-43, 1-45, 1-47, 1-48, 1-49, 1-50, 1-52, 1-53, 1-54, 1-55, 1-56, 1-57, 1-61, 1-63, 1-64, 1-67. В. Метиловый эфир 4-(4-бромфенил)-3-морфолинопиррол-2-карбоновой кислоты 1-27. 10 ммолей морфолида 2-(4-бромфенил)-3-диметиламино-тиоакриловой кислоты разбавляли 15 мл метанола, 10 ммолями глицинметилового эфира и 2 г триэтиламина. В течение 5 минут смесь нагревали до ки 4 2006 1 пения. После охлаждения разбавляли небольшим количеством ледяной воды, образующийся остаток отсасывали и просушивали. Продукт растворяли в 10 мл метанола, разбавляли 1,9 г диметилсульфата и нагревали в течение 10 минут с обратным холодильником. После добавления 2 мл триэтиламина нагревали еще 10 минут с обратным холодильником. Конечный продукт отсасывали и перекристаллизовывали. Аналогичным образом получали соединения 1-1, -4, -6, 1-8 1-9, 1-16, 1-17, 1-19, 1-21, 1-25, -26, -27, 29, 1-31, -32, 1-33, -34, -35, -37, 1-38, 1-40, 1-41, -58, -59, 1-60, 1-63 и -68. Г. 2-ацетил-4-(4-хлорфенил)-3-морфолинопиррол (1-22). 10 ммолей 4-(4-хлорфенил)-3-морфолинопиррола разбавляли 10 мл ацетангидрида и в течение 30 минут нагревали с обратным холодильником. После охлаждения выливали в ледяную воду. Конечный продукт отсасывали и перекристаллизовывали. Аналогичным образом получали соединение 1-32. Пример 2. Определение защитного действия от максимального электрошока. Путем электрического раздражения передних лап у мышей весом 8-20 г вызывали разгибательные судороги задних конечностей. Раздражение проводилось при использовании специального прибора ти 12 (частота импульсов 35 герц, широта импульсов 20 мске, осязательное соотношение 11, продолжительность импульса на каждую мышь от 400 до 600 , сила тока прямоугольного импульса 50 мА). Антиконвульсивные средства защищают животных от максимального электрошока. Результаты Соединение 1-19 при внутрибрюшинном введении Эффект. доза - ЭД 50 4,110-5 моль/кг при введении через рот ЭД 503,610-5 моль/кг Другие результаты исследования см. таблицу 2. Сравнительные значения для карбамазепина при пероральном введении ЭД 50 4,310-5 моль/кг. Пример 3. Определение активности при судорогах, вызванных пентетразолом. При внутривенном введении в копчиковую вену мышей (18-22 г) определенной дозы препарата отмечались разгибательные судороги задних конечностей животных. Снятие клинической картины судорог рассматривалось как критерий антиконвульсивного эффекта исследуемых веществ. Полученные результаты Соединение 1-27 При внутрибрюшинном введении ЭД 50 2,710-5 моль/кг. Пример 4. Определение порога появления судорог. При введении 100 мг/кг пентетразола (скорость вливания - 36 мл/час) в копчиковую вену мышей с массой тела 16-22 г отмечали первые признаки клинических судорог (миоклонические подергивания). Увеличение продолжительности введения (в сек.) до момента появления судорог в сравнении с контрольной группой рассматривалось как проявление повышения пороговой дозы для пентетразола, а следовательно как антиконвульсивный эффект исследуемого вещества. Результаты Соединение 1-10 При внутрибрюшинном введении 510-4/кг 19,4 повышение порога наступления судорог. Пример 5. Ориентировочное определение летальной дозы. Подопытные животные получали испытуемое вещество в количестве 510-4, 10-3 и 510-3 моль/кг веса тела мыши (вес 18-22 г). Через 24 часа определяли летальность животных. Результаты исследований приведены в таблице 2. Пример 6. Определение анальгетической активности в опытах на нагретой панели. Мыши весом 18-22 г через 30 минут после введения исследуемого вещества помещались на панель, нагретую до 56 С. Цель исследования - определение времени реакции на болевое термическое раздражение. Увеличение времени реакции для животных, получивших вещество, в сравнении с контрольной группой оценивалось как анальгетический эффект. Результаты Соединение 1-19 при пероральном введении 4,110-4 мол/кг торможение 95 (60 мин). Соединение 1-1 перорально 110-4 мол/кг торможение 51 (60 мин). Соединение 1-36 перорально 10-4 мол/кг торможение 42 (60 мин). Соединение 1-39 перорально 410-4 мол/кгторможение 64 (60 мин). Сравнительные данные 5 2006 1 Анальгин 55-ное торможение при пероральном введении 10-3 мол/кг (60 мин). Пример 7. Определение анальгетической активности при испытании веществ в отношении их способности воздействовать на подергивания вызван уксусной кислотой. При внутрибрюшинном введении 0,6-ной уксусной кислоты мышам с весом тела 18-22 г у последних отмечалось подергивание брюшной стенки. Мерой активности вещества служило сокращение количества реакций подергивания у обработанных животных в сравнении с контрольной группой. Наряду с веществами, обладающими анальгетической активностью, способность снимать или существенно сокращать явления подергивания обладают такие соединения, воздействующие на центральную нервную систему. Результаты соединение 1-6 перорально 110-4 мол/кг торможение 50,2,соединение 1-19 перорально 410-5 мол/кг торможение 48,9,соединение 1-21 перорально 110-4 мол/кг торможение 51,6. Сравнительные результаты Анальгин при пероральном введении 10-4 моль/кг 50 торможения. Пример 8. Определение нейротоксичности в опытах на моделях с вращающейся палочкой. Подготовленные соответствующим образом мыши с весом тела 8-22 г после введения вещества на 1 минуту высаживались на вращающуюся дощечку (5 оборотов в минуту). Мерой активности вещества служил факт преждевременного соскальзывания с дощечки. Защитный показатель представлял собой частное от значений ТД 50/ЭД 50 МЕК (единица стандартизации при действии на мышей). Результаты соединение -23 внутрибрюшинно ТД 50,310-3 мол/кг,защитный показатель 16,7,соединение 1-26 внутрибрюшинно Д 502,210-3 мол/кг,защитный показатель 9,6,соединение -36 внутрибрюшинно ТД 508,610-4 мол/кг,защитный показатель 18,3. Сравнительные данные Карбамазепин ТД 502,210-4 мол/кг,защитный показатель 5,1. Пример 9. Формы применения. Для применения предлагаются следующие лекарственные формы (рецептуры) Капсулы. 1 вес. ч. 3-аминопиррола общей формулысуспендируется в 2 вес.частях полиэтиленгликоля 600 и перерабатывается в желатиновую смесь следующего состава желатин 1 весовая часть,глицерин 5 весовых частей,вода 2 весовых части. Капсулы. Составляют смесь, включающую следующие компоненты лактоза 5 весовых частей,картофельный крахмал 5 весовых частей,стеарат магния 1 весовая часть. К этой смеси добавляют 1 вес. часть соединения общей формулы . Таблетки. Прямое таблетирование без введения в оболочку (состав компонентов на таблетку) активное вещество (например, 1-19) 100 мг,10 мг,микрокристаллическая целлюлоза 15 мг,стеарат магния 1 мг. Антиконвульсивное действие на моделях при максимальном раздражении электротоком на мышах Доза (моль/кг) внутри Торможение судорог 1-4 110-3 70 1-6 510-4 а) 10 1-8 510-4 70 1-9 510-4 70 1-10 510-4 100 1-16 510-4 100 1-17 510-4 80 1-19 510-4 100 1-20 510-4 100 1-23 510-4 100 1-25 510-4 90 1-26 510-4 10 1-27 510-4 100 1-29 510-4 20 1-31 110-3 10 1-32 510-4 100 1-34 510-4 100 1-35 510-4 100 1-36 510-4 100 1-37 510-4 10 1-38 510-4 80 1-39 510-4 100 1-40 510-4 80 1-43 510-4 100 1-44 510-4 70 1-47 510-4 90 1-48 510-4 100 1-49 510-4 18,9 в)-4 1-50 510 100 1-52 510-4 100 1-53 510-4 100 1-54 510-4 100 1-55 510-4 100 1-56 510-4 100 1-57 510-4 100 1-58 110-5 90 1-59 510-4 40 1-60 510-4 100 1-63 510-4 80 1-64 510-4 70 1-67 510-4 80 1-68 510-4 90 1-69 110-5 90 а) перорально,в) повышение порога судорог, вызванных пентетразолом. Сравнительные данные Карбамазепин ЕД 504,3 (3,2-5,8)10-5110-3510-3 Фенобарбитал ЕД 506,0 (3,9-9,2)10-55,10-4 ФенитоинЕД 502,4 (1,5-3,9)10-5110-3510-3 оставитель А.С. Жаврид Редактор Т.А. Лущаковская Корректор Т.Н. Никитина Заказ 7056 Тираж 20 экз. Государственный патентный комитет Республики Беларусь. 220072, г. Минск, проспект Ф. Скорины, 66. Ориентировочная летальная доза Доза (моль/кг) 510-3 р.о. 510-3 р.о. 110-3 510-3 110-3 510-3 510-3 р.о. 510-3 510-3 110-3 510-3 р.о. 510-3 510-4 510-3 110-3 110-3 110-3 110-3 110-3 110-3 510-3 110-3 510-3 510-3 510-3 510-3 110-3 510-3 510-3 510-3 110-4 110-3 110-3 110-3 110-3 110-3 110-3 110-4
МПК / Метки
МПК: C07D 417/04, A61K 31/40, C07D 403/04, C07D 207/34
Метки: 3-аминопирролы, средство, обладающее, действием, антиконвульсивным, фармацевтическое
Код ссылки
<a href="https://by.patents.su/9-2006-3-aminopirroly-i-farmacevticheskoe-sredstvo-obladayushhee-antikonvulsivnym-dejjstviem.html" rel="bookmark" title="База патентов Беларуси">3-аминопирролы и фармацевтическое средство, обладающее антиконвульсивным действием</a>
Предыдущий патент: Средство для защиты растений риса, кукурузы или сорго от фитотоксического действия гербицидов
Следующий патент: Кровельный гидроизоляционный материал
Случайный патент: Устройство для кротования почв