Производные ?-трикетонов тиофенового ряда, проявляющие антифосфолипазную активность антигемолитического профиля действия
Номер патента: 10192
Опубликовано: 28.02.2008
Авторы: Кучуро Светлана Викторовна, Желдакова Татьяна Анатольевна, Рубинов Дмитрий Брониславович, Литвинко Наталья Михайловна, Рахуба Галина Николаевна
Текст
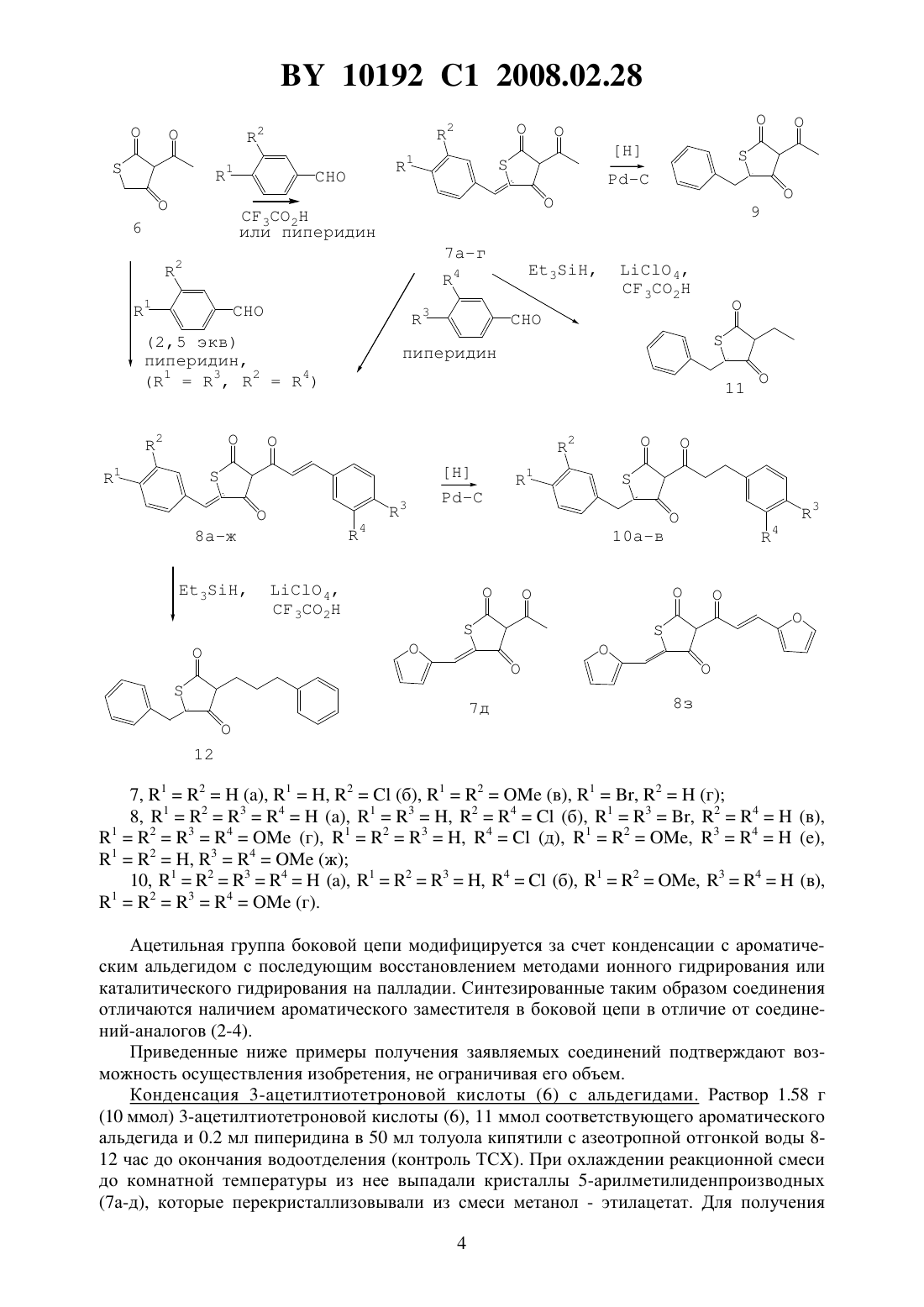
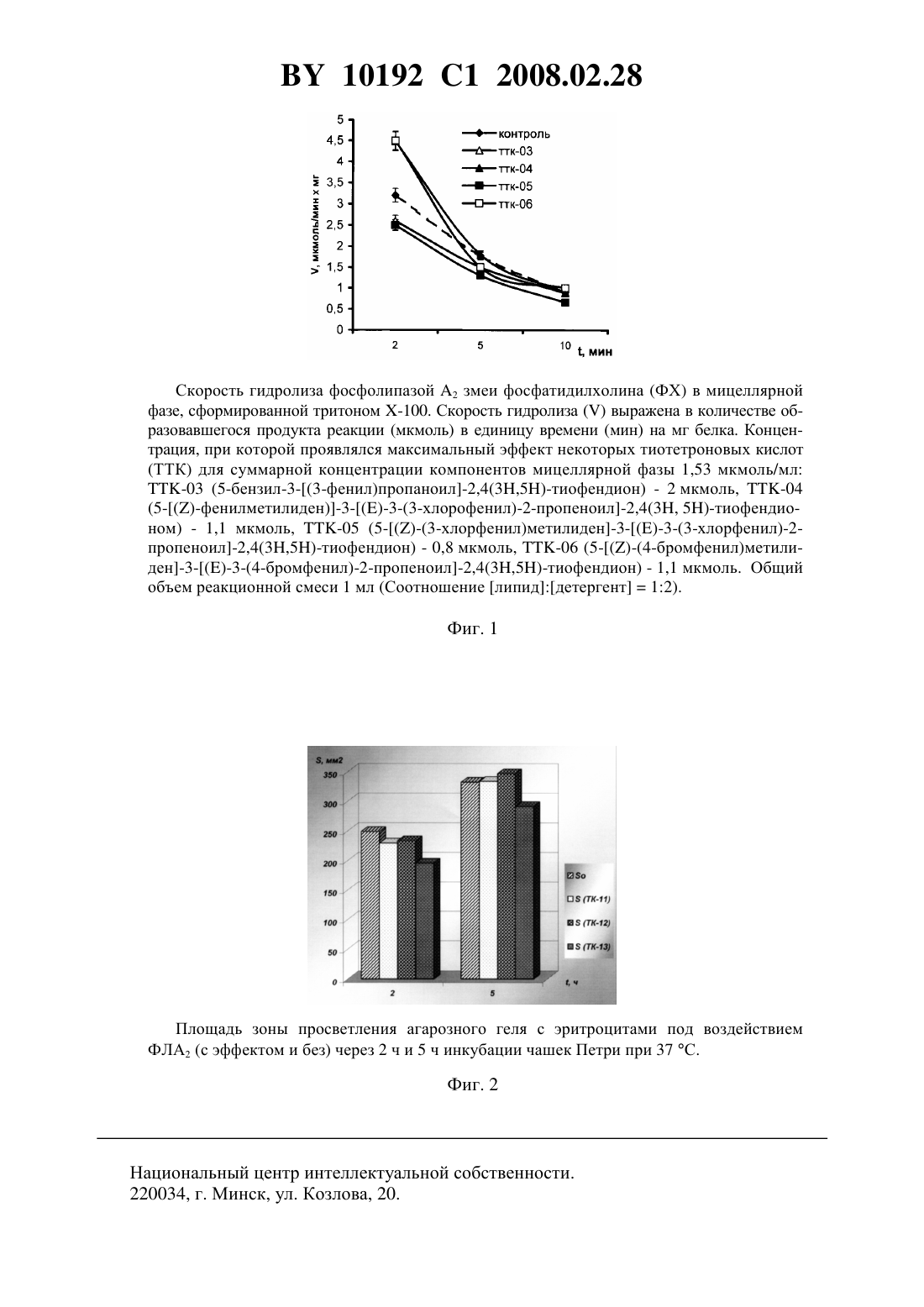
(51) МПК (2006) НАЦИОНАЛЬНЫЙ ЦЕНТР ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ ПРОИЗВОДНЫЕ -ТРИКЕТОНОВ ТИОФЕНОВОГО РЯДА,ПРОЯВЛЯЮЩИЕ АНТИФОСФОЛИПАЗНУЮ АКТИВНОСТЬ АНТИГЕМОЛИТИЧЕСКОГО ПРОФИЛЯ ДЕЙСТВИЯ(71) Заявитель Государственное научное учреждение Институт биоорганической химии Национальной академии наук Беларуси(72) Авторы Рубинов Дмитрий Брониславович Желдакова Татьяна Анатольевна Литвинко Наталья Михайловна Кучуро Светлана Викторовна Рахуба Галина Николаевна(73) Патентообладатель Государственное научное учреждение Институт биоорганической химии Национальной академии наук Беларуси(57) Производные -трикетонов тиофенового ряда общей формулы где 1 означаетили ,2 означаетили ,проявляющие антифосфолипазную активность антигемолитического профиля действия. Изобретение относится к области биоорганической химии, в частности к новым биологически активным веществам - производным -трикетонов тиофенового ряда общей формулы 10192 1 2008.02.28 где 1 означаетили ,2 означаетили ,проявляющие антифосфолипазную активность, которые могут найти применение в качестве ингибиторов секреторной фосфолипазы А 2 яда змеи, а именно в качестве противоядия - средств антигемолитического профиля действия. Известны биологически активные 3-ацил-2,4-тиофендионы (2-4), проявляющие противоартритные 1, иммуносупрессорные 2, антибактериальные свойства 3, являющиеся структурно родственными природным антибиотикам тиолактомицину (5 а) и тиотетромицину (5 б), выделенным из почвенных бактерий рода 4. Известны также соединения (4),имеющие достаточно объемную гидрофобную боковую цепь, которые ингибируют фосфолипазу А 2 (ФЛА 2, К.Ф. 3.1.1.4) форменных элементов крови и синовиальной жидкости 3. 2,галоген,алкил или алкокси 3,галоген, алкил, алкокси 4,Н, , , ,1-15,0-20. Существенные изменения уровня активности ФЛА 2, катализирующей гидролиз фосфолипидов по 2-му положению глицеринового скелета, наблюдаются при остром панкреатите, воспалительных процессах, патогенетических поражениях печени, гипоксии,аллергии и тромбообразовании, отеках вследствие радиационного поражения и развитии злокачественных новообразований. Накопление продуктов ферментативного гидролиза фосфолипидов в органах и тканях является признаком ишемической болезни и следствием активации ФЛА 2. Клеточные ФЛА 2 играют ключевую роль в биосинтезе активных метаболитов арахидоновой кислоты. Воздействие ядов змей на организм млекопитающих также связано с функционированием ФЛА 2. Описанные вещества (2-4) рассматриваются как полезные только при лечении расстройств, вызываемых продуктами окисления арахидоновой кислоты, которая высвобождается из фосфолипидов под действием внутриклеточной высокомолекулярной (80 кДа и выше) фосфолипазы А 2, содержащейся в форменных элементах крови. Соответственно,указанные соединения могут быть полезны только для предотвращения и лечения иммуно 2 10192 1 2008.02.28 воспалительных заболеваний, таких как аллергия, анафилаксия и воспаление, вызванное только оксилипинами (продуктами окисления арахидоновой кислоты). В круг таких заболеваний входят аллергические риниты, аллергическая бронхиальная астма, бронхиальные обструктивные расстройства верхних дыхательных путей, а также различных прямых гиперчувствительных реакций, таких как аллергический конъюктивит, воспалительные процессы, имеющие место при ревматоидных артритах, остеоартритах, тенденитах, бурситах,псориазе и др. Суперсемейство липолитических ферментов фосфолипаз А 2 объединяет 11 классификационных групп 5, которые делятся на два больших пула. Один пул представляют низкомолекулярные (12-18 кДа) внеклеточные ферменты, выделяемые железами внутренней секреции млекопитающих (поджелудочная железа, семенники, селезенка, тимус) и ядовитыми железами змей, у которых установлено участие аминокислоты гистидин в каталитическом акте. Второй пул представляют высокомолекулярные (80 кДа и выше) внутриклеточные ферменты, у которых установлено участие в каталитическом акте другой аминокислоты серин. Таким образом, указанные выше соединения 1-5 а,б имеют ограниченный спектр действия, распространяющийся только на группы фосфолипаз, входящих во второй пул этого суперсемейства. В то же время известно, что нервно-паралитическое и гемолитическое действие яда змей также связано с активностью низкомолекулярной формы ФЛА 2 6. Задачей настоящего изобретения являются новые производные -трикетонов тиофенового ряда общей формулы где 1 означает Н или Вг,2 означает Н или С 1,отличающиеся от соединений-аналогов наличием ароматического заместителя в боковой цепи и новым спектром действия на низкомолекулярные формы ФЛА 2, проявляющие свойства антигемолитического профиля. Поставленная задача решается получением заявляемых соединений, проявляющих ингибиторные свойства по отношению к активности низкомолекулярных секреторных фосфолипаз А 2 (ФЛА 2) и являющихся потенциальными лекарственными средствами антигемолитического профиля. Биологическое действие заявляемых соединений подтверждено тестированиемс использованием ФЛА 2 яда кобры , результаты которого приведены в разделе Исследование биологической активности. Заявляемые соединения получают конденсацией 3-ацетилтиотетроновой кислоты (6) с ароматическими альдегидами в условиях как кислотного, так и основного катализа по метиленовой группе цикла с образованием 5-замещенных -трикетонов (7) 1. Проведением этой реакции с использованием пиперидина в качестве катализатора получают 5-арилметилиденовые ацетилтиофендионы (7 а-д). 7, 12, 1, 2(б), 12(в), 1, 2(г) 8, 1234, 13, 24(б), 13, 24(в),1234(г), 123, 4(д), 12, 34,12, 34(ж) 10, 1234, 123, 4(б), 12, 34(в),1234(г). Ацетильная группа боковой цепи модифицируется за счет конденсации с ароматическим альдегидом с последующим восстановлением методами ионного гидрирования или каталитического гидрирования на палладии. Синтезированные таким образом соединения отличаются наличием ароматического заместителя в боковой цепи в отличие от соединений-аналогов (2-4). Приведенные ниже примеры получения заявляемых соединений подтверждают возможность осуществления изобретения, не ограничивая его объем. Конденсация 3-ацетилтиотетроновой кислоты (6) с альдегидами. Раствор 1.58 г(10 ммол) 3-ацетилтиотетроновой кислоты (6), 11 ммол соответствующего ароматического альдегида и 0.2 мл пиперидина в 50 мл толуола кипятили с азеотропной отгонкой воды 812 час до окончания водоотделения (контроль ТСХ). При охлаждении реакционной смеси до комнатной температуры из нее выпадали кристаллы 5-арилметилиденпроизводных(7 а-д), которые перекристаллизовывали из смеси метанол - этилацетат. Для получения 4 10192 1 2008.02.28 продуктов двойной конденсации (8 а-г,з) в реакции использовали 25 ммол соответствующего альдегида. Синтез продуктов (8 д-ж) осуществляли по вышеприведенной методике в две стадии, без выделения промежуточного продукта. При этом на первой стадии использовали эквивалентное количество альдегида, создающего арилметилиденовый заместитель в цикле, а на второй - 1.5 экв другого альдегида, конденсирующегося по боковой цепи. 3-Ацетил-5 фенилметилиден-2,4-(3)тиофендион (7 а). Выход 2.02 г (82 ). Т.пл. 147-150 С (лит. 151-152 С 7). ИК спектр, , см-1 1660, 1640, 1620, 1580, 1565. Спектр ЯМР 1 Н, , м.д. 2.62 с (3 Н, СН 3), 7.40-7.50 м (3 Н, ), 7.55-7.60 м (2 Н, ), 7.86 с(2 Н, С(О)СНСН,16.0 Гц), 16.30 ушир. с (1 Н, енол). Найдено,С 66.92 Н 4.588.16.394. 22185. Вычислено,С 66.99 Н 4.608.13. 52-Фурилметилиден-3-(Е)-3-(2-фурил)-2-пропеноил-2,4(3)тиофендион (8 з). Выход 2.00 г (64 ). Т. пл. 199-203 С (разл.). ИК спектр, , см-1 1700, 1620, 1580, 1530. Спектр ЯМР 1 Н, , м.д. 6.60 м (2 Н, ОСС 2), 6.82 д и 6.89 д (2 Н, ОССНСН 2,4.0 Гц),7.64 д и 7.70 д (2 Н, ОСНСН 2,2.0 Гц), 7.63 с (1, ), 7.84 с (2 Н, С(О)СНСН),16.40 ушир. с (1, енол). Найдено,С 61.31 Н 3.2910.27.314. 16105. Вычислено,С 61.14 Н 3.2110.20. Каталитическое гидрирование продуктов конденсации (7 а) и (8 а,г-е). Раствор 5 ммол ненасыщенного соединения в 50 мл метанола гидрировали при комнатной температуре и нормальном давлении в присутствии 100 мг 10 -ногона угле до полного насыщения водородом (ТСХ). Затем катализатор отфильтровывали, растворитель удаляли в вакууме, остаток растворяли в хлороформе, пропускали через слой силикагеля(10 г). Выход 2.25 г (98 ). Т.пл. 116-117 С (гексан). ИК спектр, , см-1 1700, 1635, 1610,1585, 1560. Спектр ЯМР 1 Н, , м.д. 2.95 т (2 Н, СОСН 2,7.5 Гц), 3.22 т (2 Н, СОСН 2 СН 2, 7.5 Гц), 3.35 м (1, РСНН), 3.82-3.92 м (2 Н, РСНН, ), 3.86 с, 3.89 с, 3.95 с и 3.98 с (12 Н, 4 ОСН 3), 6.80-7.22 м (6 Н, 2 С 6 Н 3), 12.80 ушир. с (1, енол). Найдено,С 63.00 Н 5.817.07.458, 459. 24267. Вычислено,С 62.87 Н 5.726.99. Ионное гидрирование соединений (7 а) и (8 а). К раствору 1 ммол трикетона в 5 мл трифторуксусной кислоты (ТФУК) добавляли 2 мл 1 -ного раствора перхлората лития в ТФУК и 2.0 мл (12.5 ммол) триэтилсилана. Реакционную смесь перемешивали при комнатной температуре 8-12 час (контроль ТСХ). Избыток реагентов и растворитель удаляли в вакууме. Остаток растворяли в 50 мл хлороформа, однократно промывали водой, сушили сульфатом магния, хлороформ упаривали в вакууме. 5-Бензил-3-этил-2,4-(3,5)тиофендион (11). Выход 0.14 г (60 ). Маслообразное вещество. ИК спектр, , см-1 1750, 1705, 1610. Спектр ЯМР 1 Н, , м.д. 1.00 т (3 Н, СН 3, 7.5 Гц), 2.24 кв (2 Н, СН 3 С 2,7.5 Гц), 2.93 дд (1, СНР, 1 14.0 Гц, 2 10.0 Гц), 3.55 дд(1, , 1 10.0 Гц, 2 4.0 Гц), 7.20-7.40 м (10 Н, С 6 Н 5), 10.00 ушир. с (1, енол). Найдено,С 73.98 Н 6.119.94.324. 20202. Вычислено,С 74.04 Н 6.219.88. Исследование биологической активности. Смешанные мицеллы получают солюбилизацией раствором детергента пленки, образующейся после удаления растворителя из раствора фосфатидилхолина (ФХ) в хлороформе. Смешанные мицеллы готовят включением фосфатидилхолина в фазу поверхностноактивных веществ - дезоксихолата натрия (ДОХ, анионный детергент) и тритона-Х-100(ТХ, неионный детергент) при оптимальном соотношении 12. Реакционная смесь содержала 2 мМ СаС 2 и 0,05 М трис-, рН 7,4. Реакцию гидролиза смешанных мицелл начинают добавлением в среду при 20 С раствора ФЛА 2 змеи (0,066 ед./мл) и останавливают добавлением ЭДТА до конечной концентрации 15 мМ. Преинкубация фермента с -трикетонами тиофенового ряда продолжалась в течение 80 мин. Продукты ферментативной реакции из реакционной среды экстрагируют двумя объемами смеси хлороформ/метанол 21 (по объему). Степень экстракции составляет не менее 85 . Нижний слой отделяют, растворитель упаривают и продукты реакции анализируют с помощью тонкослойной хроматографии на силикагеле в системе растворителей хлороформ/метанол/вода 65254. Пластины проявляли реагентом на фосфолипиды, пятна фосфолипида и его лизопроизводного выскребали и анализировали в них содержание фосфора по методу, описанному в работе 8. За единицу активности ФЛА 2 принимали количество фермента, катализирующее образование 1 мкмоль продукта/мин при 20 С 10192 1 2008.02.28 На основе изменения скорости гидролиза ФХ (мкмольмин-1 мг-1) в мицеллярной фазе под действием ФЛА 2 яда змеив отсутствие (0) и в присутствиипроизводных тиотетроновой кислоты обнаружено, что по глубине воздействия на липолиз наиболее существенное ингибиторное действие в описанных условиях проведения эксперимента оказали дихлорзамещенное арилметилиденовое производное (8 б) и не содержащий олефиновых связей ни в цикле, ни в боковой цепи трикетон (10 а) на всем временном интервале скорость гидролиза ФХ после преинкубации фермента с (8 б) и (10 а) была вдвое ниже контрольной величины (фиг. 1). На фиг. 1 показана зависимость скорости гидролиза фосфолипазой А 2 змеи фосфатидилхолина (ФХ) в мицеллярной фазе, сформированной тритоном Х-100 (приложение 1). Проведен первичный скрининг действия полученных производных тиотетроновой кислоты на процесс гемолиза при воздействии ФЛА 2 яда змеина эритроциты, включенные в агарозный гель. Для выявления среди -трикетонов тиофенового ряда антигемолитических эффекторов ФЛА 2 используется модификация экспрессного метода диффузии фермента в тонком слое агарозного геля 9 с включенными в него эритроцитами вместо яичного желтка в качестве субстрата. Преинкубация ФЛА 2 с соединениями (8 бг) и (10 а) приводила к четкому визуальному изменению площади зоны лизиса, что свидетельствовало о существенном эффекте этих соединений на гемолитическую активность ФЛА 2 (фиг. 2). На фиг 2 приведено изменение площади зоны просветления агарозного геля с эритроцитами под воздействием ФЛА 2 (с эффектором и без) через 2 ч и 5 ч инкубации чашек Петри при 37 С (приложение 2). Источники информации 1.. . . . . (С). 1968, 1501. 2..,. . . 1983, 36, 1589. 3. Патент США 5366993, .1507 333/1661 31/38. с, .А.,С 1, С, , , о ,заявки 71627. Заявл. 03.06.1993. 4.Т.,.,.,.,. . . 1982, 35, 401. 5. , , (2000) . . , 1006, 1-9. 6. Литвинко Н.М. Активность фосфолипаз А 2 и С при биохимическом моделировании. Мн., 2002. 7. , Т (1988) . . , 23, 897-904. 8. оу , Коу , // . . - 1975. - . 114. -1. . 129-141. 9. Пат.5752 РБ, МПК // Способ определения эффекторных свойств физиологически активных соединений / Н.М. Литвинко, С.В. Кучуро, Т.А. Желдакова, Е.Р. Филич (РБ) зарегистрировано 07.08.2003. Скорость гидролиза фосфолипазой 2 змеи фосфатидилхолина (ФХ) в мицеллярной фазе, сформированной тритоном -100. Скорость гидролизавыражена в количестве образовавшегося продукта реакции (мкмоль) в единицу времени (мин) на мг белка. Концентрация, при которой проявлялся максимальный эффект некоторых тиотетроновых кислот(ТТК) для суммарной концентрации компонентов мицеллярной фазы 1,53 мкмоль/мл(5 фенилметилиден)-33-(3-хлорофенил)-2-пропеноил-2,4(3, 5)-тиофендионом) - 1,1 мкмоль, -05 (5(3-хлорфенил)метилиден-33-(3-хлорфенил)-2 пропеноил-2,4(3,5)-тиофендион) - 0,8 мкмоль, -06 (5(4-бромфенил)метилиден-33-(4-бромфенил)-2-пропеноил-2,4(3,5)-тиофендион) - 1,1 мкмоль. Общий объем реакционной смеси 1 мл (Соотношение липиддетергент 12). Площадь зоны просветления агарозного геля с эритроцитами под воздействием ФЛА 2 (с эффектом и без) через 2 ч и 5 ч инкубации чашек Петри при 37 С. Национальный центр интеллектуальной собственности. 220034, г. Минск, ул. Козлова, 20. 9
МПК / Метки
МПК: A61P 43/00, C07D 333/00
Метки: действия, тиофенового, антигемолитического, производные, проявляющие, ряда, антифосфолипазную, активность, профиля, трикетонов
Код ссылки
<a href="https://by.patents.su/9-10192-proizvodnye-triketonov-tiofenovogo-ryada-proyavlyayushhie-antifosfolipaznuyu-aktivnost-antigemoliticheskogo-profilya-dejjstviya.html" rel="bookmark" title="База патентов Беларуси">Производные ?-трикетонов тиофенового ряда, проявляющие антифосфолипазную активность антигемолитического профиля действия</a>
Предыдущий патент: 3,5-Дизамещенные производные тиотетроновой кислоты, проявляющие антифосфолипазную активность антипанкреатического профиля действия, и способ их получения
Следующий патент: Градирня
Случайный патент: Насосная установка