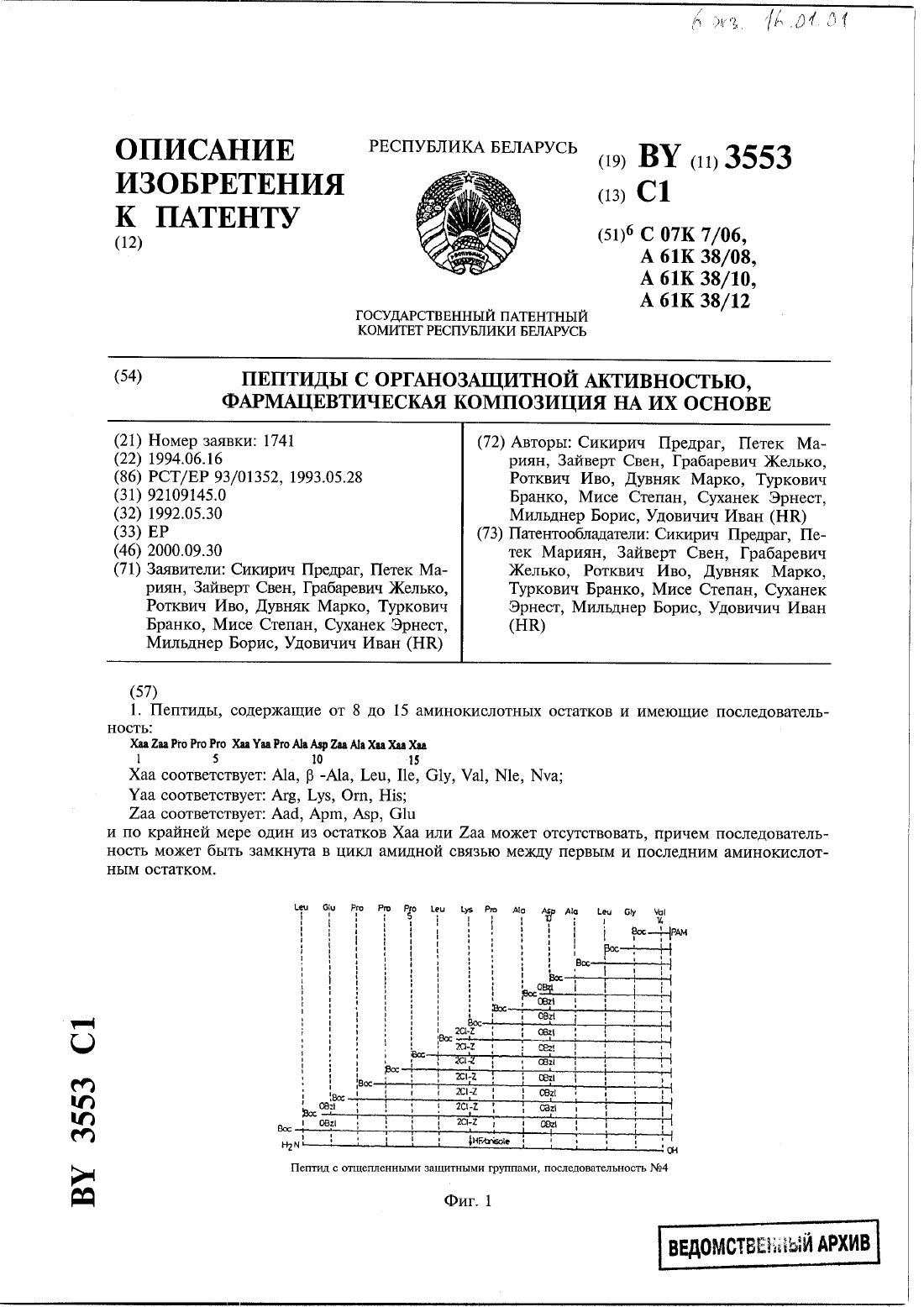
Пептиды с органозащитной активностью, фармацевтическая композиция на их основе
Номер патента: 3553
Опубликовано: 30.09.2000
Авторы: Удовичич Иван, Мильднер Борис, Туркович Бранко, Мисе Степан, Дувняк Марко, Петек Мариян, Зайверт Свен, Ротквич Иво, Суханек Эрнест, Грабаревич Желько, Сикирич Предраг
Текст
2. Пептиды по п. 1, отличающиеся тем, что по меньшей мере 1 и самое большее 7 аминокислотных остатков с 1 по 15 отсутствуют.3. Пептид по п. 1 представляет собой последовательность Ъш 6111 Рго Рго Рго О 1 у Вуз Рго М Азр Акр М Ьш 01 у Ул 10(Ну 6111 Рго Рю Рго (Ну Ьуя Рго М Азр Аар М (Ну Ьш ум 1 5 ю 155. ПСПТИД ПО П. 1 представляет СОбОЙ ПОСЛСДОВЗТСЛЬНОСТЬ ли они Рго Рю Рго Ьш Ьув Рю А Адр Аар Ми Ъец (Ну Уз6. Пептид по п. 1 представляет собой последовательность Ъеи 6111 Рго Рго Рго Ьеи Ьуз Рго А 1 а Азр АЬЪш 61 у Ул7. Пептид по п. 1 представляет собой последовательность Сг 1 у 61 и то Рю Рго (Ну Ьу Рго М Адр М (Ну мл Уз 1 - 5 10 14 8. Пептид по п. 1 представляет собой последовательность бшРго РгоРгоЬепЬувРгоАиАвр 1 5 . 99. Пептид по п. 1 представляет собой последовательность 611 Рго Рго Рго Ьш Ъув Рго А 1 а1 . 5 8 10. Пептид по п. 1 представляет собой последовательность АарРгоРго РгоЦеАтвРгоАЬАдр 1 5 91 1. Циклический пептид по п. 1, представляет собой последовательность ъщбшРгсРгоРгоьшъуаРгоАпАхрАи ЪшСНуУЦ12. Циклический пептид по п. 1 представляет собой последовательностьОт 6111 Рю Рто Рго 61 у М Рго Ми Аэр 2 513. Фармацевтическая композиция для защиты от образования желудочно-кишечных язв различной этиологии, радиационных поражений и мальформаций, защиты при химических ожогах, отеках, травмах, костных переломах, вирусных инфекциях, депрессивных и шоковых состояниях, нарушениях допаминэргической этиологии, содержащая в качестве активного начала один или несколько пептидов по любому из пп. 1-12, взятых в эффективном количестве,в смеси с фармацевтически приемлемым твердым или жидким носителем.Изобретение относится к новым пептидам, обладающим высокой биологической активностью того же типа, которая присуща известному природному соединению ВРС, но имеющим более короткие аминокислотные цепи.Биологически активный белок с органе-защитной (огвапо-ргокесгйуе) активностью, который выделен из организма человека или животного и назван ВРС (Воду Ргогесйпз Сошропп соединение, защищающее организм), раскрыт в Европейском патенте 1, а также в публикации 3. Этот белок имеет высокую мол. м. - 4000015000 Дальтон и только частично установленную структуру. Это соединение имеет очень широкий спектр биологической активности, защищая от язв, защищает печень, оказывает противовирусное и противоотечное действие, обладая общей противовоспалительной активностью, противоопухолевой активностью и другим действием. Их следует применять в терапии перечисленных заболеваний, а также в терапии заболеваний и расстройств нервной системы, нарушений допаминэргической (аорапппегвйс) этиологии,в хирургии, в стоматологии, для лечения фертильности и в ветеринарии. Но такой широкий спектр активности может быть, вероятно, следствием неопределенной структуры или даже недостаточной чистоты или однородности выделенного соединения ВРС.Мы открыли синтетические пептиды, содержащие в цепи только 8-15 аминокислотных остатков, с мол. м. 900-1600 Дальтон, которые обладают биологической активностью природного защищающего организм соединения ВРС, но с увеличенной селективностью. Наши новыепептиды более экономичны при производстве и менее подвержены действию побочных реакций, поскольку они содержат меньше аминокислотных остатков, чем ВРС.В соответствии с одной из сторон изобретения предлагается класс синтетических пептидов,которые обнаруживают удивительно высокую биологическую активность, особенно в смысле защиты организма. В любом случае эти синтетические соединения с совершенно определенным строением имеют большое преимущество при сравнении с высокомолекулярным белком ВРС, строение которого установлено только частично и которое возможно получать по сложному технологическому процессу из непостоянных природных источников.Конкретнее, это изобретение относится к новому классу биологически высокоактивных пептидов, содержащих 8-15 аминокислотных остатков, которые изображаются следующей основной структурной формулой с использованием трехбуквенного кода аминокислот и цифр,стоящих под каждым аминокислотным остатком, обозначающих положение остатка в пептиднои цепи1 5 10 15 в которой один или большее число аминокислотных остатков являются замещенными. Заместители в Хаа, Уаа и 2 аа, которые могут быть использованы, показаны ниже. Заместитель Остаток Нейтральные алифатические аминокислоты А 1 а, ЬА 1 а, Ьеи, Пе, (Ну,Уа 1, Ше, Муа Хаа Основные аминокислоты Ьуз, Агв, Ош, Нтз Уаа Кислые аминокислоты 6111, Азр, Ааа, Арт 2 аа Предпочтительными пептидами являются следующие е 3.1 а.Мо 1В соответствии с еще одной стороной изобретения предлагаются аналогичные пептиды с концевыми амидными или карбоксигруппами у концевых Сатомов, имеющие вышеупомянутую структурную формулу, в которой отсутствуют по крайней мере один и самое большее семь аминокислотных остатков с 1 по 15, и по крайней мере один из остальных аминокислотных остатков может быть замещен в соответствии с вышеприведенной схемой замещения.Предпочтительными пептидами являются следующиеВ СООТВСТСТВИИ С СЩС ОДНИМ вариантом ОСУЩССТВЛСНИЯ ИЗООРСТСНИЯ ПСПТИДЬ, ИМСЮЩИСописанные выше структурные формулы, в которых может быть пропущен по крайней мере один аминокислотный остаток и по крайней мере один из оставшихся аминокислотных остат КОВ МОЖСТ бЫТЬ замещен так, как УКЗЗЗНО ВЫШЕ, ПРОВОДЯТ В ЦИКЛИЧССКУЮ форму ПУТСМ образования НОВОЙ СВЯЗИМЗИСДУ первым И ПОСЛЕДНИМ ЗМИНОКИСЛОТНЫМ ОСТЗТКОМ В МОЛЕКУ ле. ПРСДПОЧТИТСЛЬНЫМИ пептидами ЯВЛЯЮТСЯ СЛСДУЮЩИСЗаявители обнаружили, что при применении вышеописанные пептиды показывают биологическую активность, равную или большую, чем активность основного белка ВРС.Проведены фармакологические исследования упомянутых пептидов на различных обычных моделях йп уйго и йп уйуо и обнаружены фармакологические свойства, перечисленные далее.Язва желудка, вызванная стрессом от неподвижности. В этих экспериментах используют белых крыс Легат (самцов) (180-200 г). Всех животных фиксируют в положении лежа на спине в течение 48 ч при комнатной температуре. Немедленно после этого животных умерщвляют и определяют размеры патологических изменений. Проводят обработку пептидами с последовательностями ЫЫ 4, 6 и 2 при дозировке 10 мкг или 10 нг на кг веса тела, 1.р. или 1.3., за 1 ч до причиняющей вред процедуры.Как при 1.5., так и при 1.р. введении даже такие маленькие дозы, как 10 нг/кг, оказывают сильное защитное деиствие.Гистаминная модель язвы. В этих экспериментах используют белых крыс Легат (самок)(180-200 г). Вводят подкожно гидрохлорид гистамина (растворенный в дист. воде) при дозировке 400 мг/кг веса тела. Через 24 ч животных умерщвляют. Пептиды с последовательностью Ы 4 вводят при дозировке 1,0 мкг, 100 нг и 50 нг на кг веса тела, 1.р. и 1.3. (внутрибрюшинно и внутрижелудочно). Получают сильную и зависящую от дозы защиту. Одинаковая активность обнаружена и при 1.р., и при внутрибрюшинном способе введения.Индуцированный скипидаром Щечный отек. Животные самцы крыс Легат (180-240 г),Ы 10 в каждой группе. Скипидар вводят внутримышечно, 0,02 мл на крысу. Контрольный раствор 0,9 физиологический, внутримышечно (0,02 мл на крысу, 2 х). Пептиды с последовательностями ЫЫ 2 и 4 применяют при дозах 10 мкг и 10 нг/кг, 1.р. и 1.3. вводят за 1 ч перед введением скипидара. Щечный отек замеряют через 24 ч после индуцирования отека. Статистический анализ Мапп-Шшшеу. Исследованные пептиды эффективны при дозе 10 мкг/кг веса тела.Хирургия действие на резаные раны кожи. В этих экспериментах используют самцов белых крыс (10 для каждого эксперимента, вес тела 200-250 г). Крыс с ранами кожи держат каждую отдельно в отдельных клетках. На коже спины каждого животного под легкой эфирной анестезией размещают параллельно разрезы (3 см) на расстоянии 1,5 см от средней линии спины. Края одной раны затем сближают двумя хирургическими скобками, а другую оставляют необработанной. Сразу же после повреждения между ранами внутридермально вводят пептид с последовательностью Ы 4, растворенный в физиологическом растворе, при дозах 1,0 мкг и 1,0 нг/кг веса тела или физиологический раствор - в контрольной группе, при дозе 0,5 мл/кг.Отчетливое заживляющее действие исследуемого пептида было очевидно на тех и других ранах - как на ранах, стянутых скобками, так и на ранах, оставшихся без хирургической обработки. Через 5 дней обработанная группа показывает меньшее число воспалительных клеток и существенно лучше развитые ретикулярные волокна, чем контрольная группа.Действие на опытные ожоги. В этом эксперименте используют самцов белых крыс, линия Нэгаг (Ы 10, вес тела 200-250 г). При легкой эфирной анестезии прижигают слизистую оболочку носа в течение 5 с. За 1 ч до нанесения травмы применяют пептид с последовательностью Ы 4 при дозе 10 мкг/кг веса тела, ьр. Контрольная группа 5,0 мл/кг веса тела физиологического раствора, 1.р. Проведенная процедура обычно дает значительное вздутие морды и постоянно становится смертельной для животных контрольной группы (но не для животных прошедших лечение) в течение девяти дней после нанесения ран. В противоположность контрольным животным у обработанных наблюдается только очень незначительная припухлость морды. Затем носовое нормальное дыхание оказывается только слегка нарушенным и спокойно восстанавливается.Действие при лечении переломов. В этих экспериментах используют самцов белых крыс линии Штат (270-300 г - вес тела). Под эфирным наркозом ломают руками левые большеберцовые кости в средней части. Иммобилизацию не проводят, и животным позволяют свободно передвигаться по клеткам. Животных умерщвляют на 5-й, 8-й, 12-й и 30-й день после нанесения травм.Пептид с последовательностью Ы 4 дают при дозировке 10,0 мкг/кг веса тела, 1.р., за 1 ч до нанесения травмы и затем один раз в день (последнее введение - за 24 ч перед умерщвлением). Контрольной группе в то же время вводят эквиобъемное количество физиологического раствора (0,9 , 5,0 мл/кг веса тела, 1.р.). Существенное увеличение скорости заживления отмечают у всех обработанных пептидом животных в каждом интервале, в котором проводят исследования. Примечательно, что все обработанные пептидом животные устойчиво показывают более слабую местную постгравматическую гематому, чем контрольные животные, и они восстанавливают свои поврежденные функции значительно быстрее.Противовирусную активность исследуют на новорожденных - в возрасте 24 ч - мышах линии ВАЬВ-С обоего пола.Используют вирусы АКВО-ТВЕ ( клещевой. энцефалит), Вйаша денге 1, 2, 3, 4, 51111313,саг-Мне, Са 1 оуо гепатита А, ЬСМ (лимфатический хориоменингит) и герпеса типа 1 в виде суспензии вируса при разбавлении 104 (0,02 мл/мышь), полученной так, как обычно принято,и введенной 1.0. или р.о. (гепатит А). С учетом различия в вирулентности ДОЗЫ подбирают таким образом, чтобы можно было проводить сравнение Люд в 0,02 мл инокулята, 1.0. (или р.о.,гепатит А), при разбавлении 104. В этом случае мы можем сравнивать ход заражения различными вирусами без учета возможной инокуляции вирусами различной концентрации.Пептид с последовательностью М 4 используют при концентрации 20,0 мкг/мл в 0,9 физиологическом растворе и вводят только в виде одной дозы - 2,0 мкг/кг веса тела - 1.с. или 1.р.а) за 2 ч до применения вируса (-211)Контрольная группа такой же объем физиологического раствора 1.0. или 1.р. Результаты сведены в табл. 1.Числа в табл. 1 указывают период (дни) до того времени, когда погибают мыши, инфицированные всеми вирусами, в группах, обработанных пептидом или физиологическим раствором (контрольные).Антидепрессионная активность. Для обнаружения антидепрессионной активности проводят испытания Гогсес вшйттйпв по Рогзоп е а 1., Еиг.1.Р 11 агшасоЬ., 47, 379-391, 1978.Для этого эксперимента берут самцов крыс Шйзсаг (вес тела 180-240 г). Исследуемый пептид с последовательностью Ы 4 дают накануне испытания и в день испытания за один час до эксперимента (1.р.).Контрольная группа физиологический раствор, 1.р.Животных наблюдают в течение 5 мин. Измеряют время неподвижности (ТЕ).Величина Т 1 в контрольной группе составляет около 150 с, в группе, обработанной пептидом, - только 60-70 с. Этот эффект является длительным он еще присутствует через 16 дней.Доза отклика 10 мкг - 10 нг/кг полный эффект 10 пг/кг эффект еще присутствует 1 пг/кг эффект исчезает.Действие на модель болезни Паркинсона. Для исследований используют хорошо известные модели болезни Паркинсона (Кагако 1 а 5. е а 1., Рпагшасо 1. Тох 1 со 1., 67, 95-100, 1990) резерпиновую модель И МРТР-модель.Используют самцов мышей ЫМШ-Наппоуег (для МРТР-модели) или обоих полов (для резерпиновой модели).МРТР применяют при дозировке мг/кг веса тела, 1.р., один раз в день в течение Шести дней подряд, и затем в течение следующих четырех дней - при более высокой дозе 50 мг/кг. Исследуемый пептид с последовательностью М 4 вводят при дозировке 1,5 мкг и 15,0 нг/кг веса тела 1.р., за 15 мин до каждого введения МРТР или через 15 мин после каждого введения МРТР.Резерпин используют при дозировке 5 мг/кг веса тела, 1.р. Испытуемый пептид применяют при дозе 10 мкг или 10 нг/кг веса тела, 1.р., за 15 мин до введения резерпина или через 24 ч после введения резерпина, в той же дозе.Контрольная группа равный объем физиологического раствора, 5 мл/кг веса тела, 1.р.После предшествующей обработки пептидом наблюдают существенное сокращение гипокинезии, ригидности (каталепсии) и тремора.В МРТР-модели предварительная обработка пептидом отчетливо уничтожает развитие каталепсии и уменьшает акинезию и появление тремора. Последующая обработка (через 15 мин) существенно предотвращает дальнейшее развитие МРТР-каталепсии и заметно уменьшает акинезию и тремор. Обычно высокая смертность (50 ) отмечается после введения только одного МРТР и уменьшается у животных, обработанных пептидом как при предшествующей, так и при последующей обработках.Действие введения пептида при геморрагическом шоке. Во всех экспериментах используют взрослых самок белых крыс линии Штат (150-180 г).Действие при геморрагическом шоке исследуют в двух сериях экспериментов.а) Животным пускают кровь (1 мл за 3 мин, 2 мин пауза) до тех пор, пока не наступит смерть. Оценивают удаленный объем крови, приводящий к летальному исходу, у животных,обработанных пептидом с последовательностью Ы 4 (10,0 мкг или 10 нг/кг веса тела, 1.р.) или физиологическим раствором (5,0 мл/кг веса тела, 1.р.), обработка проводится за 15 мин до начала кровопускания, В группе, обработанной более высокой дозой пептида, постоянно отме
МПК / Метки
МПК: A61K 38/12, A61K 38/08, A61K 38/10, C07K 7/06
Метки: основе, композиция, фармацевтическая, органозащитной, пептиды, активностью
Код ссылки
<a href="https://by.patents.su/11-3553-peptidy-s-organozashhitnojj-aktivnostyu-farmacevticheskaya-kompoziciya-na-ih-osnove.html" rel="bookmark" title="База патентов Беларуси">Пептиды с органозащитной активностью, фармацевтическая композиция на их основе</a>