Способ выявления сенсибилизации у лабораторных животных к ксенобиотикам
Номер патента: 4819
Опубликовано: 30.12.2002
Авторы: Шевляков Виталий Васильевич, Буйницкая Анна Васильевна, Эрм Галина Ивановна, Ушков Александр Александрович
Текст
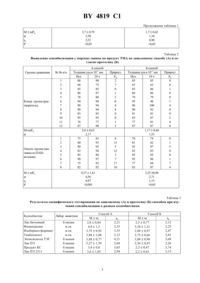
НАЦИОНАЛЬНЫЙ ЦЕНТР ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ СПОСОБ ВЫЯВЛЕНИЯ СЕНСИБИЛИЗАЦИИ У ЛАБОРАТОРНЫХ ЖИВОТНЫХ К КСЕНОБИОТИКАМ(73) Патентообладатель Государственное учреждение Научно-исследовательский институт санитарии и гигиены(57) Способ выявления сенсибилизации у лабораторных животных к ксенобиотикам путем воздействия на ухо сенсибилизированным животным провокационной разрешающей дозой изучаемого вещества и определения степени опухания уха, отличающийся тем, что провокационную дозу вводят в ухо внутрикожно и по разнице в толщине уха после и до тестирования судят о сенсибилизирующих свойствах ксенобиотиков.(56)2094800 1, 1997.2094801 1, 1997.2094855 1, 1997.2094856 1, 1997. Изобретение относится к медицине, а именно к области экспериментальной аллергологии и токсикологии. Известен способ выявления сенсибилизации в экспериментах на лабораторных мышах к химическим веществам 1 (аналог), который заключается во введении провокационной разрешающей дозы изучаемого вещества в подушечку (под апоневроз) задней лапы предварительно сенсибилизированным этим веществом животным с оценкой развития гиперчувствительности замедленного типа по степени отека лапы, определяемой по разнице толщины опытной (вещество) и контрольной (растворитель) лап. Недостатками данного способа являются невысокая чувствительность вследствие неполноценных условий в тканях апоневроза лап для реализации гиперергического воспаления (малоразветвленная сеть лимфо- и кровоснабжения, отдаленность периферических лимфоузлов),значительная вероятность ошибок в измерениях толщины лап в результате мягкости и подвижности тканей подушечки и морфо-анатомических различий лап у одного и того же животного, т.е. не обеспечивается объективность результатов. Известен способ выявления в экспериментах на мышах сенсибилизации по гиперчувствительности замедленного типа (ГЗТ) к химическим веществам 2 (прототип). Способ заключается в оценке выраженности индукции ГЗТ по степени опухания уха мышей (тест опухания уха - ТОУ), регистрируемой измерением толщины уха после постановки провокационной кожной пробы - нанесение на кожу уха разрешающей дозы вещества, которым предварительно сенсибилизированы животные. К недостаткам известного способа относится его недостаточная чувствительность и точность. Это обусловлено тем, что многие испытуемые вещества обладают слабой трансдермальной проникающей способностью, а при нанесении кожных проб с растворами веществ значительная их часть теряется вследствие стекания с поверхности уха, остаточных количеств в дозаторах и на пипетках. В результате этого количество проникающего через кожу веществасенсибилизатора недостаточно для индукции аллергической воспалительной реакции, что может приводить к неверным выводам - об отсутствии у этих веществ сенсибилизирующей способности. К тому же проводится измерение и сравнение толщины колатеральных ушей животных с опытной (вещество) и контрольной(растворитель) кожными пробами, что вследствие морфо-анатомических различий ушей у того же животного может приводить к некорректным результатам. Задачей настоящего изобретения является повышение чувствительности, точности и упрощение способа. Поставленная задача достигается следующим образом. Предложен способ выявления сенсибилизации у лабораторных животных к ксенобиотикам путем воздействия на ухо сенсибилизированным животным провокационной разрешающей дозой изучаемого вещества и определения степени опухания уха, когда провокационную дозу вводят в ухо внутрикожно и по разнице в толщине уха после и до тестирования судят о сенсибилизирующих свойствах ксенобиотиков. Статистически достоверное по критериюСтьюдента (при Р 0,05) возрастание средней величины показателя ТОУ в опытной группе животных по сравнению с контрольной свидетельствует об индукции ГЗТ и позволяет оценить изучаемый ксенобиотик как потенциальный аллерген. Статистическая недостоверность сравниваемых среднегрупповых показателей ТОУ указывает на отсутствие сенсибилизирующей активности у вещества. С использованием предлагаемого способа и описанного в прототипе оценены сенсибилизирующие свойства ряда химических веществ. В табл. 1 и 2 приведены результаты оценки чувствительности способов на примере вытяжки из ПАН-волокна Нитрон С и терпено-малеинового аддукта (ТМА) соответственно на белых мышах и морских свинках. У сенсибилизированных вытяжкой из ПАН-волокна мышей среднегрупповые показатели ТОУ в опыте и контроле при эпикутанном провокационном тестировании (прототип) были статистически недостоверны (0,9), тогда как при внутрикожном тестировании разница была существенна(2,52, Р 0,05). Наличие сенсибилизации подтверждалось и достоверными уровнями клеточноопосредованной гипериммунной реакцией- реакцией специфического лейколизиса (РСЛЛ) в контрольной группе - 2,511,15 и в опытной - 7,411,56(2,7, Р 0,02). Аналогично заявляемым способом выявлена сенсибилизирующая активность продукта ТМА на морских свинках (табл. 2), что подтверждалось и высокими уровнями положительных аллергодиагностических реакций, тогда как по способу прототипа результаты были недостоверные. В то же время при установлении на животных сенсибилизирующей способности у изучаемых ксенобиотиков способом прототипа среднегрупповые показатели ТОУ и значения критерияпо сравнению с соответствующими контрольными группами заявляемым способом были более высокими и значимыми (табл. 3). Таблица 1 Выявление сенсибилизации у белых мышей на вытяжку из ПАН-волокна Нитрон С по заявленному способу (А) и согласно прототипу (Б) Группы сравнения Таблица 2 Выявление сенсибилизации у морских свинок на продукт ТМА по заявленному способу (А) и согласно прототипу (Б) Группы сравнения Таблица 3 Результаты специфического тестирования по заявляемому (А) и прототипу (Б) способам при изучении сенсибилизации к разным ксенобиотикам Ксенобиотик Лак битумный Фенантралин Изоборнил-формиат Тиабендазол Эпоксисмола ТЭГ Лак ПЭ Продукт КС Лак ПЭ 2311 4819 1 Сущность изобретения заключается в следующем. По предлагаемому способу разрешающая доза химического вещества, которым сенсибилизированы лабораторные животные (мыши, крысы, морские свинки),вводится внутрикожно в строго необходимом количестве в чувствительную зону уха, чем достигается точная дозировка и оптимальные условия для реализации вторичного клеточного иммунного ответа в форме гиперергического аллергического воспаления по замедленному типу с развитием отека тканей. По величине разницы в толщине того же уха после и до внутрикожного тестирования животных судят о степени отека и соответственно о выраженности индуцированной ГЗТ. В прототипе же разрешающая провокационная доза вещества наносится на поверхность уха мышей с измерением толщины колатеральных ушей с опытной и контрольной кожными пробами и оценкой величины их разницы. Заявляемый способ осуществляется следующим образом. Опытным (сенсибилизированным известными способами испытуемым химическим веществом) и контрольным (растворитель) лабораторным животным в срединный сегмент наружной поверхности уха внутрикожно вводится микро-или туберкулиновым шприцом в объеме по 40-60 мкл раствора (вытяжки) испытуемого вещества в расчетной концентрации, соответствующей сенсибилизирующей дозе. До введения и через 24 часа после него инженерным микрометром измеряют толщину уха с точностью до 0,01 мм. По разнице (приросту) величин толщины уха в 10-2 мм после и до тестирования определяют степень опухания уха у животного - показатель ТОУ. О выраженности ГЗТ и наличии сенсибилизирующих свойств у испытуемого ксенобиотика судят по статистическому различию по критериюСтьюдента среднегрупповых показателей ТОУ в опыте и контроле. При статистически достоверных различиях при Р 0,05 ксенобиотик является потенциальным аллергеном, при отсутствии - не обладает сенсибилизирующей активностью. Технический результат заявляемого способа повышение чувствительности выявления сенсибилизации к ксенобиотикам за счет элиминации влияния физико-химических свойств вещества и его трансдермальной проникающей способности, оптимальных условий при внутрикожном введении вещества для быстрой реализации клеточного гиперергического иммунного ответа с развитием воспаления повышение точности исследования вследствие строго определенного количества вводимой разрешающей дозы вещества, измерения степени отека одного и того же уха животного упрощение исследования, так как исключается необходимость постановки теста с растворителем испытуемого вещества на колатеральное ухо животных. Способ промышленно применим в медицине, в частности в аллергологии и токсикологии. Источники информации 1. Черноусов А.Д. Метод определения аллергенной активности низкомолекулярных химических веществ на мышах//Гигигена труда. -1987. -6. - С. 45-47. 2.,,,.//.. . -1986. - . 84. -1. - . 93-114 (прототип). Национальный центр интеллектуальной собственности. 220072, г. Минск, проспект Ф. Скорины, 66. 4
МПК / Метки
МПК: G09B 23/28
Метки: способ, лабораторных, животных, ксенобиотикам, выявления, сенсибилизации
Код ссылки
<a href="https://by.patents.su/4-4819-sposob-vyyavleniya-sensibilizacii-u-laboratornyh-zhivotnyh-k-ksenobiotikam.html" rel="bookmark" title="База патентов Беларуси">Способ выявления сенсибилизации у лабораторных животных к ксенобиотикам</a>
Предыдущий патент: Способ переработки кубового остатка производства диметилтерефталата
Следующий патент: Коллектор доильного аппарата
Случайный патент: Измельчитель