Составы эстрамустина с улучшенными фармацевтическими свойствами
Номер патента: 5206
Опубликовано: 30.06.2003
Авторы: Джованни БУЦЦИ, Джузеппе КОЛОМБО, Джузеппе МАККАРИ, Лорена МУДЖЕТТИ, Алессандро МАРТИНИ
Текст
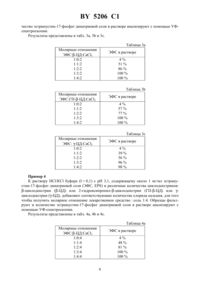
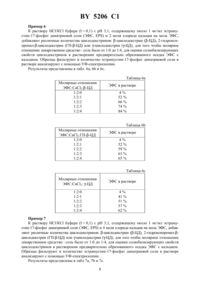
47/40,61 35/00 НАЦИОНАЛЬНЫЙ ЦЕНТР ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ(71) Заявитель ФАРМАЦИЯ ЭНД АПДЖОН АБ(72) Авторы Алессандро МАРТИНИ Джузеппе МАККАРИ Лорена МУДЖЕТТИ Джузеппе КОЛОМБО Джованни БУЦЦИ(73) Патентообладатель ФАРМАЦИЯ ЭНД АПДЖОН АБ(57) 1. Фармацевтическая композиция для перорального применения, содержащая производное эстрамустина и циклодекстрин при их молярном соотношении 1(0,5-10,0), причем в качестве производного эстрамустина она содержит эстрамустин-17-фосфат или эстрамустин-17-фосфата динатриевую соль. 2. Фармацевтическая композиция по п. 1, отличающаяся тем, что циклодекстрин является -циклодекстрином, -циклодекстрином, -циклодекстрином, частично этерифицированным -циклодекстрином, диметилциклодекстрином или дегидратированным циклодекстрином. 3. Фармацевтическая композиция по п. 2, отличающаяся тем, что циклодекстрин является -циклодекстрином. 4. Фармацевтическая композиция по п. 2, отличающаяся тем, что циклодекстрин является гидроксипропилциклодекстрином. 5. Фармацевтическая композиция по п. 2, отличающаяся тем, что циклодекстрин является -циклодекстрином. 6. Фармацевтическая композиция по п. 2, отличающаяся тем, что циклодекстрин является дегидратированным циклодекстрином. 7. Фармацевтическая композиция по любому из пп. 1-6, отличающаяся тем, что дополнительно содержит фармацевтически приемлемый носитель или разбавитель. 8. Фармацевтическая композиция по любому из пп. 1-7, отличающаяся тем, что предназначена для лечения опухоли. 9. Применение циклодекстрина в качестве ингибитора осаждения производного эстрамустина в желудочно-кишечном тракте при получении лекарственного препарата для перорального введения, содержащего фармацевтическую композицию по любому из пп. 1-8. 10. Применение циклодекстрина по п. 9, отличающееся тем, что лекарственный препарат используется для лечения опухоли. 5206 13299104, 1967., 12 , 1996, 3749.0477107 1, 1992.0351561 , 1990. Данное изобретение относится к фармацевтическим композициям, содержащим производное эстрамустина и циклодекстрин. Циклодекстрины здесь и ниже ЦД- хорошо известные олигосахариды, состоящие из -глюкозных остатков, имеющие структуру с цилиндрической пустотой, способную включать различные гостевые молекулы. В самом деле, одно из самых интересных свойств ЦД заключается в их особенности образовывать включения или комплексы. Это взаимодействие сильно зависит от гидрофобности молекулы гостя, пространственного затруднения между лекарственным средством и ЦД и размера ЦД полости. Так или иначе,этот тип комплексообразования придает новые физико-химические свойства лекарственным средствам, и его интенсивно используют в фармацевтической области для улучшения растворимости и стабильности активных лекарственных веществ О..,. . ., 17, 1503 (1991) ., . . .,1991, 15 и, как следствие, их характеристик растворения и биодоступности. Более обычно, комплексообразованное лекарственное средство - ЦД используют для улучшения биодоступности активных молекул, имеющих очень низкую растворимость в воде, но хорошую скорость абсорбции (всасывания) через биологические мембраны ..,, 323 (1985). Указанные комплексы включения обычно получают в жидкой среде, и затем, после высушивания, их получают в форме порошка. Пригодны различные способы получения твердых соединений включения, такие как смешение К.., . . ., 10, 1 (1982), соосаждение К.., .(1989), сушка-замораживанием Р.., Патент США 4 603 123, 29 июля (1986). В некоторых случаях образование комплекса в твердой фазе является термодинамически самопроизвольным и включение обычно может быть достигнуто путем растирания С.., . . ., 71,19 (1991). Нами неожиданно обнаружено, что характеристики биодоступности некоторых лекарственных средств могут быть еще улучшены с помощью ЦД также для молекул с высокой растворимостью в воде, что теоретически не требует какого-либо конкретного подхода, в частности, предназначенного для улучшения их растворимости или их скорости растворения из терапевтической лекарственной формы. Данное изобретение относится к фармацевтической композиции, содержащей производное эстрамустина и циклодекстрина. Производные эстрамустина, в соответствии с изобретением, являются, например, соединения формулы где 1 представляет (С 1-С 4)-алкил иравно 0, 1 или 2, и фармацевтически приемлемые соли. Особенно предпочтительными производными эстрамустина являются соединения формулы 1, где,метансульфонатная соль, т.е. эстрамустин-17 аланинат метансульфонат. Эстрамустин-17-фосфат динатриевая соль (пат. Великобритании 1 016 959) является лекарственный средством, используемым при опухоли простаты, наиболее широко при лечении пациентов, которых нельзя далее лечить гормонами, и пациентов с плохим прогнозом. Лекарственное средство применяется для всех пациентов, у которых болезнь распространилась через метастатические опухоли. По мере того как опухоль уменьшается,боль, вызываемая опухолью, также ослабевает. Несмотря на эффективность при лечении и способность к всасыванию через желудочно-кишечную стенку, эстрамустин-17-фосфат динатриевая соль имеет сильные ограничения при пероральном введении вследствие его взаимодействия с пищей и питьем необходимо вводить лекарственный препарат натощак для того, чтобы избежать повторного осаждения лекарственного препарата, которое вызывается катионами и, в частности, ионами кальция ., . . .., 38, 189 (1990). Этот факт существенно понижает биодоступность лекарственного средства и вызывает побочные эффекты в желудочно-кишечном тракте. Эстрамустин-17 аланинат (патентная заявка ЕР 351561) имеет те же самые терапевтические показания, что и эстрамустин-17-фосфат динатриевая соль, и ему присущ тот же самый недостаток, связанный с переосаждением, но вызываемым анионами, такими как ионы хлора. Данное изобретение, главным образом, относится к использованию любого ЦД, природного (-ЦД, -ЦД и -ЦД), синтетического или полусинтетического (как, например,гидроксипропилЦД или диметилЦД) или дегидратированного .., патент США 5 126 333, 30 июня (1992). В частности, предпочтительными циклодекстринами являются -циклодекстрин, гидроксипропилциклодекстрин и -циклодекстрин. Авторами неожиданно было обнаружено, что когда циклодекстрины смешивают с эстрамустин-17-фосфат динатриевой солью, растворимость лекарственного средства сама по себе существенно не изменяется, но эффекты повторного осаждения лекарственного средства, вызываемого катионами, совсем незначительны, поскольку циклодекстрины способны загородить участок взаимодействия эстрамустин-17-фосфата с кальцием или другими катионами. Образование комплекса в растворе между лекарственным средством и соответствующим циклодекстрином может предотвратить повторное осаждение свободного лекарственного средства или соли лекарственного средства в физиологических условиях. 5206 1 Это явление может иметь большое преимущество при введении лекарственного средства, делая его биодоступность более высокой независимо от условий пустого/не пустого желудка. Циклодекстрины неожиданно оказались способными не только предотвращать повторное осаждение эстрамустин-17-фосфата в присутствии катионов, но, кроме того, позволять поступать в раствор лекарственному средству, когда, например, ионы кальция присутствуют в среде растворения, и повторно растворять уже образованный осадок эстрамустин-17-фосфата с кальцием. Показано, что циклодекстрины взаимодействуют с эстрамустин-17 аланинатом,предотвращая повторное осаждение различными видами анионов. Кроме того, необходимо обратить внимание на то, что для этого применения нет необходимости получать комплекс между лекарственным средством и циклодекстрином в твердом состоянии, а достаточно ввести простую физическую смесь из двух химических компонентов. Соотношение между лекарственным средством и циклодекстрином может варьироваться, например, от 10,5 до 110 (молярное соотношение). Предпочтительное молярное соотношение составляет от 11 до 14. Подходящий диапазон составляет от 11 до 12. Фармацевтический состав, содержащий композицию согласно изобретению лекарственное средство - циклодекстрин, которая входит в объем изобретения, может быть получен следующими известными и обычными способами. Предлагаемая система лекарственное средство - циклодекстрин может быть использована для получения твердого, полутвердого или жидкого составов для пероральных лекарственных форм, например таблеток, твердых или мягких желатиновых капсул, саше и т.д., с добавлением или без добавления одного или более наполнителей, обычно используемых для фармацевтических составов. Могут присутствовать фармацевтически приемлемые носители или разбавители. Доза зависит от возраста, веса, состояний пациента и способа введения. Например, доза, предназначенная для перорального введения людям, составляет от 50 до 1500 мг ежедневно. Данное изобретение относится также к фармацевтической композиции, указанной выше, для использования в способе лечения человека или животного с помощью терапии,в частности для лечения опухоли. Данное изобретение также относится к применению циклодекстрина при получении лекарственного препарата, пригодного для перорального введения производного эстрамустина пациенту, причем указанный лекарственный препарат содержит производное эстрамустина и циклодекстрин, и к применению циклодекстрина при получении лекарственного препарата для лечения опухоли, причем лекарственный препарат содержит производное эстрамустина и циклодекстрин. Композиция по настоящему изобретению может быть использована в способе лечения или предотвращения опухоли, который включает введение субъекту, страдающему от нее или предрасположенному к ней, эффективного количества композиции. Следующие примеры представлены только с целью лучшей иллюстрации данного изобретения, но их не следует рассматривать как ограничивающие объем изобретения. Пример 1 К раствору НС/КС буфера (0,1) с рН 3,1, содержащему 640 мкг/мл эстрамустин 17-фосфат динатриевой соли (ЭФС, ), добавляют соответствующие количества хлорида кальция, для того чтобы достигнуть молярное отношение лекарственное средствосоль в интервале от 10 до 11. Образцы фильтруют и количество эстрамустин-17-фосфат динатриевой соли в растворе анализируют с помощью УФ-спектроскопии. Результаты приведены в табл. 1. 5206 1 Таблица 1 Молярные отношения ЭФССаС 2 10 1 0,25 10,5 1 1-циклодекстрин (-ЦД), 2-гидроксипропилциклодекстрин (ГПЦД) или -циклодекстрин (-ЦД), добавляют соответствующие количества хлорида кальция, для того чтобы молярное отношение лекарственное средствосоль было 11. Образцы фильтруют и количество эстрамустин-17-фосфат динатриевой соли в растворе анализируют с помощью УФ-спектроскопии. Результаты представлены в табл. 2 а, 2 и 2 с. Таблица 2 а Молярные отношения ЭФС в растворе ЭФС-ЦДСаС 2 101 16111 52121 90131 100141 100 Таблица 2 Молярные отношения ЭФСГПЦДСаС 2 101 111 121 131 141 Молярные отношения ЭФС -ЦДСаС 2 101 111 121 131 141-циклодекстрин (-ЦД), 2-гидроксипропилциклодекстрин (ГПЦД) или -циклодекстрин (-ЦД), добавляют соответствующие количества хлорида кальция, для того чтобы получить молярное отношение лекарственное средствосоль 12. Образцы фильтруют и коли 5 Молярные отношения ЭФС -ЦДСаС 2 102 112 122 132 142-циклодекстрин (-ЦД) или 2-гидроксипропилциклодекстрин (ГПЦД) или циклодекстрин (-ЦД), добавляют соответствующие количества хлорида кальция, для того чтобы получить молярное отношение лекарственное средствосоль 14. Образцы фильтруют и количество эстрамустин-17-фосфат динатриевой соли в растворе анализируют с помощью УФ-спектроскопии. Результаты представлены в табл. 4 а, 4 и 4 с. Таблица 4 а Молярные отношения ЭФС-ЦДСаС 2 104 114 124 134 144 Пример 5 К раствору НС/КС буфера (0,1) с рН 3,1, содержащему около 1 мг/мл эстрамустин-17-фосфат динатриевой соли (ЭФС, ) и 1 моль хлорида кальция на моль ЭФС,добавляют различные количества циклодекстринов -циклодекстрин (-ЦД), 2-гидроксипропилциклодекстрин (ГПЦД) или -циклодекстрин (-ЦД), для того чтобы получить молярное отношение лекарственное средствосоль от 10 до 14, для оценки солюбилизирующих свойств циклодекстринов в растворении предварительно образованного осадка ЭФС с кальцием. Образцы фильтруют и количество эстрамустин-17-фосфат динатриевой соли в растворе анализируют с помощью УФ-спектроскопии. Результаты представлены в табл. 5 а, 5 и 5 с. Таблица 5 а Молярные отношения ЭФС в растворе ЭФССаС 2-ЦД 110 16112 77113 83114 95 Таблица 5 Молярные отношения ЭФССаС 2 ГПЦД 110 112 113 114 Молярные отношения ЭФССаС 2 -ЦД 110 112 113 114 5206 1 Пример 6 К раствору НС/КС буфера (0,1) с рН 3,1, содержащему около 1 мг/мл эстрамустин-17-фосфат динатриевой соли (ЭФС, ) и 2 моля хлорида кальция на моль ЭФС,добавляют различные количества циклодекстринов -циклодекстрин (-ЦД), 2-гидроксипропилциклодекстрин (ГПЦД) или -циклодекстрин (-ЦД), для того чтобы молярное отношение лекарственное средствосоль было от 10 до 14, для оценки солюбилизирующих свойств циклодекстринов в растворении предварительно образованного осадка ЭФС с кальцием. Образцы фильтруют и количество эстрамустин-17-фосфат динатриевой соли в растворе анализируют с помощью УФ-спектроскопии. Результаты представлены в табл. 6 а, 6 и 6 с. Таблица 6 а Молярные отношения ЭФССаС 2-ЦД 120 121 122 123 124 Молярные отношения ЭФССаС 2 ГПЦД 120 121 122 123 124 Молярные отношения ЭФССаС 2 -ЦД Пример 7 К раствору НС/КС буфера (0,1) с рН 3,1, содержащему около 1 мг/мл эстрамустин-17-фосфат динатриевой соли (ЭФС, ) и 4 моля хлорида кальция на моль ЭФС, добавляют различные количества циклодекстринов -циклодекстрин (-ЦД), 2-гидроксипропил-циклодекстрин (ГПЦД) или -циклодекстрин (-ЦД), для того чтобы молярное отношение лекарственное средствосоль было от 10 до 14, для оценки солюбилизирующих свойств циклодекстринов в растворении предварительно образованного осадка ЭФС с кальцием. Образцы фильтруют и количество эстрамустин-17-фосфат динатриевой соли в растворе анализируют с помощью УФ-спектроскопии. Результаты представлены в табл 7 а, 7 и 7 с. 8 5206 1 Таблица 7 а Молярные отношения ЭФССаС 2-ЦД 140 141 142 143 144 Молярные отношения ЭФССаС 2 ГПЦД 140 141 142 143 144 Молярные отношения ЭФССаС 2 -ЦД Пример 8 Тест на скорость растворения проводили сравнивая характеристики уже продаваемого,свободного циклодекстрина, состава эстрамустин-17-фосфат динатриевой соли и состава, содержащего эстрамустин-17-фосфат динатриевая сольгидроксипропилциклодекстрин(ЭФС/ГПЦД) в молярном соотношении 12. Условия соответствовали тесту на скорость растворения. (способ корзины) в погруженных состояниях, 37 С, 100 об/мин,НС/КС буфер рН 3,1 (0,1) с 1 молем хлорида кальция в среде растворения на моль лекарственного средства. Результаты показаны в табл. 8. Пример 9 Тест на скорость растворения проводили сравнивая характеристики различных составов эстрамустин-17-фосфат динатриевой соли (ЭФС), содержащих различные циклодекстрины -циклодекстрин (-ЦД), 2-гидроксипропилциклодекстрин (ГПЦД), -циклодекстрин (-ЦД) или дегидратированныйциклодекстрин (деЦД) в молярном отношении 12 с лекарственным средством. Условия соответствовали тесту на скорость растворения(0,1) с 1 молем хлорида кальция в среде растворения на моль лекарственного средства. 9 Процент в растворе ЭФСЦД молярное отношение с Пример 10 Тест на скорость растворения проводили сравнивая характеристики различных составов эстрамустин-17-фосфат динатриевой соли (ЭФС), содержащих различные циклодекстрины -циклодекстрин (-ЦД) или 2-гидроксипропилциклодекстрин (ГПЦД) в 12 молярном отношении с лекарственным средством. Условия соответствовали тесту на скорость растворения. (способ корзины) в погруженных состояниях, 37 С, 100 об/мин, НС/КС буфер рН 6,8 (0,1) с 1 молем хлорида кальция в среде растворения на моль лекарственного средства. Результаты показаны в табл. 10. Таблица 10 Время (минуты) 30 Процент в растворе ЭФСЦД молярное отношение с Пример 11 Тест на скорость растворения проводили сравнивая характеристики различных составов эстрамустин-17-фосфат динатриевой соли (ЭФС), содержащих различные циклодекстрины -циклодекстрин (-ЦД) или 2-гидроксипропилциклодекстрин (ГПЦД) в 12 молярном отношении с лекарственным средством. Условия соответствовали тесту на скорость растворения. (способ корзины) в погруженных состояниях, 37 С, 100 об/мин, НС/КС буфер рН 3,1 (0,1) с 5 молями хлорида кальция в среде растворения на моль лекарственного средства. Результаты показаны в табл. 11. Таблица 11 Процент в растворе ЭФСЦД молярное отношение с Национальный центр интеллектуальной собственности. 220034, г. Минск, ул. Козлова, 20. 10
МПК / Метки
МПК: A61K 47/40, A61K 31/565, A61P 35/00, A61K 47/48
Метки: свойствами, составы, фармацевтическими, улучшенными, эстрамустина
Код ссылки
<a href="https://by.patents.su/10-5206-sostavy-estramustina-s-uluchshennymi-farmacevticheskimi-svojjstvami.html" rel="bookmark" title="База патентов Беларуси">Составы эстрамустина с улучшенными фармацевтическими свойствами</a>
Предыдущий патент: Инсектицидная композиция, способ борьбы с термитами
Следующий патент: Тиски слесарные
Случайный патент: Устройство для измерения сопротивления изоляции электрических сетей постоянного тока