Бинарная инсектицидная композиция
Номер патента: 11593
Опубликовано: 28.02.2009
Авторы: Петкевич Сергей Константинович, Золотарь Ромуальда Михайловна, Нечай Наталья Ивановна, Гончарук Виолетта Михайловна, Поткин Владимир Иванович, Быховец Анатолий Иосифович
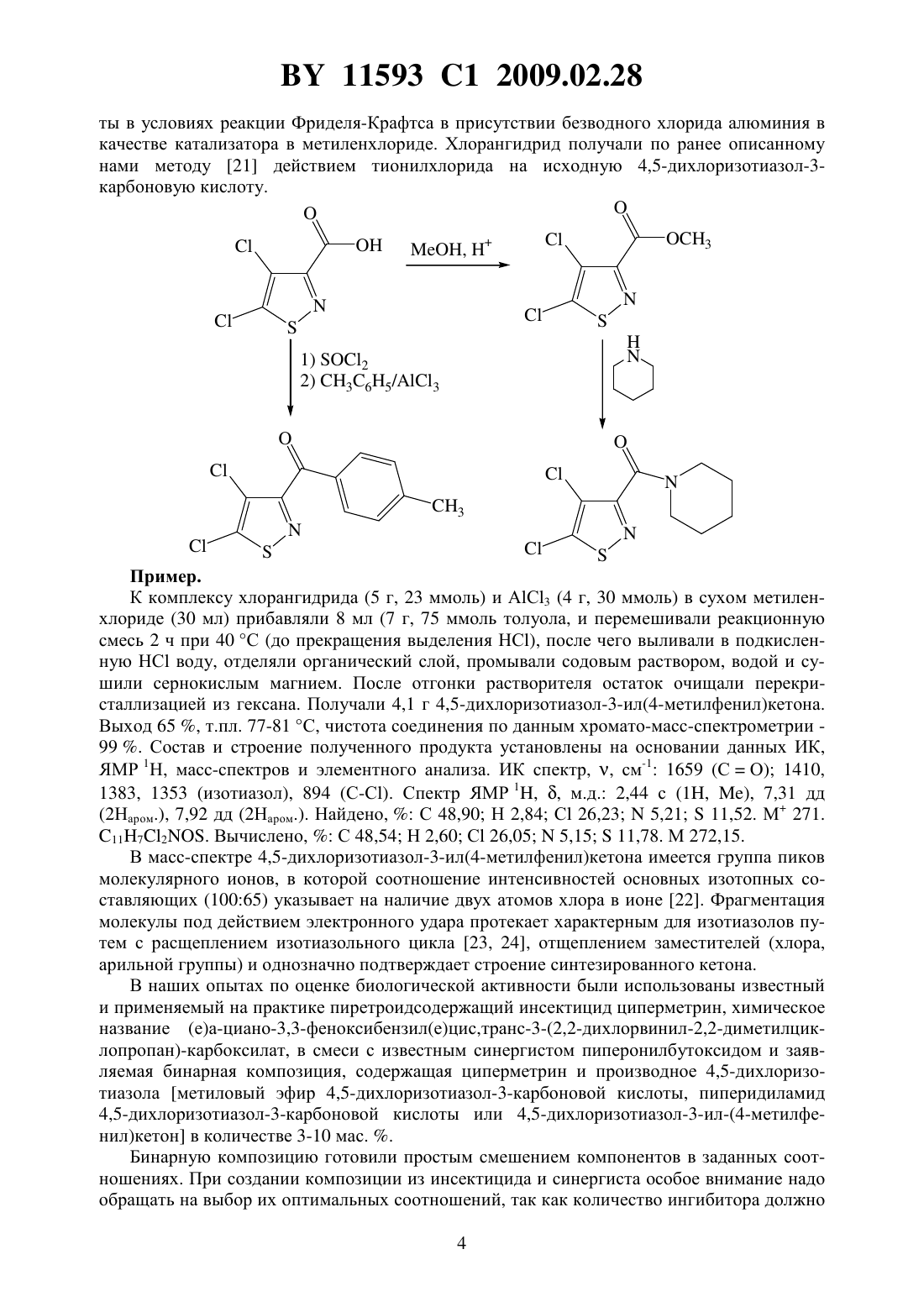
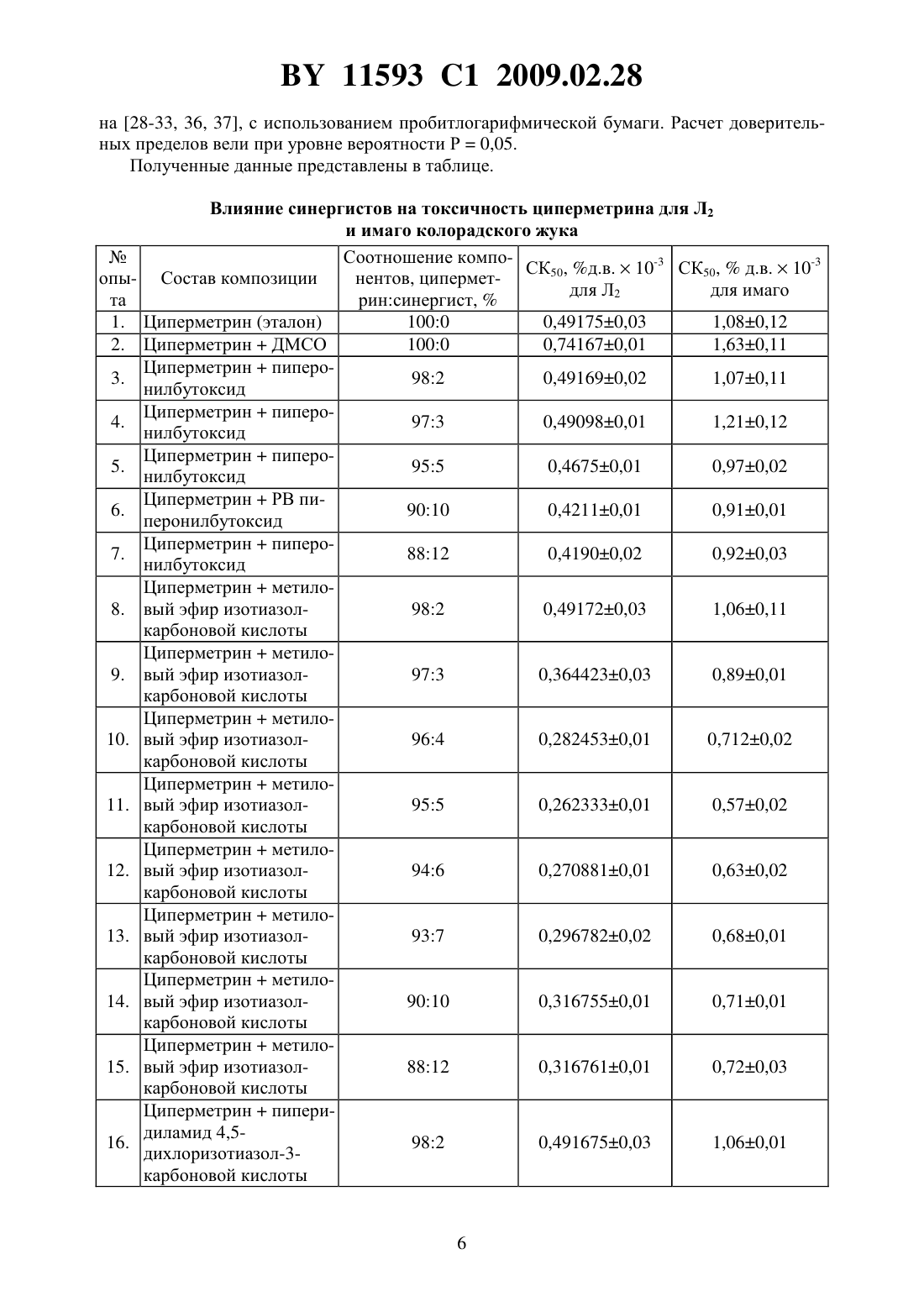
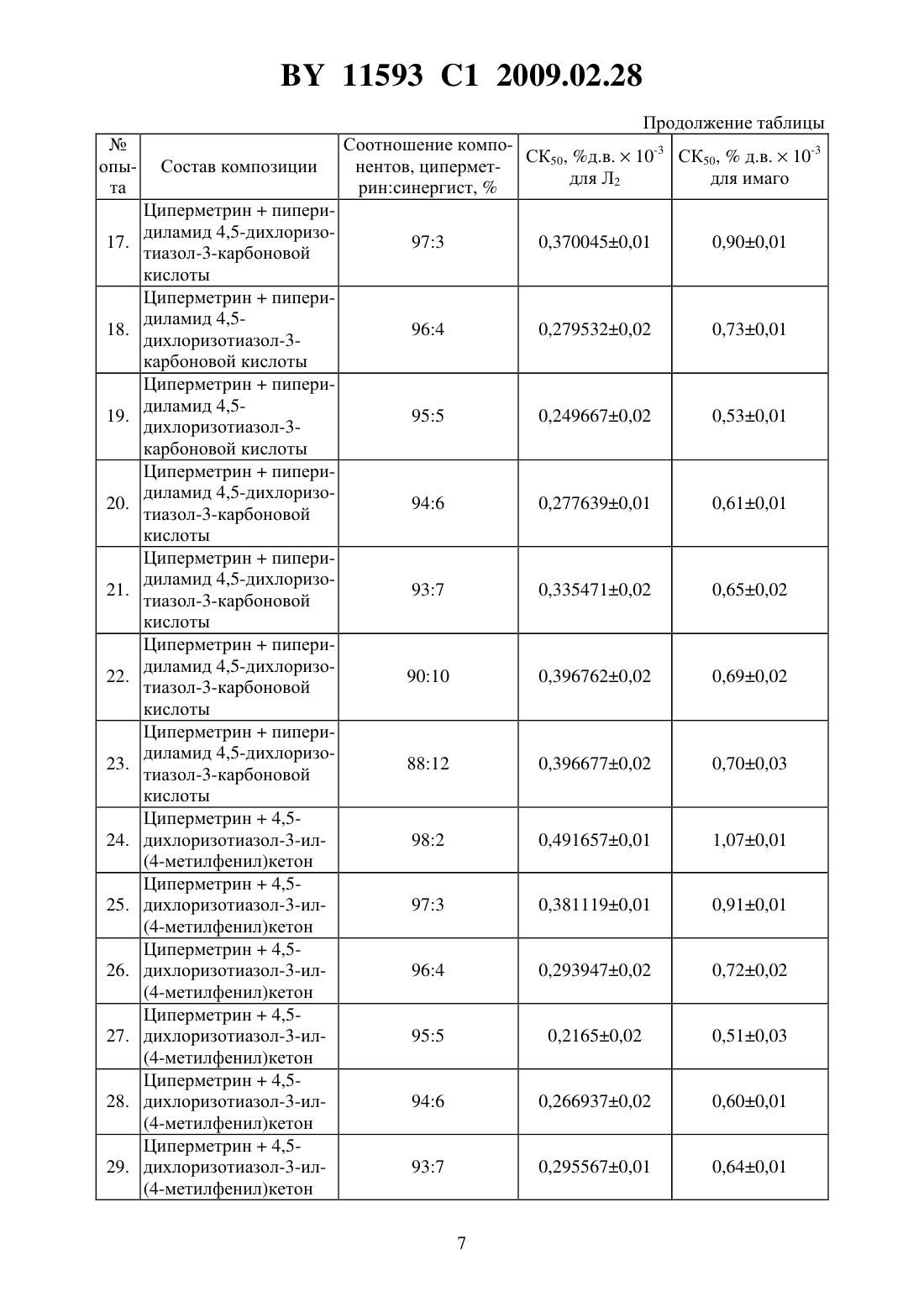
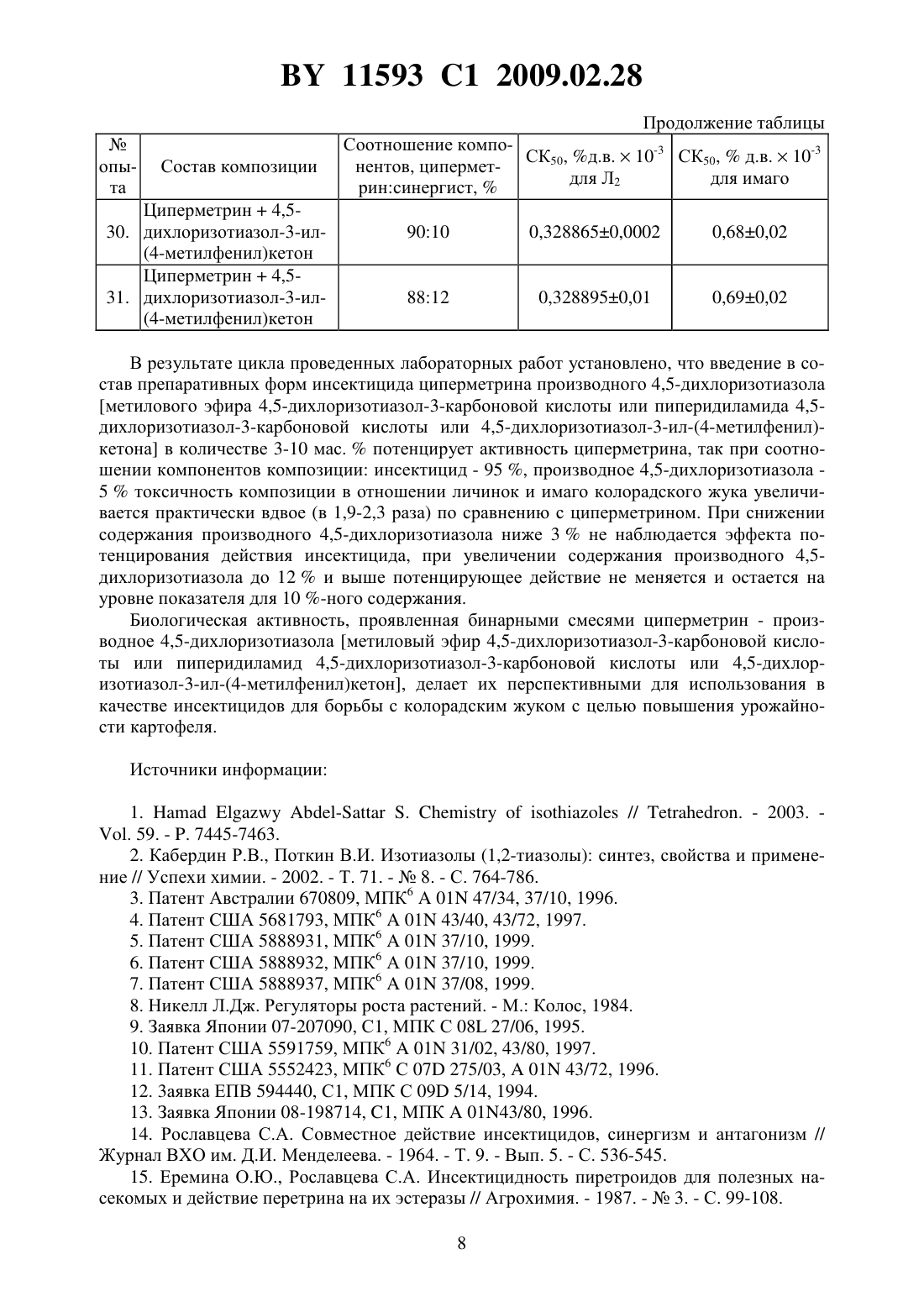
Текст
(71) Заявители Государственное научное учреждение Институт физикоорганической химии Национальной академии наук Беларуси Государственное научное учреждение Институт биоорганической химии Национальной академии наук Беларуси(72) Авторы Поткин Владимир Иванович Быховец Анатолий Иосифович Нечай Наталья Ивановна Золотарь Ромуальда Михайловна Петкевич Сергей Константинович Гончарук Виолетта Михайловна(73) Патентообладатели Государственное научное учреждение Институт физико-органической химии Национальной академии наук Беларуси Государственное научное учреждение Институт биоорганической химии Национальной академии наук Беларуси(56)2176879 1, 2001.4536506, 1985.2045183 1, 1995.2002101803 , 2003. ПОТКИН В.И. и др. Весц Акадэм навук Беларус, сер.хм.навук. - 1994.4. - С. 85-88.(57) Бинарная инсектицидная композиция, содержащая пиретроидный инсектицид циперметрин и синергист, отличающаяся тем, что в качестве синергиста содержит производное 4,5-дихлоризотиазола общей формулы при следующем соотношении компонентов, мас.циперметрин производное 4,5-дихлоризотиазола Предполагаемое изобретение относится к области сельского хозяйства, а именно к применению химических средств в растениеводстве для защиты сельскохозяйственных культур от вредителей. 11593 1 2009.02.28 Интенсификация сельскохозяйственной деятельности в настоящее время невозможна без создания и использования высокоэффективных пестицидных препаратов. Перспективным способом борьбы с резистентными расами вредителей является переход на применение смесей пестицидов с синергистами. Интерес к проблеме, связанной с поиском новых ингибиторов (синергистов) ферментных систем членистоногих разной направленности, способных усиливать токсическое действие инсектоакарицидов, в настоящее время резко возрос. Это обусловлено постоянно растущим числом вредителей сельскохозяйственных культур, развивших резистентность к широко распространенным современным систематически применяемым, главным образом пиретроидным, препаратам. Добавление к пестицидам синергистов является способом повышения их эффективности и продлением сроков применения препаратов. Известными синергистами биоактивных соединений являются производные изотиазола 1,2. 4-Карбметоксиизотиазолы, содержащие в положении 3 замещенную семикарбазонную группу в смеси с известными гербицидами (дикамба, глифосат, 2,4-Д, гербициды на основе феноксипропионовой и феноксимасляной кислот) усиливают их биологическое действие 37. Калиевая соль 3,4-дихлоризотиазол-5-карбоновой кислоты является регулятором роста растений и помимо ростингибирующих свойств способна повышать отзывчивость растений на последующую обработку дефолиантами 8. Ряд замещенных изотиазолов и изотиазолонов входит в состав синергических бактерицидных препаратов 9-13. Известным и одним из первых синергистов, потенцирующих активность пиретринов,является пиперонилбутоксид - ингибитор микросомальных монооксигеназ членистоногих. Исследованиями на комнатной мухе, капустной моли и гусеницах совок была установлена эффективность его комплексного применения с пиретроидными инсектицидами перметрином, циперметрином и эсфенвалератом 14. Важно отметить, что подобный синергетический эффект наблюдался как на чувствительных, так и резистентных популяциях этих видов. На колорадском жуке также было показано усиление токсичности перметрина и эсфенвалерата под действием этого синергиста в зависимости от его концентрации в смесевых комбинациях, однако наблюдаемый эффект относительно невелик 15. Следует также отметить, что используются достаточно большие добавки пиперонилбутоксида к инсектицидам, соотношение синергиста и пиретрина составляют 101 или 51 14. Известна инсектицидная композиция, содержащая в качестве активных ингредиентов смесь циперметрина и фипронила - 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметил-сульфинилпиразола в синергетически активном соотношении 16. Композиция предназначена для борьбы с насекомыми, паразитирующими на зеленых растениях, преимущественно с колорадским жуком. Однако содержание синергиста в композиции также достаточно велико, соотношение циперметрина и фипронила находится в пределах 1,5-4,51 соответственно. Задача изобретения - расширение арсенала средств борьбы с насекомыми-вредителями сельскохозяйственных культур, представителями отряда жесткокрылых, в частности с вредителем картофеля - колорадским жуком , и повышение урожайности картофеля. Поставленная задача решается бинарной композицией, обладающей высокой инсектицидной активностью в отношении личинок и имаго колорадского жука, содержащей пиретроидный инсектицид циперметрин химическое название (е)а-циано-3,3-феноксибензил(е)цис,транс-3-(2,2-дихлорвинил-2,2-диметилциклопропан)-карбоксилат формулы 11593 1 2009.02.28 и синергист, в качестве которого используется производное 4,5-дихлоризотиазола с функциональными группами в положении 3 гетероцикла общей формулы 3 , при следующем соотношении компонентов, мас.циперметрин 90-97 производное 4,5-дихлоризотиазола 3-10. Синтез первых двух производных 4,5-дихлоризотиазола (метилового эфира и пиперидиламида 4,5-дихлоризотиазол-3-карбоновой кислоты), использованных для инсектицидных смесей, нами опубликован ранее 2,17. 4,5-дихлоризотиазол-3-ил-(4-метилфенил)кетон является новым соединением, синтез его не описан. Сведения о применении этих соединений в качестве пестицидов как в индивидуальном виде, так и смесях с другими химическими соединениями отсутствуют. Использованные нами производные дихлоризотиазола являются доступными химическими соединениями. Их получают на основе 4,5-дихлоризотиазол-3-карбоновой кислоты,ранее недоступного региоизомера дихлоризотиазолкарбоновых кислот - известных биоактивных соединений 8. В свою очередь, 4,5-дихлоризотиазол-3-карбоновую кислоту (синтез ее впервые описан нами) получают окислительным гидролизом 4,5-дихлор-3 трихлорметилизотиазола 18, синтез которого основан на открытой нами новой реакции нитросоединений, заключающейся во взаимодействии с элементарной серой 2 нитропентахлор-1,3-бутадиена 19, легко получаемого нитрованием азотной кислотой или нитрующими смесями 2 Н-пентахлор-1,3-бутадиена - продукта дегидрохлорирования димера промышленного многотоннажного и дешевого трихлорэтилена 20. 3 1.2(2)2 2 2. - 22 Метиловый эфир 4,5-дихлоризотиазол-3-карбоновой кислоты получают с препаративным выходом этерификацией 4,5-дихлоризотиазол-3-карбоновой кислоты метанолом, а пиперидиламид 4,5-дихлоризотиазол-3-карбоновой кислоты легко синтезируется действием пиперидина на метиловый эфир 4,5-дихлоризотиазол-3-карбоновой кислоты 17. Методики, примеры синтеза и физико-химические характеристики этих производных изотиазола описаны нами в литературе 17, 18. Синтез ранее неизвестного 4,5-дихлоризотиазол-3-ил-(4-метилфенил)кетона осуществляли ацилированием толуола хлорангидридом 4,5-дихлоризотиазол-3-карбоновой кисло 3 11593 1 2009.02.28 ты в условиях реакции Фриделя-Крафтса в присутствии безводного хлорида алюминия в качестве катализатора в метиленхлориде. Хлорангидрид получали по ранее описанному нами методу 21 действием тионилхлорида на исходную 4,5-дихлоризотиазол-3 карбоновую кислоту. Пример. К комплексу хлорангидрида (5 г, 23 ммоль) и АС 3 (4 г, 30 ммоль) в сухом метиленхлориде (30 мл) прибавляли 8 мл (7 г, 75 ммоль толуола, и перемешивали реакционную смесь 2 ч при 40 С (до прекращения выделения НС), после чего выливали в подкисленную НС воду, отделяли органический слой, промывали содовым раствором, водой и сушили сернокислым магнием. После отгонки растворителя остаток очищали перекристаллизацией из гексана. Получали 4,1 г 4,5-дихлоризотиазол-3-ил(4-метилфенил)кетона. Выход 65 , т.пл. 77-81 С, чистота соединения по данным хромато-масс-спектрометрии 99 . Состав и строение полученного продукта установлены на основании данных ИК,ЯМР 1 Н, масс-спектров и элементного анализа. ИК спектр, , см-1 1659 (СО) 1410,1383, 1353 (изотиазол), 894 (С-С). Спектр ЯМР 1, , м.д. 2,44 с (1, ), 7,31 дд(2 Наром.), 7,92 дд (2 Наром.). Найдено,С 48,90 Н 2,84 С 26,235,2111,52. М 271. 1172. Вычислено,С 48,54 Н 2,60 С 26,055,1511,78. М 272,15. В масс-спектре 4,5-дихлоризотиазол-3-ил(4-метилфенил)кетона имеется группа пиков молекулярного ионов, в которой соотношение интенсивностей основных изотопных составляющих (10065) указывает на наличие двух атомов хлора в ионе 22. Фрагментация молекулы под действием электронного удара протекает характерным для изотиазолов путем с расщеплением изотиазольного цикла 23, 24, отщеплением заместителей (хлора,арильной группы) и однозначно подтверждает строение синтезированного кетона. В наших опытах по оценке биологической активности были использованы известный и применяемый на практике пиретроидсодержащий инсектицид циперметрин, химическое название (е)а-циано-3,3-феноксибензил(е)цис,транс-3-(2,2-дихлорвинил-2,2-диметилциклопропан)-карбоксилат, в смеси с известным синергистом пиперонилбутоксидом и заявляемая бинарная композиция, содержащая циперметрин и производное 4,5-дихлоризотиазола метиловый эфир 4,5-дихлоризотиазол-3-карбоновой кислоты, пиперидиламид 4,5-дихлоризотиазол-3-карбоновой кислоты или 4,5-дихлоризотиазол-3-ил-(4-метилфенил)кетон в количестве 3-10 мас. . Бинарную композицию готовили простым смешением компонентов в заданных соотношениях. При создании композиции из инсектицида и синергиста особое внимание надо обращать на выбор их оптимальных соотношений, так как количество ингибитора должно 11593 1 2009.02.28 быть достаточным для инактивации фермента, в противном случае его потенциальные возможности не будут реализованы в полной мере. Тест-объектами служили личинки и имаго колорадского жука минской популяции. Собранных в природе колорадских жуков помещали в лаборатории в 10 литровые стеклянные сосуды на букеты из листьев картофеля. На дно сосуда помещали увлажненную фильтровальную бумагу, а на стенки прикрепляли гофрированные полоски фильтровальной бумаги для откладки яиц самками жуков. После размещения колорадских жуков, верх сосуда затягивали мельничным газом. Жуки активно питались и спаривались. Яйцекладки колорадского жука на листьях картофеля и фильтровальных бумажках регулярно собирали и помещали по одной в чашки Петри на увлажненный фильтр. Через 4 дня, в каждую чашку помещали свежий лист картофеля, чтобы отродившиеся личинки могли питаться. В дальнейшем корм менялся ежедневно. Личинки колорадского жука содержались в чашках Петри до нужного для эксперимента возраста Л 1-Л 4. Температура воздуха в лабораторном помещении поддерживалась на уровне 2123 С, относительная влажность воздуха 78-80 , световой день - 18 ч 25, 26. Оценка токсичности ядов производится на основе определения дозы (концентрации),вызывающей отравление определенной части популяции вредных организмов. Стандартными токсикологическими параметрами действия препарата служат величины СК 50 и СК 95, т.е. концентрации действующего вещества (д.в.), убивающие соответственно 50 и 95 особей данного вида. Определение величины СК 50 и СК 95 велось по стандартным методикам Методические рекомендации по выявлению инсектоакарицидного, росторегулирующего и других типов воздействия химических соединений на членистоногих,Методические рекомендации по определению биологической активности жидких инсектицидов контактного действия, Методические рекомендации для энтомотоксикологических исследований Природная чувствительность членистоногих к пестицидам и др. 27-33. В основе методик лежит изучение реакции вредителя на серию дозировок какого-либо препарата - от минимальной, вызывающей гибель 5-10 чувствительных особей, до максимальной, при использовании которой гибнет 90 особей и более. В целях стандартизации опытов все расчеты ведутся по действующему веществу (д.в.) препарата, и употребляется одинаковая схема разведения, так называемая логарифмическая 0,10,05- 0,025- 0,01- 0,005 и т.д. Отравление имаго и личинок проводили контактно-кишечным способом. При контактно-кишечном способе отравления насекомые вместе с листом картофеля обрабатывались необходимой концентрацией д.в. препарата 25, 27-34. Для эксперимента использовали откалиброванных по весу имаго и по возрасту и весу личинок на второй день после линьки. Отравление подопытных насекомых проводили всегда в одно и то же время суток в 10 часов утра - в период максимальной активности питания 26, 35. Лабораторные опыты закладывались в 6 повторностях, в каждой повторности - по 80 личинок необходимого возраста. Гибель личинок учитывали через одни, три, пять суток после обработки. Контролем служили личинки, обработанные чистым растворителем и воспитанные в аналогичных адекватных условиях. Как правило, прямое токсическое действие препарата проявляется постепенно через более или менее продолжительный отрезок времени, при этом, чем ниже концентрация раствора, тем медленнее идет процесс отмирания. В каждом конкретном случае (по дням эксперимента) подсчет погибших и живых подопытных насекомых ведется в опыте и в контроле, а затем высчитывают для каждой повторности суммарный процент гибели насекомых и среднее его значение по варианту с поправкой на контроль. Для этого используется формула Аббота 36, 37. После серии испытаний проводился расчет среднесмертельных концентраций (СК 50),обеспечивающих 50 гибель подопытных насекомых, по методу Литчфилда и Уилкоксо 5 11593 1 2009.02.28 на 28-33, 36, 37, с использованием пробитлогарифмической бумаги. Расчет доверительных пределов вели при уровне вероятности Р 0,05. Полученные данные представлены в таблице. Влияние синергистов на токсичность циперметрина для Л 2 и имаго колорадского жука Соотношение компоСК 50, д.в.10-3 СК 50,д.в.10-3 Состав композиции нентов, циперметдля Л 2 для имаго ринсинергист,Циперметрин (эталон) 1000 0,491750,03 1,080,12 ЦиперметринДМСО 1000 0,741670,01 1,630,11 Циперметринпиперо 982 0,491690,02 1,070,11 нилбутоксид Циперметринпиперо 973 0,490980,01 1,210,12 нилбутоксид Циперметринпиперо 955 0,46750,01 0,970,02 нилбутоксид ЦиперметринРВ пи 9010 0,42110,01 0,910,01 перонилбутоксид Циперметринпиперо 8812 0,41900,02 0,920,03 нилбутоксид Циперметринметиловый эфир изотиазол 982 0,491720,03 1,060,11 карбоновой кислоты Циперметринметиловый эфир изотиазол 973 0,3644230,03 0,890,01 карбоновой кислоты Циперметринметиловый эфир изотиазол 964 0,2824530,01 0,7120,02 карбоновой кислоты Циперметринметиловый эфир изотиазол 955 0,2623330,01 0,570,02 карбоновой кислоты Циперметринметиловый эфир изотиазол 946 0,2708810,01 0,630,02 карбоновой кислоты Циперметринметиловый эфир изотиазол 937 0,2967820,02 0,680,01 карбоновой кислоты Циперметринметиловый эфир изотиазол 9010 0,3167550,01 0,710,01 карбоновой кислоты Циперметринметиловый эфир изотиазол 8812 0,3167610,01 0,720,03 карбоновой кислоты Циперметринпиперидиламид 4,5982 0,4916750,03 1,060,01 дихлоризотиазол-3 карбоновой кислоты Состав композиции Циперметринпиперидиламид 4,5-дихлоризотиазол-3-карбоновой кислоты Циперметринпиперидиламид 4,5 дихлоризотиазол-3 карбоновой кислоты Циперметринпиперидиламид 4,5 дихлоризотиазол-3 карбоновой кислоты Циперметринпиперидиламид 4,5-дихлоризотиазол-3-карбоновой кислоты Циперметринпиперидиламид 4,5-дихлоризотиазол-3-карбоновой кислоты Циперметринпиперидиламид 4,5-дихлоризотиазол-3-карбоновой кислоты Циперметринпиперидиламид 4,5-дихлоризотиазол-3-карбоновой кислоты Циперметрин 4,5 дихлоризотиазол-3-ил(4-метилфенил)кетон Циперметрин 4,5 дихлоризотиазол-3-ил(4-метилфенил)кетон Циперметрин 4,5 дихлоризотиазол-3-ил(4-метилфенил)кетон Циперметрин 4,5 дихлоризотиазол-3-ил(4-метилфенил)кетон Циперметрин 4,5 дихлоризотиазол-3-ил(4-метилфенил)кетон Циперметрин 4,5 дихлоризотиазол-3-ил(4-метилфенил)кетон В результате цикла проведенных лабораторных работ установлено, что введение в состав препаративных форм инсектицида циперметрина производного 4,5-дихлоризотиазола метилового эфира 4,5-дихлоризотиазол-3-карбоновой кислоты или пиперидиламида 4,5 дихлоризотиазол-3-карбоновой кислоты или 4,5-дихлоризотиазол-3-ил-(4-метилфенил)кетона в количестве 3-10 мас.потенцирует активность циперметрина, так при соотношении компонентов композиции инсектицид - 95 , производное 4,5-дихлоризотиазола 5 токсичность композиции в отношении личинок и имаго колорадского жука увеличивается практически вдвое (в 1,9-2,3 раза) по сравнению с циперметрином. При снижении содержания производного 4,5-дихлоризотиазола ниже 3 не наблюдается эффекта потенцирования действия инсектицида, при увеличении содержания производного 4,5 дихлоризотиазола до 12 и выше потенцирующее действие не меняется и остается на уровне показателя для 10 -ного содержания. Биологическая активность, проявленная бинарными смесями циперметрин - производное 4,5-дихлоризотиазола метиловый эфир 4,5-дихлоризотиазол-3-карбоновой кислоты или пиперидиламид 4,5-дихлоризотиазол-3-карбоновой кислоты или 4,5-дихлоризотиазол-3-ил-(4-метилфенил)кетон, делает их перспективными для использования в качестве инсектицидов для борьбы с колорадским жуком с целью повышения урожайности картофеля. Источники информации 1.- .// . - 2003. . 59. - . 7445-7463. 2. Кабердин Р.В., Поткин В.И. Изотиазолы (1,2-тиазолы) синтез, свойства и применение // Успехи химии. - 2002. - Т. 71. -8. - С. 764-786. 3. Патент Австралии 670809, МПК 601 47/34, 37/10, 1996. 4. Патент США 5681793, МПК 601 43/40, 43/72, 1997. 5. Патент США 5888931, МПК 601 37/10, 1999. 6. Патент США 5888932, МПК 6 А 01 37/10, 1999. 7. Патент США 5888937, МПК 601 37/08, 1999. 8. Никелл Л.Дж. Регуляторы роста растений. - М. Колос, 1984. 9. Заявка Японии 07-207090, С 1, МПК С 08 27/06, 1995. 10. Патент США 5591759, МПК 601 31/02, 43/80, 1997. 11. Патент США 5552423, МПК 6 С 07 275/03,01 43/72, 1996. 12. 3 аявка ЕПВ 594440, С 1, МПК С 09 5/14, 1994. 13. Заявка Японии 08-198714, 1, МПК 0143/80, 1996. 14. Рославцева С.А. Совместное действие инсектицидов, синергизм и антагонизм // Журнал ВХО им. Д.И. Менделеева. - 1964. - Т. 9. - Вып. 5. - С. 536-545. 15. Еремина О.Ю., Рославцева С.А. Инсектицидность пиретроидов для полезных насекомых и действие перетрина на их эстеразы // Агрохимия. - 1987. -3. - С. 99-108. 8 11593 1 2009.02.28 16. Патент РФ 2176879, МПК 6 А 01 53/08, 43/56, 2001 (прототип). 17. Поткин В.И., Нечай Н.И., Кабердин Р.В. Синтез функциональных производных изотиазола // Весц АНБ Сер. хм. навук. - 1994. -4. - С. 85-88. 18. Кабердин Р.В., Поткин В.И., Ольдекоп Ю.А. Синтез и некоторые реакции 3-трихлорметил-4,5-дихлоризотиазола // Журнал органической химии. - 1990. - Т. 26. - Вып. 7. С. 1560-1566. 19. Кабердин Р.В., Поткин В.И., Ольдекоп Ю.А. Синтез 3-трихлорметил-4,5 дихлоризотиазола из 2-нитропентахлор-1,3 -бутадиена и элементной серы новая реакция нитросоединений // Доклады АН СССР. - 1988. - Т. 300. -5. - С. 1133-1135. 20. Кабердин Р.В., Поткин В.И. Трихлорэтилен в органическом синтезе // Успехи химии. - 1994. - Т. 63. -8. - С. 673-693. 21. Нечай Н.И., Дикусар Е.А., Поткин В.И., Кабердин Р.В. Синтез амидов и эфиров 4,5-дихлоризотиазол-3-карбоновой кислоты // Журнал органической химии. - 2004. - Т. 40. Вып. 7. - С. 1050-1055. 22. Тахистов В.В. Практическая масс-спектрометрия органических соединений. - Л. Изд-во ЛГУ, 1977. - 268 с. 23.Т.. .3- // . 1968. - . 24. -20. - . 6237-6258. 24..-.,.,..// . . . . - 1969. - . 268.1. - . 12-14. 25. Быховец С.Л. Колорадский жук // Природная чувствительность членистоногих к пестицидам Метод. рек. для энтом. исслед. - Л., 1986. - С. 50-53. 26. Кожанчиков И.В. Методы исследования экологии насекомых. - М.,1961.286 с. 27. Быховец А.И., Быховец С.Л., Токсичность синтетических перетроидов для колорадского жука // Химия в сел. хоз-ве. - 1981. -8. - С. 34-36 28. Выявление инсектоакарицидного, росторегулирующего и других типов воздействия химических соединений на членистоногих. Методические рекомендации. - Чебоксары,1982. - С. 65. 29. Природная чувствительность членистоногих к пестицидам. Методические рекомендации для энтомотоксикологических исследований. - Л., 1986. - 62 с. 30. Определение резистентности вредителей сельскохозяйственных культур и зоофагов к пестицидам. Методические указания. - М., 1990. - С.65 31. Методические рекомендации по определению устойчивости вредителей сельскохозяйственных культур и энтомофагов к пестицидам. - М. ВАСХНИЛ, 1977. - 32 с. 32. Методические рекомендации по определению биологической активности жидких инсектицидов контактного действия - М., 1979. - 19 с. 33. Методические указания по определению устойчивости вредителей и возбудителей болезней сельскохозяйственных культур и энтомофагов к пестицидам. - М., 1984. - 68 с. 34. Быхавец С.Л. Даследаванне хуткасц развццястраты рэзстэнтнасц да нсектыцыдау у каларадскага жука // Весц АН БССР Сер. с.-г. навук. - 1987. - 4. - С. 74-77. 35. Колорадский картофельный жук (.) / Под ред. Р.С. Ушатинской. - М., 1985. - 375 с. 36. Беленький М.Б. Элементы количественной оценки фармакологического эффекта. Рига Изд. АН Латв. ССР, 1963. - 195 с. 37. Гар К.А. Методы испытания токсичности и эффективности инсектицидов. - М.,1963. - 288 с. Национальный центр интеллектуальной собственности. 220034, г. Минск, ул. Козлова, 20. 9
МПК / Метки
МПК: A01P 7/04, A01N 43/72, A01N 53/00
Метки: композиция, бинарная, инсектицидная
Код ссылки
<a href="https://by.patents.su/9-11593-binarnaya-insekticidnaya-kompoziciya.html" rel="bookmark" title="База патентов Беларуси">Бинарная инсектицидная композиция</a>
Предыдущий патент: Противопаразитарный препарат
Следующий патент: Гидравлическая система мобильной машины